-Рубрики
- Медицина (88)
- Основы веры (53)
- История (42)
- Информатика (14)
- Интересно (11)
- Опера (9)
- Психиатрия (8)
- Психотроника (8)
- Мультимедиа (6)
- Поэзия (6)
- Атеизм (5)
- Лекарства (5)
- Эзотерика (5)
- Психология (2)
- Притчи (1)
- Мысли (1)
- Анатомия (0)
-Подписка по e-mail
-Поиск по дневнику
-Интересы
-Друзья
-Постоянные читатели
-Статистика
Прощение выше мщения, а доброта сильнее гнева
МОЛИТВА ОПТИНСЬКИХ СТАРЦIВ |
Господи, дай менi зустрiти з душевним спокоєм усе, що принесе менi цей день. Дай менi цілковито вiддатися на волю Твою святу. На всяк час дня цього в усьому настав мене i пiдтримай мене, Господи. Якi б я не дістав звiстки, навчи мене приймати їх зi спокiйною душею i твердим переконанням, що на все Свята воля Твоя. У всiх дiлах моїх i словах керуй думками моїми i почуттями. У всiх непередбачених випадках не дай менi, забути, що все Ти посилаєш. Навчи мене просто i мудро ставитись до всiх людей, нiкого не ображаючи, анi засмучуючи. Господи, дай менi силу перенести втому i всi подiї цього дня. Керуй моєю волею i навчи мене молитись, вiрити, надіятись, терпiти, прощати i любити.
|
СУДИННІ ЗАХВОРЮВАННЯ ГОЛОВНОГО ТА СПИННОГО МОЗКУ(прод.) |
МИНУЩІ ПОРУШЕННЯ МОЗКОВОГО КРОВООБІГУ
Минущі порушення мозкового кровообігу (МПМК) - це гостро виникаючі на тлі основного захворювання дисциркуляційні явища у головному мозку, що супроводжуються тимчасовими загальномозковими та вогнищевими симптомами із зворотнім їх розвитком протягом 24 годин. Це одна із найбільш частих клінічних форм гострого порушення мозкового кровообігу. Такі хворі у неврологічних стаціонарах складають близько 20% від усіх пацієнтів із судинними захворюваннями головного мозку.
До минущих порушень мозкового кровообігу відносять транзиторні ішемічні атаки (ТІА)(приблизно 1/3 усіх випадків МПМК) і гіпертонічні кризи (2/3 усіх МПМК), незалежно від того, проявляються вони загальномозковими чи вогнищевими симптомами.
Гіпертонічні кризи (ГК) найчастіше виникають при гіпертонічній хворобі, нирковій та наднирковій гіпертонії, ТІА - при атеросклерозі, стенозуючих ураженнях магістральних артерій голови, захворюваннях серця (вади серця, пролапс мітрального клапана, інфаркт міокарда); значно рідше вони зустрічаються при васкулітах різної етіології (інфекційно-алергічних, сифілітичних), при системних васкулітах (вузликовий периартеріїт) тощо. Значно меншу роль у їхньому розвитку відіграють цукровий діабет, здавлювання остеофітами хребетних артерій.
ТРАНЗИТОРНІ ІШЕМІЧНІ АТАКИ
ПАТОГЕНЕЗ. Основними патогенетичними чинниками ТІА є:
тромбемболічні та
гемодинамічні, які тісно пов'язані між собою.
1. Найбільш частими чинниками ТІА вважають тромбемболічні, тобто мікроемболію мозкових судин. Розрізняють артеріогенні та кардіогенні мікроемболи.
а) Артеріогенні мікроемболи являють собою дрібні частинки, що відірвалися від пристінкових тромбів при розпаді атеросклеротичних бляшок. Важливу роль у розвитку ТІА відіграють артеріоартеріальні емболії, які є конгломератами еритроцитів, тромбоцитів, що утворюються у зміненій ділянці стінки великих судин і з током крові через магістральні артерії голови потрапляють у дистальні судини невеликого калібру, кінцеві гілки артеріальної системи, частіше кіркові гілки мозкових артерій, викликаючи їх тимчасову оклюзію. Подразнюючи ендотелій, вони спричиняють спазм судин і підвищують проникність їх стінок із наступним розвитком периваскулярного набряку мозкової тканини, що супроводжується виникненням вогнищевих симптомів. Утворенню цих тромбів сприяють зміни:
- фізико-хімічних властивостей крові
а) підвищення в'язкості, агрегації та адгезії тромбоцитів і еритроцитів,
б) зниження їх здатності до деформації,
- біохімічних властивостей крові
а) гіперліпідемія,
б) гіперглікемія,
в) діабетичний кетоз.
Тромбоцитарні емболи крихкі, легко піддаються лізису, що і зумовлює зворотній розвиток неврологічного дефіциту.
б) Кардіогенні мікроемболи спричинюють ТІА у хворих з:
- миготливою аритмією,
- вадами серця,
- інфарктом міокарду,
- у хворих на ревматичний ендокардит з пролапсом мітрального клапану.
2. ТІА також зумовлюють мікротромбози при захворюваннях крові:
- поліцитемія,
- мікроглобулінемія,
- тромбоцитози.
3. Одним з механізмів ТІА може бути атеросклеротичний стеноз мозкових чи магістральних судин голови, особливо у поєднанні з:
- падінням артеріального тиску,
- порушенням серцевого ритму,
- інфарктом міокарду,
- кровотечею.
Сам стеноз може бути не лише причиною МПМК, але й джерелом "вторинних" емболій.
4. ТІА можуть бути викликані тромбозом або облітерацією магістральної артерії на шиї, коли добре розвинута сітка колатерального кровообігу і артеріальне коло великого мозку сприяють відновленню кровотоку дистальніше місця оклюзії та попередженню стійкої ішемії мозкової речовини.
5. Нерідко ТІА виникають за механізмом “обкрадання”. Наприклад, при оклюзії підключичної артерії кровопостачання руки здійснюється через вертебро-базилярний басейн головного мозку шляхом ретроградного перетоку в ущерб кровопостачанню головного мозку. При цьому, клінічно звучить симптоматика басейну інтактної судини.
6. Важливу роль у патогенезі ТІА відіграють уроджені стенози, патологічна звивистість та гіпоплазії чи інші аномалії розвитку магістральних артерій голови.
7. Здебільшого, причиною ТІА у вертебро-базилярному басейні буває стиснення хребетної артерії остеофітами при шийному остеохондрозі.
8. Певну роль у виникненні ТІА відіграє механізм судинної мозкової недостатності, коли виникає невідповідність між потребою мозку та повноцінним забезпеченням тканини кров'ю (наприклад, при серцевій слабкості, різкому зниженні, артеріального тиску, внутрішній кровотечі тощо)
9. Не менш важливе значення в патогенезі ТІА мають кисневе голодування, порушення церебрального метаболізму.
КЛІНІКА. ТІА (або транзиторні ішемії) розвиваються у більшості випадків гостро, раптово і значно рідше - поступово з повільним розвитком симптомів. Як правило, маніфестують вогнищевою неврологічною симптоматикою, яка значно переважвє над загальномозковими проявами. Іншими словами, ТІА є регіональними МПМК. Клінічні прояви їх різноманітні і залежать від локалізації і тривалості дисциркуляційних розладів.
Розрізняють дві групи симптомів при ТІА:
а) вогнищеві
б) загальномозкові.
Загальномозкові симптоми, якщо вони є, проявляються:
- головним болем,
- запамороченням несистемного чи системного характеру,
- нудотою, блюванням,
- відчуттям вираженої загальної слабкості,
- пеленою перед очима,
- короткочасною втратою свідомості.
Вогнищеві, або регіональні, залежать від судинного басейну, в якому виникає дисциркуляція.
ТІА в каротидному басейні (зустрічається у 30 % усіх випадків ТІА) клінічно проявляються симптомами дисфункції коркових відділів мозку. Каротидний - це басейн внутрішніх сонних артерій, від яких відходять: очна артерія, передня та середня мозкові артерії. Зона кровопостачання - передній відділ лобної частки, внутрішня поверхня півкулі до тім'яно-потиличної борозни, на конвекситальній поверхні мозку кора лобної, тім'яної та скроневої часток, підкоркові ядра, внутрішня капсула. При дисциркуляції в системі внутрішньої сонної артерії найбільш частими бувають наступні вогнищеві симптоми:
1. суб'ктивні (відчуття затерпання. оніміння, поколювання на обличчі або в руці чи нозі) та об'єктивні чутливі розлади (гіпестезія поверхневої чутливості в ділянці обличчя, руки чи ноги, іноді зниження глибокої чутливості в пальцях кисті чи ступні)
2. рухові порушення такі, як центральний парез руки чи ноги, окремих пальців на кисті чи ступні, з підвищенням сухожилкових рефлексів, зниженням шкірних, патологічними знаками Бабінськогоо, Россолімо, тощо. Геміпарез чи геміплегія виникають лише у вкрай важких випадках.
3. При ураженні лівої півкулі мозку виникають розлади мови - минуща афазія або коркова дизартрія, які поєднуються із чутливими та руховими розладами у правих кінцівках.
4. При ТІА, зумовлених закупоренням або стенозом внутрішньої сонної артерії на шиї, розвивається минущий перехресний оптико-пірамідний синдром Ласко-Радовича: зниження зору або сліпота на стороні ураження та слабкість кінцівок на протилежному боці. Іноді зниження зору на одне око поєднується лише з гіперрефлексією контрлатеральних кінцівок.
5. При наявності патології магістральних судин голови ТІА можуть маніфестувати фокальними джексонівськими руховими та чутливими нападами.
ТІА у системі вертебро-базилярного басейну складають майже 70 % усіх випадків ТІА. Так, як вертебро-базилярний басейн забезпечує кровопостачання стовбуга головного мозку, мозочка, кори потиличної частки, медіобазальні структури скроневих часток мозку, то клінічно спостерігається відповідна симптоматика:
1. вестибулярний синдром - проявляється:
- системним запамороченням,
- шумом у голові та вухах,
- головним болем у потиличній ділянці,
- "пеленою" перед очима,
- нудотою,
- блюванням,
- ністагмом,
- розладами рівноваги;
2. мозочково-стовбуровий синдром - проявляється порушенням координації і синергії рухів та рівноваги (а саме статики);
3. синдром окорухових розладів - парез погляду, розлади конвергенції, диплопія, косоокість;
4. бульбарний синдром - порушення ковтання, голосу та вимови;
5. альтернуючі синдроми зустрічаються відносно рідко;
6. зорові розлади у вигляді:
- фотопсій,
- геміанопсій,
- метаморфопсій,
- невиразності,
- дефектів поля зору,
- появи оптичних феноменів (кольорів, фігур).
7. атонічно-адинамічний синдром - виникає при раптовій ішемії ретикулярної формації та нижніх олив у ділянці довгастого мозку і проявляється нападами раптового зниження м'язового тонусу, що призводить до падіння хворого без втрати свідомості. Ці напади найчастіше виникають при патології шийного відділу хребта у момент різкого повороту або закидання голови назад. Нерідко виникає синдром Унтерхарншайдта, коли втрата м'язового тонусу поєднується із втратою свідомості на короткий час (синдром Сикстинської капели - виникає у туристів похилого віку під час огляду фресок Мікельанжело на куполі Сикстинської капели у Римі. Внаслідок різкого перерозгинання шиї змінюється кровоток у хребетних артеріях).
8. корсаківський синдром - виникає при ішемії медіобазальних структур скроневої ділянки мозку і проявляється атаками тимчасових розладів пам'яті на біжучі події з конфабуляторним компонентом та дезорієнтацією.
9. пароксизмальний гіперсомнічний і катаплексичний синдроми та вегетативно-судинні розлади виникають при ішемії гіпоталамічних структур.
10. синдром скроневої епілепсії.
11. ураження різних структур лімбічної системи проявляеться змінами з боку емоційно-вольової сфери:
- підвищена втомлюваність,
- зниження працездатності,
- подразливість,
- часто пригнічений настрій, апатія,
- інколи пароксизмальне підвищення артеріального тиску.
12. синдром підключичного обкрадання - виникає при стенозі підключичної артерії, внаслідок чого кровоток в хребетній артерії стає ретроградним, забезпечуючи кровопостачанняруки ("рука-провокатор"). При цьому синдром клінічно проявляється ішемією стовбура: втрата свідомості та інші симптоми вертебро-базилярної недостатності.
Нерідко зустрічаються одночасно атеросклеротичне ураження сонної і хребетної артерій, особливо у людей похилого віку. При множинному ураженні магістральних судин голови можуть виникати симптоми порушення кровообігу як у сонній, так і в хребетно-основній системі. Тому, крім каротидних та вертебро-базилярних ішемічних кризів виділяють поєднані минущі порушення мозкового кровообігу , такі як коронарно-церебральні, аорто-церебральні, гепато-церебральні, холецисто-церебральні та ін.
Необхідно зазначити, що ТІА мають тривалість від декількох хвилин до доби, проте найчастіше вони продовжуються 10-15 хвилин. Нерідко зустрічаються випадки, коли загальномозкова та вогнищева симптоматика зникає протягом декількох наступних днів. Для ТІА характерні рецидиви, коли протягом року атаки повторюються до 3-5 разів. Ще одна особливість, про яку слід згадати, це більша частота ТІА у вертебро-базилярному басейні і найбільша їх повторюваність при локалізації в хребетно-базилярному басейні на відміну від ТІА у каротидному басейні. Проте прогноз при ТІА в системі сонної артерії завжди серйозніший, оскільки протягом одного, рідше двох років після першої атаки розвивається інсульт. Несприятливим є прогноз минущого порушення мозкового кровообігу, якщо воно виникає на тлі кардіальної патології з порушенням ритму серцевої діяльності. Повторюваність ТІА декілька разів на добу свідчить про патологію магістральних артерій голови.
Діагноз ТІА потрібно диференціювати із синкопальними пароксизмами (зомління). Синкопальні пароксизми виникають, як правило, у хворих молодого віку з вегетативною дисфункцією, зі схильністю до ортостатичних реакцій. ТІА у вертебро-базилярній системі часто супроводжуються нападами системного запаморочення, яке потрібно відрізняти від ураження лабіринту, хвороби Меньєра. Встановленню діагнозу допомагають дані анамнезу та отоневрологічного обстеження. Виявлення додаткових неврологічних симптомів (зорові, слухові, мозочкові розлади, порушення чутливості) свідчить про судинний генез захворювання.
ГІПЕРТОНІЧНІ ЦЕРЕБРАЛЬНІ КРИЗИ
Гіпертонічні церебральні кризи складають13-15% від усіх гострих порушень мозкового кровообігу, а також 2/3 хворих МПМК.
ПАТОГЕНЕЗ. До недавнього часу більшість клініцистів дотримувались тієї точки зору, згідно якої у відповідь на раптове підвищення артеріального тиску при гіпертонічних кризах виникає спазм судин головного мозку, що призводить до дефіциту мозкового кровопостачання. Результати експериментальних досліджень останніх десятиліть довели, що вазоспазм у момент підвищення артеріального тиску є проявом реакції авторегуляції мозкового кровообігу. Вазоспазм захищає головний мозок від надлишкової перфузії. При швидкому і більш значному підвищенні артеріального тиску (більше 180-200 мм рт. ст.) авторегуляційні механізми не компенсують зростання перфузійного тиску, внаслідок чого виникає зрив реакції авторегуляції мозкового кровообігу і гіперемія головного мозку, створюються умови для набряку мозку, дефіциту мозкового кровообігу та розвитку ішемії тканин мозку. Таким чином, у патогенезі церебральних гіпертонічних кризів виняткове значення має єдиний чинник зриву авторегуляції мозкового кровообігу.
КЛІНІКА ГІПЕРТОНІЧНИХ КРИЗІВ. Як уже зазначалось, гіпертонічні кризи є проявом загострення гіпертонічної хвороби чи симптоматичної артеріальної гіпертензії, коли у момент різкого підвищення артеріального тиску розвивається гіперемія та набряк мозку, які супроводжуються появою загальномозкових і рідше вогнищевих симптомів, що зникають протягом доби. Гіпертонічний церебрально-судинний криз супроводжується, крім значного підйому артеріального тиску:
- головним болем,
- відчуттям важкості у голові,
- психомоторним збудженням,
- іноді потьмаренням свідомості,
- почервонінням обличчя,
- серцебиттям,
- затрудненням дихання,
- болем у ділянці серця,
- нудотою, блюванням,
- часом розвиваються епілептичні напади.
Спостерігаються також різко виражені дифузні вегетативні порушення:
- пітливість,
- відчуття похолодання кінцівок,
- зміна частоти дихання, пульсу,
- зміна кольору обличчя.
Виділяють три типи кризів у залежності від типу системної гемодинаміки:
1. гіперкінетичний тип - супроводжується збільшенням серцевого викиду зі зростанням серцевого індексу більше 4,5 л/хвґм2 при нормальному або дещо зниженому периферичному судинному опорі;
2. гіпокінетичний тип - супроводжується неадекватним зниженням серцевого викиду і зменшенням серцевого індексу до 2,8 л/хвґм2 при, відповідно, різкому зростанні загального периферичного опору;
3. еукінетичний тип - розвивається при нормальному серцевому викиді (серцевий індекс суттєво не змінюється) та помірно підвищеному загальному периферичному опорі.
Для адекватного лікування гіпертонічного кризу важливо виявити його основний механізм, а тому розпізнавання типу церебрально-судинного кризу є необхідним.
Клінічно гіпертонічний криз гіперкінетичного типу проявляється наступними ознаками:
1. характерним є швидкий розвиток кризу на фоні доброго самопочуття, без передвісників,
2. підвищується переважно систолічний тиск (більше 180-200 мм рт. ст.),
3. загальномозкові симптоми виражені різко: психомоторне збудження, різкий пульсуючий головний біль з нудотою та блюванням, мерехтіння мушок перед очима,
4. різко виражені вегетативні прояви: затруднене дихання, почервоніння чи блідість шкіри, поліурія, емоційна лабільність, жар та тремтіння у всьому тілі,
5. незначна тривалість кризу, до декількох годин,
6. розвивається не лише у хворих на гіпертонічну хворобу, але й при деяких формах симптоматичної артеріальної гіпертензії.
Особливості кризу гіпокінетичного типу:
1. поступовий розвиток на тлі тривалої гіпертензії, на пізніх стадіях гіпертонічної хвороби,
2. підвищується діастолічний тиск,
3. з'являються виражені зміни на ЕКГ: сповільнення внутрішлуночкової провідності, зниження сегменту ST,
4. при цій формі кризу існує велика небезпека розвитку ішемічного інсульту.
Клінічні особливості кризу еукінетичного типу:
1. швидкий розвиток,
2. підвищується і систолічний, і діастолічний тиск,
3. з'являються явища гострої недостатності лівого шлуночка, набряк легень.
Залежно від стану церебральної гемодинаміки, гіпертонічні кризи поділяють на:
1. гіперволемічний тип - пульсове кровонаповнення більше 0,12 Ома,
2. нормоволемічний тип - пульсове кровонаповнення коливається в межах 0,09-0,11 Ома,
3. гіповолемічний тип - пульсове кровонаповнення менше 0,08 Ома.
За тривалістю гіпертонічні кризи ділять на:
а) легкі - тривають до 1 години,
б) середньої важкості - тривають декілька годин,
в) важкі - тривають більше 5-6 годин, але не більше доби.
Критерії частоти:
а) при легких кризах: часті - більше 4 разів на місяць, середньої частоти - 3-4 рази на місяць, рідкі - 1-2 рази на місяць.
б) середньої важкості і важкі: часті - більше 5 разів на рік, середньої частоти - 3-5 разів на рік, рідкі - 1-2 рази на рік.
Вогнищевих симптомів ураження головного мозку при церебрально-судинних кризах здебільшого не буває, але можуть виявлятись ригідність потиличних м’язів, симптом Керніга, підвищення тиску спинномозкової рідини.
ДІАГНОСТИКА МПМК. При діагностуванні проминучих розладів мозкового кровообігу діагноз легкої транзиторної ішемічної атаки чи гіпертонічного кризу, коли симптоми порушення кровообігу тривають недовго, від декількох хвилин до години, не виникає затрудненнь. Проте, коли у хворого раптово з'являється загальномозкова та вогнищева симптоматика дизгемії і триває декілька годин, діагноз динамічного розладу мозкового кровообігу виставляється ретроспективно, уже після зникнення клінічних симптомів, так як у цьому випадку невідомо, чи не розвинеться інсульт. Оскільки транзиторна ішемічна атака чи гіпертонічний криз часто є першим проявом патології серцево-судинної системи, важливим є вияснення основного судинного захворювання, яке призвело до виникнення МПМК. З метою обстеження судинних хворих використовують наступні спеціальні методи обстеження:
1. Ультразвукова доплерографія - визначає наявність оклюзій чи стенозів у магістральних артеріях голови та шиї, у інтракраніальних судинах, а також стан колатерального кровотоку.
2. Реоенцефалографія з функціональними пробами виявляє асиметрію кровотоку, величину кровонаповнення, зміни судинного тонусу та еластичності судинної стінки.
3. Електроенцефалографія - виявляє дифузні і локальні зміни біопотенціалів мозку.
4. ЕКГ - визначають стан коронарних судин, порушення ритму серцевої діяльності тощо.
5. Рентгенографія шийного відділу хребта - виявляє симптоми остеохондрозу і аномалії розвитку хребта.
6. Детальне отоневрологічне обстеження - для виключення ураження лабіринту при вираженому вестибулярному синдромі.
7. Офтальмологічне обстеження - виявляє склеротичні чи інші (наприклад, гіпертонічні) зміни на очному дні.
8. Аналаз крові - включає дослідження реологічних властивостей крові, гемокоагуляції і виявляє підвищенняагрегації форменних елементів крові, в'язкості крові, гематокриту.
9. Біохімічне дослідження крові - виявляє протеїнемію, високий рівень холестерину, бета- та пребеталіпопротеїдів.
10. Церебральну ангіографію проводять у хворих зі схильністю до минущих порушень мозкового кровообігу в разі підозри на оклюзуючий процес (звуження, тромбоз), патологічну звивистість, аномалії розвитку екстракраніального відділу магістральних судин голови і дуги аорти, а також при аневризмах, ангіомах тощо.
ДИФЕРЕНЦІЙНА ДІАГНОСТИКА. МПМК диференціюють з наступними пароксизмальними станами:
1. Мігренозний криз,
2. Вестибулярний криз, як прояв хвороби Меньєра,
3. Вестибулярний криз при вегето-судинній дистонії,
4. Синкопальний стан,
5. Епілептичний напад,
6. Гіпертензивний криз (при пухлині ЗЧЯ, церебральному арахноїдиті, тощо).
ЛІКУВАННЯ. Госпіталізації підлягають хворі з:
а) важким церебрально-судинним кризом, який загрожує перейти в інсульт,
б) повторним кризом з вираженою вогнищевою симптоматикою,
в) важким гіпертонічним кризом при високих показниках артеріального тиску, що не піддаються зниженню,
г) коронарно-церебральним кризом з підозрою на інфаркт міокарда чи пролонгованим нападом стенокардії. Хворим із МПМК призначають ліжковий режим до закінчення гострого періоду і в наступні дні, залежно від загального стану і самопочуття хворого.
Основні принципи лікування МПМК такі:
1) нормалізація артеріального тиску;
2) своєчасне і адекватне відновлення мозкового і колатерального кровообігу;
3) покращення мікроциркуляції та реологічних властивостей крові, попередження агрегації форменних елементів крові,
4) зниження підвищеної згортальності крові;
5) зменшення проникності судинної стінки;
6) попередження набряку мозку і зниження внутрішньочерепної гіпертензії, поліпшення венозного відтоку крові;
7) поліпшення серцевої діяльності і нормалізація артеріального тиску;
8) покращення метаболізму нейронів;
9) усунення вегетативного синдрому.
Лікування гіпертонічних кризів:
1. При кризах любого типу застосовують:
універсальні гіпотензивні засоби:
клофелін 1 мл 0,01 % розчину внутрішньовенно на 20 мл ізотонічного розчину натрію хлориду;
дибазол 1% 2-4 мл внутрішньом'язово чи внутрішньовенно;
спазмолітики:
папаверину гідрохлорид 2% 2 мл внутрішньом'язово,
но-шпа 2% 2 мл внутрішньом'язово,
галідор 25% 2 мл внутрішньом'язово,
еуфілін 2,4% 10 мл внутрішньовенно на 20 мл фізрозчину.
кардіоселективні бетаадреноблокатори:
атенолол, атеносан по 25 мг-50 мг на добу,
ніфедипін 10-20 мг,
корінфар, кордипін по 10-20 мг під язик;
пролонговані:
корінфар ретард 10-20 мг двічі на добу,
адалат 20 мг 1-2 рази на добу,
норваск 5-10 мг на добу.
інгібітори АПФ:
капотен 25-50 мг,
ренітек, енап, еналапріл 5-10 мг.
2. При гіпертонічному гіперкінетичному кризі на догоспітальному етапі використовують пероральні гіпотензивні засоби у комбінації з діуретиками. Широко застосовують:
антагоністи кальцію - ніфедипін, адалат, кордарон, кордипін по 10-20 мг під язик, при цьому таблетку слід розжовувати. Уже через 10-20 хв атреріальний тиск знижується і досягає максимального зниження на 30-60 хв. При необхідності дозу можна повторити.
інгібітори АПФ - каптоприл (капотен) по 25-50 мг, його гіпотензивна дія проявляється через 15-30 хв,
клофелін 0,075-0,15 мг понижує артеріальний тиск через 30-60 хв, прийом препарату слід повторювати погодинно до сумарної дози 0,6 мг,
лабеталол по 200-400 мг викликає більш повільний гіпотензивний ефект,
При прийомі вищезгаданих ліків зниження артеріального тиску може призвести до артеріальної гіпотонії.
Невідкладну допомогу при неускладнених гіпертонічних кризах починають із введення:
дибазолу 1% розчин 2-4 мл та 2 мл 1% розчину лазиксу внутрішньовенно, з повторним введенням через 2-3 години;
клофеліну 1 мл 0,01% у 20 мл ізотонічного розчину натрію хлориду при внутрішньовенному (повільному) введенні можна досягти помірного зниження артеріального тиску. Однак препарат може викликати початкову пресорну реакцію;
рауседилу 1 мл 0,1% розчину (не володіє пресорною дією).
У разі, коли криз супроводжується тахікардією або різким порушенням ритму серцевої діяльності, слід використовувати
а) бетаадреноблокатори:
анаприлін 0,1% розчин 5 мл внутрішньовенно, потім у таблетках по 40 мг на добу, обзидан,
пропранолол 0,01% розчин 5 мл,
піндолол 5 мл 0,02% розчину в вену в 20 мл 5% розчину глюкози.
Протипокази: брадикардія, порушення атріовентрикулярної провідності,
б) антагоністи кальцію:
верапаміл 2 мл 0,25% розчину в 10 мл ізотонічного розчину натрію хлориду внутрішньовенно.
У випадках психомоторного збудженння призначають:
сибазон 2 мл 0,5% розчину внутрішньом'язово,
дроперидол 1 мл 0,25% розчину внутрішньом'язово,
піпольфен 1-2 мл 2,5% розчину внутрішньом'язово.
3. При гіпокінетичному гіпертонічному кризі застосовують
а) периферичні вазодилятатори:
натрію нітропрусид 0,05 г у 1000 мл 5% глюкози призначають внутрішньовенно крапельно зі швидкістю введення 0,25-10 мкг/кг/хв під ретельним контролем артеріального тиску (максимальний артеріальний тиск не повинен знижуватись менше 110 мм рт. ст.); інфузію препарату припиняють, якщо при швидкості введення 8 мкг/кг/хв гіпотензивний ефект не настає протягом 10 хв. Препарат протипоказаний, як і інші периферичні вазодилятатори, у випадках утруднення відтоку крові із вен мозку;
апресин 1 мл 2% розчину у 20 мл ізотонічного розчину хлориду натрію внутрішньовенно повільно,
діазоксид 20 мл 1,5% розчину внутрішньовенно протягом 10-30 с.
Апресин і діазоксид при супровідній патології ІХС, а також через зростання серцевого викиду після їх введення, необхідно поєднувати з b-адреноблокаторами.
б) антагоністи кальцію:
ніфедипін по 10-20 мг (1-2 драже) сублінгвально,
верапаміл 0,25% розчин 2 мл у 10 мл ізотонічного розчину натрію хлориду внутрішньовенно повільно.
4. При еукінетичному кризі застосовують клофелін, спазмолітики, антагоністи кальцію.
5. При усіх гіпертонічних кризах за гіпо- й еукінетичними типами центральної гемодинаміки у хворих з бурхливою психоемоційною й вегетативною реакцією показані внутрішньовенні крапельні інфузії:
аміназину по 1-2 мл 2,5% розчину в 100-200 мл ізотонічного розчину натрію хлориду внутрішньовенно крапельно із швидкістю 15-30 крапель за 1 хв; при недостатній ефективності повторюють інфузії аміназину (0,5-1 мл) внутрішньом’язово
сибазону 2 мл 0,5% розчину внутрішньом'язово,
піпольфену 2 мл 2,5% розчину внутрішньом'язово.
6. Гіпертонічний криз із симпатоадреналовою симптоматикою можна успішно лікувати
піроксаном по 2-3 мл 1% розчину внутрішньом’язово,
фентоламіном по 1 мл 0,5% розчину внутрішньовенно
тропафеном по 1 мл 1% розчину внутрішньом’язово або внутрішньовенно.
7. При гіпертонічних кризах з дуже високим артеріальним тиском (незалежно від типу гемодинаміки), які резистентні до вищезгаданих гіпотензивних засобів, а також в умовах загрози розвитку лівошлуночкової недостатності та набряку легень застосовують гангліоблокатори:
бензогексоній 0,5-1 мл 2,5% розчину внутрішньом'язово або підшкірно,
пентамін 1 мл 5% розчину внутрішньовенно крапельно на 200 мл 5% розчину глюкози.
Ці препарати вводять крапельно у вену, протягом 1-2 годин, понижуючи артеріальний тиск не більше ніж на 30%.
8. Для зниження внутрішньочерепного тиску та боротьби з набряком мозку хворим із гіпертонічним кризом вводять:
еуфілін або синтофілін 10 мл 2,4% розчину з лазиксом 2-4 мл 1% розчину в 10 мл ізотонічного розчину натрію хлориду.
9. Для підвищення стійкості мозку до набряку й гіпоксії використовують оксибутират натрію (20% розчин 10 мл внутрішньовенно в 10 мл 0,5% розчину глюкози).
10. Для профілактики гіпертонічних кризів використовують:
комбінацію антиадренергічних засобів, вазодилятаторів і діуретиків (адельфан, кристепін, трирезид К, тразитензин та ін.) в ефективних дозах (1-4 таблетки на добу),
антагоністи кальцію,
інгібітори ангіотензин-конвертуючого ферменту (капотен, еналаприл, раміприл та ін.),
бета-адреноблокатори.
ФАРМАКОТЕРАПІЯ ТРАНЗИТОРНИХ ІШЕМІЧНИХ АТАК.
1. Нормалізація артеріального тиску.
А) При серцевій недостатності й зниженні систолічного артеріального тиску нижче 120 мм рт. ст. призначають кардіотонічні засоби:
корглікон 1 мл 0, 06% розчину або
строфантин К 0,25 -1 мл 0,5% розчину внутрішньовенно в ізотонічному розчині хлориду натрію,
кордіамін 1 мл підшкірно або внутрішньом’язово,
сульфокамфокаїн 2 мл розчину внутрішньом’язово.
Б) Якщо артеріальний тиск значно знижений, призначають
кофеїн 1 мл 10% розчину підшкірно або внутрішньом’язово.
В) При колапсі вводять:
строфантин К 1 мл 0, 05% розчину
мезатон 1 мл 1% розчину та
преднізолон 60-120 мг в 200 мл ізотонічного розчину натрію хлориду чи 5% розчину глюкози внутрішньовенно.
Г) При тяжкій серцевій недостатності призначають
норадреналіну гідротартрат 2-4 мл 0,1% розчину внутрішньовенно крапельно в 1000 мл 5% розчину глюкози або
дофаміну 200 мг в 400 мл 5% розчину глюкози або 0,9% розчину натрію хлориду внутрішньовенно.
Д) Для посилення дії серцевих глікозидів їх рекомендується поєднувати з анаболічними стероїдами:
ретаболілом 50 мг внутрішньом’язово 1 раз у 5 днів 5 разів,
панангіном 1 драже тричі на добу
вітамінами групи В.
Е) При помірному підвищенні артеріального тиску (систолічний не більше 180 мм рт.ст.) призначають:
дибазол 2-4 мл 1% розчину внутрішньом'язово,
папаверину гідрохлорид 1-2 мл 2% розчину внутрішньом'язово,
но-шпу 2-4 мл 2% розчину внутрішньом'язово.
2) Для покращення мозкового кровообігу призначають вазоактивні препарати:
еуфілін 10 мл 2,4% розчину в 10 мл ізотонічного розчину натрію хлориду,
кавінтон 10-20 мг внутрішньовенно крапельно в 200 мл 0,9% розчину натрію хлориду,
інстенон 2 мл внутрішньовенно крапельно в 200 мл 5% розчину глюкози або струйно в 20 мл 40% розчину глюкози,
цинаризин дозою 0,025 г тричі на день
німотоп по 60 мг 4 рази на добу.
3) Для покращення мікроциркуляції і реологічних властивостей крові призначають:
пентоксифілін 5-10 мл внутрішньовенно крапельно в 250-500 мл ізотонічного розчину натрію хлориду,
реополіглюкін або реоглюман внутрішньовенно крапельно протягом 30-60 хв.
ксантинолу нікотинат 2 мл 15% розчину внутрішньом’язово або внутрішньовенно в 200 мл ізотонічного розчину натрію хлориду,
серміон 4-8 мг в 100-200 мл ізотонічного розчину натрію хлориду внутрішньовенно при супровідній артеріальній гіпертензії.
4. При тенденції до гіперкоагуляції або коли ТІА протікає з вираженою вогнищевою симптоматикою з метою попередження інсульту превентивно призначають
а) антикоагулянти прямої дії
гепарин по 5-10 тис. ОД підшкірно 2-4 рази на добу (продовжуючи час згортання у два рази) протягом 3-7 днів,
б) непрямої дії (знижуючи протромбіловий індекс до 50-40% в стаціонарі та до 55-60% в амбулаторних умовах, не допускаючи гематурії):
пелентан 0,1-0,3 г,
фенілін 0,015-0,03г,
синкумар 0,004г,
омефін 0,05г,
фепромарон 0,005г
двічі-тричі на добу протягом 2-3 тижнів з поступовим зниженням дози
в) антиагреганти:
ацетилсаліцилова кислота дозою 1 мг/кг ваги тіла 1 раз на добу,
трентал 5 мл 2% розчину внутрішньовенно крапельно або в таблетках по 0,2 (протипоказаний при інфаркті міокарда, не слід поєднувати з гепарином, не давати натще)
агапурин по 1 таблетці тричі на добу,
ксантинолу нікотинат 1-2 мл 15% розчину внутрішньом'язово
курантил по 0,025 г 2-3 рази на добу (протипоказаний при низькому артеріальному тиску, коронарній недостатності),
солкосерил 10-20 мл внутрішньовенно крапельно 5-7 днів,
тиклід (тиклопідин) по 0,25 г двічі на добу до 2-3 місяців,
плавікс (клопідогрель) 75 мг на добу,
пармідин 0,5 г тричі на добу,
танакан по 40 мг тричі на добу.
5. Для боротьби з набряком мозку застосовують:
гліцерин дозою 0,5-1,5 г/кг на добу всередину або внутрішньовенно крапельно дозою 50 мл 10% розчину в 200 мл ізотонічного розчину натрію хлориду,
ізосорбіт 1-2 г/кг крапельно у вигляді 50% розчину,
манітол 150-200 мл 10-20% розчину внутрішньовенно крапельно,
фуросемід 0,04-0,08 г вранці,
дихлотіазид 0,025-0,1 г вранці,
етакринову кислоту 0,05 г вранці,
лазикс 2 мл 1% розчину внутрішньом’язово або внутрішньовенно в 40 мл ізотонічного розчину натрію хлориду або з 10 мл 2,4% розчину еуфіліну,
тріампур 1-2 таблетки вранці,
дексон 4-8 мг внутрішньом’язово або внутрішньовенно,
альбумін людської сироватки дозою 50-100 мл 5% розчину внутрішньовенно крапельно,
антигістамінні засоби (супрастин, димедрол дозою 2 мл 1% розчину внутрішньом’язово).
6. Для покращання нейронального метаболізму призначають ноотропи:
ноотропіл 5-10 мл 20% розчину внутрішньовенно повільно або по 1 капсулі тричі на добу,
енцефабол (піридитол) по 1 драже тричі на добу,
інстенон 2 мл внутрішньовенно крапельно або внутрішньом'язово,
солкосерил 10-20 мл внутрішньовенно крапельно,
актовегін 2 мл внутрішньом'язово або 5-10 мл внутрішньовенно крапельно (протипоказаний при серцево-судинній недостатності, олігоурії, набряку легень),
церебролізин 1-5 мл 15% розчину внутрішньом'язово,
вітаміни групи В внутрішньом'язово,
АТФ 1мл внутрішньом'язово,
кокарбоксилаза 50-100 мг внутрішньом'язово.
7. Показана антиоксидантна терапія:
токоферола ацетат 1 мл внутрішньом'язово,
тіатріазолін 1 мл внутрішньом'язово,
емоксипін 3 мл внутрішньом'язово.
8. Симптоматична терапія:
а) при запамороченні - белоїд (беласпон, белатамінал) по 1 драже тричі на добу,
б) при блюванні та гикавці - аміназин (1 мл 2,5% розчину внутрішньом’язово), валідол (1 таблетка під язик), галоперидол (1,5-2 мг) через рот, або дроперидол (1-2 мл 0,25% розчину) внутрішньом’язово або 1 мл в 20 мл 40% розчину глюкози внутрішньовенно, сибазон (2-4 мл 0,5% розчину у вену), тіетилперазин (1 драже 2-3 рази на добу або 1-2 мл внутрішньом’язово), церукал (0,01 перорально або 2 мл внутрішньом’язово 0,5% розчину),
в) при інтенсивних цефалгіях - баралгін (спазган) по 5 мл внутрішньом’язово, внутрішньовенно, аналгін, седалгін, пенталгін, гірчичники на комірцеву зону,
г) для зменшення проникності судин - рутин (0,02 г), аскорбінову кислоту (0,25 г), аскорутин (1 таблетка), дицинон (0,25 г), кальцію глюконат (0,5 г), вікасол (0,015 г) тричі на добу всередину.
д) для усунення вегетативних розладів, ангіодистонічних порушень - седативні засоби та транквілізатори: бром з валеріаною, корвалол, інстенон перорально, димедрол, піпольфен, белоїд, белатамінал, валокордин, анаприлін, піроксан.
9. Хірургічне лікування призначають при повторних ТІА, зумовлених патологією магістральних судин голови в екстракраніальному відділі. Перед операцією проводять ультразвукову доплерографію екстра- та інтракраніальних судин голови, при необхідності - церебральну ангіографію. Покази до хірургічного лікування:
1) гемодинамічно значущий стеноз внутрішньої сонної артерії з повторними ТІА або з незначною залишковою органічною неврологічною симптоматикою;
2) патологічна звивистість внутрішньої сонної артерії;
3) гостре закупорення сонної артерії на шиї з вираженою вогнищевою симптоматикою без втрати свідомості в перші 6-12 годин;
4) атеросклеротичний стеноз, закупорення хребетних артерій на місці їх відходження або стискання хребетної артерії остеофітами;
5) закупорення підключичної артерії у проксимальному відділі.
ПРОФІЛАКТИКА МПМК включає своєчасну діагностику та лікування основного захворювання (атеросклерозу, гіпертонічної хвороби, серцевої патології, цукрового діабету, васкулітів) на тлі якого виникають МПМК, корекцію факторів ризику, які спричинюють прогресування судинної патології мозку (зловживання алкоголем, куріння, і особливо - поєднаня цих факторів, надлишкова вага тіла).
Важливу роль у профілактиці МПМК відіграють наступні фактори:
1. правильна організація режиму праці й відпочинку,
2. додержання режиму харчування. Дієту слід збагачувати вітамінами, калієм, магнієм, йодом. Кількість кухонної солі обмежують до 4-6 г на добу. Слід обмежити продукти, які збуджують центральну нервову систему: міцний чай, каву, какао, алкоголь, а також гострі закуски, приправи, копчені продукти;
3. вирішення соціальних проблем.
ПРАЦЕЗДАТНІСТЬ. При минущих порушеннях мозкового кровообігу хворі повинні бути визнані тимчасово непрацездатними. Питання про працездатність в майбутньому залежить від характеру перебігу основного судинного захворювання, ефективності лікування, особливостей умов праці. При частих повторних МПМК необхідно працевлаштувати хворого для виключення нервово-психічного та фізичного навантаження чи направити хворого на МСЕК для встановлення групи інвалідності.
ГОСТРА ГІПЕРТОНІЧНА ЕНЦЕФАЛОПАТІЯ
Гостра гіпертонічна енцефалопатія виникає здебільшого на тлі злоякісної артеріальної гіпертонії, ниркової гіпертонії, еклампсії, при підйомах систолічного артеріального тиску вище 200-270 мм рт. ст. і діастолічного - вище 120 мм рт. ст.
ПАТОГЕНЕЗ. Розвиток гострої гіпертонічної енцефалопатії пов’язують з інфільтраційним набряком і набуханням мозку у відповідь на збільшення мозкового кровообігу при високому артеріальному тиску із інтравазальними геморагіями і плазморагіями, які розвиваються у м’якій мозковій оболонці півкуль великого мозку і мозковому стовбурі (Ганнушкіна І. В., Лебедєва Н.В., 1987). Окрім того, набряк мозку призводить до зниження мозкового кровообігу з виникнення вогнищ розм’якшення паренхіми мозку і геморагій.
КЛІНІКА. Відмінною особливістю клініки гострої гіпертонічної енцефалопатії є швидкий розвиток, тривалий перебіг (більше доби), важкість стану хворого та резистентність до гіпотензивної терапії. Клінічна картина характеризується появою загальномозкових та вогнищевих симптомів, із значною перевагою перших.
1. Із загальномозкових проявів спостерігається наступна неврологічна симптоматика:
дифузний головний біль, тупого, розпираючого характеру, рідше він локалізується в потиличній ділянці. Нерідко біль іррадіює в очні яблука;
нудота, блювання;
відчуття шуму в голові та вухах;
запаморочення, переважно несистемного характеру;
розлади зору у вигляді яскравих плям, зірочок, спіралей, короткочасних випадінь поля зору або різким зниженням зору аж до сліпоти;
вегетативно-судинні розлади: гіперемія або блідість обличчя, біль у ділянці серця, серцебиття або брадикардія, сухість у роті, гіпергідроз;
розлади емоційно-психічної сфери: подразливість, занепокоєння.
У важких випадках спостерігають:
- порушення свідомості,
- оглушення,
- сонливість,
- психомоторне збудження,
- дезорієнтацію у просторі та часі,
- епілептичні напади,
- кома.
Можлива поява менінгеальних симптомів: ригідність потиличних м’язів, симптоми Керніга, Брудзинського. На очному дні виявляють застійні диски зорових нервів, стази, дрібні крововиливи, розширення вен, інколи - явища альбумінуричного ретиніту.
2. Із вогнищевих симптомів нерідко спостерігається:
затерпання кінцівок,
зниження больової чутливості в ділянці обличчя, язика;
анізорефлексія сухожилкових та периостальних рефлеків;
порушення чутливості за гемітипом,
координаційні розлади;
чіткі субкортикальні рефлекси: Марінеску-Радовічі, губний рефлекс Бехтерева.
Діагностика. Поперековий прокол виявляє значне підвищення внутрішньочерепного тиску - до 500-600 мм вод. ст. Кількість білка та клітинний склад ліквору не змінюються, однак інколи з’являється білково-клітинна дисоціація. На комп’ютерній томограмі спостерігають ознаки набряку тканини головного мозку. Характерні зміни біохімічних показників крові: гіперглікемія, гіперхолестеринемія, підвищення вмісту гістаміну, а також лейкоцитів.
Гостра гіпертонічна енцефалопатія частково або повністю регресує на фоні лікування протягом декількох діб, але інколи може закінчуватися летально.
ЛІКУВАННЯ. 1. Нормалізація артеріального тиску. При гострій гіпертонічній енцефалопатії не слід швидко і значно знижувати артеріальний тиск. Доцільно підтримувати його на рівні близько 150/100 мм рт. ст. Найкращими гіпотензивними препаратами для цього вважаються:
нітропрусид натрію внутрішньовенно під постійним контролем артеріального тиску зі швидкістю 8 мкг/кг за хвилину,
гангліоблокатори: пентамін 0,5-1 мл 5% розчину внутрішньом’язево або внутрішньовенно струйно,
арфонад 5 мл 0,5-1% розчину в 100 мл ізотонічного розчину натрію хлориду,
бензогексоній 1-2 мг 2,5% розчину внутрішньовенно.
2. Для боротьби з набряком мозку та зниження внутрішньочерепного тиску вводять
еуфілін 10 мл 2,4% розчину з лазиксом 2-4 мл 1% розчину в 10 мл ізотонічного розчину натрію хлориду внутрішньовенно,
альбумін людської сироватки 50-100 мл 5% розчину внутрішньовенно крапельно,
антигістамінні засоби: супрастин 2 мл 1% розчину
або димедрол 2 мл 1% розчину в 100 мл ізотонічного розчину натрію хлориду внутрішньовенно крапельно.
сульфат магнію 10-20 мл 25% розчину внутрішньом’язово.
3. Для зняття психомоторного збудження, епілептичних нападів:
дроперидол 1-2 мл 2,5% розчину в 20 мл ізотонічного розчину натрію хлориду внутрішньовенно струйно,
сибазон 2-4 мл 0,5% розчину внутрішньом’язово.
4. Симптоматична терапія:
при цефалгічному синдромі - аналгін, спазгам, седалгін, трамал, трамадол, піроксикам.
при блюванні та гикавці - церукал, галоперидол, аміназин, валідол;
Після нормалізації артеріального тиску переходять на звичні пероральні гіпотензивні препарати. Застосування спазмолітиків (папаверин, но-шпа) при гострій гіпертонічній енцефалопатії протипоказане.
Минущі порушення мозкового кровообігу (МПМК) - це гостро виникаючі на тлі основного захворювання дисциркуляційні явища у головному мозку, що супроводжуються тимчасовими загальномозковими та вогнищевими симптомами із зворотнім їх розвитком протягом 24 годин. Це одна із найбільш частих клінічних форм гострого порушення мозкового кровообігу. Такі хворі у неврологічних стаціонарах складають близько 20% від усіх пацієнтів із судинними захворюваннями головного мозку.
До минущих порушень мозкового кровообігу відносять транзиторні ішемічні атаки (ТІА)(приблизно 1/3 усіх випадків МПМК) і гіпертонічні кризи (2/3 усіх МПМК), незалежно від того, проявляються вони загальномозковими чи вогнищевими симптомами.
Гіпертонічні кризи (ГК) найчастіше виникають при гіпертонічній хворобі, нирковій та наднирковій гіпертонії, ТІА - при атеросклерозі, стенозуючих ураженнях магістральних артерій голови, захворюваннях серця (вади серця, пролапс мітрального клапана, інфаркт міокарда); значно рідше вони зустрічаються при васкулітах різної етіології (інфекційно-алергічних, сифілітичних), при системних васкулітах (вузликовий периартеріїт) тощо. Значно меншу роль у їхньому розвитку відіграють цукровий діабет, здавлювання остеофітами хребетних артерій.
ТРАНЗИТОРНІ ІШЕМІЧНІ АТАКИ
ПАТОГЕНЕЗ. Основними патогенетичними чинниками ТІА є:
тромбемболічні та
гемодинамічні, які тісно пов'язані між собою.
1. Найбільш частими чинниками ТІА вважають тромбемболічні, тобто мікроемболію мозкових судин. Розрізняють артеріогенні та кардіогенні мікроемболи.
а) Артеріогенні мікроемболи являють собою дрібні частинки, що відірвалися від пристінкових тромбів при розпаді атеросклеротичних бляшок. Важливу роль у розвитку ТІА відіграють артеріоартеріальні емболії, які є конгломератами еритроцитів, тромбоцитів, що утворюються у зміненій ділянці стінки великих судин і з током крові через магістральні артерії голови потрапляють у дистальні судини невеликого калібру, кінцеві гілки артеріальної системи, частіше кіркові гілки мозкових артерій, викликаючи їх тимчасову оклюзію. Подразнюючи ендотелій, вони спричиняють спазм судин і підвищують проникність їх стінок із наступним розвитком периваскулярного набряку мозкової тканини, що супроводжується виникненням вогнищевих симптомів. Утворенню цих тромбів сприяють зміни:
- фізико-хімічних властивостей крові
а) підвищення в'язкості, агрегації та адгезії тромбоцитів і еритроцитів,
б) зниження їх здатності до деформації,
- біохімічних властивостей крові
а) гіперліпідемія,
б) гіперглікемія,
в) діабетичний кетоз.
Тромбоцитарні емболи крихкі, легко піддаються лізису, що і зумовлює зворотній розвиток неврологічного дефіциту.
б) Кардіогенні мікроемболи спричинюють ТІА у хворих з:
- миготливою аритмією,
- вадами серця,
- інфарктом міокарду,
- у хворих на ревматичний ендокардит з пролапсом мітрального клапану.
2. ТІА також зумовлюють мікротромбози при захворюваннях крові:
- поліцитемія,
- мікроглобулінемія,
- тромбоцитози.
3. Одним з механізмів ТІА може бути атеросклеротичний стеноз мозкових чи магістральних судин голови, особливо у поєднанні з:
- падінням артеріального тиску,
- порушенням серцевого ритму,
- інфарктом міокарду,
- кровотечею.
Сам стеноз може бути не лише причиною МПМК, але й джерелом "вторинних" емболій.
4. ТІА можуть бути викликані тромбозом або облітерацією магістральної артерії на шиї, коли добре розвинута сітка колатерального кровообігу і артеріальне коло великого мозку сприяють відновленню кровотоку дистальніше місця оклюзії та попередженню стійкої ішемії мозкової речовини.
5. Нерідко ТІА виникають за механізмом “обкрадання”. Наприклад, при оклюзії підключичної артерії кровопостачання руки здійснюється через вертебро-базилярний басейн головного мозку шляхом ретроградного перетоку в ущерб кровопостачанню головного мозку. При цьому, клінічно звучить симптоматика басейну інтактної судини.
6. Важливу роль у патогенезі ТІА відіграють уроджені стенози, патологічна звивистість та гіпоплазії чи інші аномалії розвитку магістральних артерій голови.
7. Здебільшого, причиною ТІА у вертебро-базилярному басейні буває стиснення хребетної артерії остеофітами при шийному остеохондрозі.
8. Певну роль у виникненні ТІА відіграє механізм судинної мозкової недостатності, коли виникає невідповідність між потребою мозку та повноцінним забезпеченням тканини кров'ю (наприклад, при серцевій слабкості, різкому зниженні, артеріального тиску, внутрішній кровотечі тощо)
9. Не менш важливе значення в патогенезі ТІА мають кисневе голодування, порушення церебрального метаболізму.
КЛІНІКА. ТІА (або транзиторні ішемії) розвиваються у більшості випадків гостро, раптово і значно рідше - поступово з повільним розвитком симптомів. Як правило, маніфестують вогнищевою неврологічною симптоматикою, яка значно переважвє над загальномозковими проявами. Іншими словами, ТІА є регіональними МПМК. Клінічні прояви їх різноманітні і залежать від локалізації і тривалості дисциркуляційних розладів.
Розрізняють дві групи симптомів при ТІА:
а) вогнищеві
б) загальномозкові.
Загальномозкові симптоми, якщо вони є, проявляються:
- головним болем,
- запамороченням несистемного чи системного характеру,
- нудотою, блюванням,
- відчуттям вираженої загальної слабкості,
- пеленою перед очима,
- короткочасною втратою свідомості.
Вогнищеві, або регіональні, залежать від судинного басейну, в якому виникає дисциркуляція.
ТІА в каротидному басейні (зустрічається у 30 % усіх випадків ТІА) клінічно проявляються симптомами дисфункції коркових відділів мозку. Каротидний - це басейн внутрішніх сонних артерій, від яких відходять: очна артерія, передня та середня мозкові артерії. Зона кровопостачання - передній відділ лобної частки, внутрішня поверхня півкулі до тім'яно-потиличної борозни, на конвекситальній поверхні мозку кора лобної, тім'яної та скроневої часток, підкоркові ядра, внутрішня капсула. При дисциркуляції в системі внутрішньої сонної артерії найбільш частими бувають наступні вогнищеві симптоми:
1. суб'ктивні (відчуття затерпання. оніміння, поколювання на обличчі або в руці чи нозі) та об'єктивні чутливі розлади (гіпестезія поверхневої чутливості в ділянці обличчя, руки чи ноги, іноді зниження глибокої чутливості в пальцях кисті чи ступні)
2. рухові порушення такі, як центральний парез руки чи ноги, окремих пальців на кисті чи ступні, з підвищенням сухожилкових рефлексів, зниженням шкірних, патологічними знаками Бабінськогоо, Россолімо, тощо. Геміпарез чи геміплегія виникають лише у вкрай важких випадках.
3. При ураженні лівої півкулі мозку виникають розлади мови - минуща афазія або коркова дизартрія, які поєднуються із чутливими та руховими розладами у правих кінцівках.
4. При ТІА, зумовлених закупоренням або стенозом внутрішньої сонної артерії на шиї, розвивається минущий перехресний оптико-пірамідний синдром Ласко-Радовича: зниження зору або сліпота на стороні ураження та слабкість кінцівок на протилежному боці. Іноді зниження зору на одне око поєднується лише з гіперрефлексією контрлатеральних кінцівок.
5. При наявності патології магістральних судин голови ТІА можуть маніфестувати фокальними джексонівськими руховими та чутливими нападами.
ТІА у системі вертебро-базилярного басейну складають майже 70 % усіх випадків ТІА. Так, як вертебро-базилярний басейн забезпечує кровопостачання стовбуга головного мозку, мозочка, кори потиличної частки, медіобазальні структури скроневих часток мозку, то клінічно спостерігається відповідна симптоматика:
1. вестибулярний синдром - проявляється:
- системним запамороченням,
- шумом у голові та вухах,
- головним болем у потиличній ділянці,
- "пеленою" перед очима,
- нудотою,
- блюванням,
- ністагмом,
- розладами рівноваги;
2. мозочково-стовбуровий синдром - проявляється порушенням координації і синергії рухів та рівноваги (а саме статики);
3. синдром окорухових розладів - парез погляду, розлади конвергенції, диплопія, косоокість;
4. бульбарний синдром - порушення ковтання, голосу та вимови;
5. альтернуючі синдроми зустрічаються відносно рідко;
6. зорові розлади у вигляді:
- фотопсій,
- геміанопсій,
- метаморфопсій,
- невиразності,
- дефектів поля зору,
- появи оптичних феноменів (кольорів, фігур).
7. атонічно-адинамічний синдром - виникає при раптовій ішемії ретикулярної формації та нижніх олив у ділянці довгастого мозку і проявляється нападами раптового зниження м'язового тонусу, що призводить до падіння хворого без втрати свідомості. Ці напади найчастіше виникають при патології шийного відділу хребта у момент різкого повороту або закидання голови назад. Нерідко виникає синдром Унтерхарншайдта, коли втрата м'язового тонусу поєднується із втратою свідомості на короткий час (синдром Сикстинської капели - виникає у туристів похилого віку під час огляду фресок Мікельанжело на куполі Сикстинської капели у Римі. Внаслідок різкого перерозгинання шиї змінюється кровоток у хребетних артеріях).
8. корсаківський синдром - виникає при ішемії медіобазальних структур скроневої ділянки мозку і проявляється атаками тимчасових розладів пам'яті на біжучі події з конфабуляторним компонентом та дезорієнтацією.
9. пароксизмальний гіперсомнічний і катаплексичний синдроми та вегетативно-судинні розлади виникають при ішемії гіпоталамічних структур.
10. синдром скроневої епілепсії.
11. ураження різних структур лімбічної системи проявляеться змінами з боку емоційно-вольової сфери:
- підвищена втомлюваність,
- зниження працездатності,
- подразливість,
- часто пригнічений настрій, апатія,
- інколи пароксизмальне підвищення артеріального тиску.
12. синдром підключичного обкрадання - виникає при стенозі підключичної артерії, внаслідок чого кровоток в хребетній артерії стає ретроградним, забезпечуючи кровопостачанняруки ("рука-провокатор"). При цьому синдром клінічно проявляється ішемією стовбура: втрата свідомості та інші симптоми вертебро-базилярної недостатності.
Нерідко зустрічаються одночасно атеросклеротичне ураження сонної і хребетної артерій, особливо у людей похилого віку. При множинному ураженні магістральних судин голови можуть виникати симптоми порушення кровообігу як у сонній, так і в хребетно-основній системі. Тому, крім каротидних та вертебро-базилярних ішемічних кризів виділяють поєднані минущі порушення мозкового кровообігу , такі як коронарно-церебральні, аорто-церебральні, гепато-церебральні, холецисто-церебральні та ін.
Необхідно зазначити, що ТІА мають тривалість від декількох хвилин до доби, проте найчастіше вони продовжуються 10-15 хвилин. Нерідко зустрічаються випадки, коли загальномозкова та вогнищева симптоматика зникає протягом декількох наступних днів. Для ТІА характерні рецидиви, коли протягом року атаки повторюються до 3-5 разів. Ще одна особливість, про яку слід згадати, це більша частота ТІА у вертебро-базилярному басейні і найбільша їх повторюваність при локалізації в хребетно-базилярному басейні на відміну від ТІА у каротидному басейні. Проте прогноз при ТІА в системі сонної артерії завжди серйозніший, оскільки протягом одного, рідше двох років після першої атаки розвивається інсульт. Несприятливим є прогноз минущого порушення мозкового кровообігу, якщо воно виникає на тлі кардіальної патології з порушенням ритму серцевої діяльності. Повторюваність ТІА декілька разів на добу свідчить про патологію магістральних артерій голови.
Діагноз ТІА потрібно диференціювати із синкопальними пароксизмами (зомління). Синкопальні пароксизми виникають, як правило, у хворих молодого віку з вегетативною дисфункцією, зі схильністю до ортостатичних реакцій. ТІА у вертебро-базилярній системі часто супроводжуються нападами системного запаморочення, яке потрібно відрізняти від ураження лабіринту, хвороби Меньєра. Встановленню діагнозу допомагають дані анамнезу та отоневрологічного обстеження. Виявлення додаткових неврологічних симптомів (зорові, слухові, мозочкові розлади, порушення чутливості) свідчить про судинний генез захворювання.
ГІПЕРТОНІЧНІ ЦЕРЕБРАЛЬНІ КРИЗИ
Гіпертонічні церебральні кризи складають13-15% від усіх гострих порушень мозкового кровообігу, а також 2/3 хворих МПМК.
ПАТОГЕНЕЗ. До недавнього часу більшість клініцистів дотримувались тієї точки зору, згідно якої у відповідь на раптове підвищення артеріального тиску при гіпертонічних кризах виникає спазм судин головного мозку, що призводить до дефіциту мозкового кровопостачання. Результати експериментальних досліджень останніх десятиліть довели, що вазоспазм у момент підвищення артеріального тиску є проявом реакції авторегуляції мозкового кровообігу. Вазоспазм захищає головний мозок від надлишкової перфузії. При швидкому і більш значному підвищенні артеріального тиску (більше 180-200 мм рт. ст.) авторегуляційні механізми не компенсують зростання перфузійного тиску, внаслідок чого виникає зрив реакції авторегуляції мозкового кровообігу і гіперемія головного мозку, створюються умови для набряку мозку, дефіциту мозкового кровообігу та розвитку ішемії тканин мозку. Таким чином, у патогенезі церебральних гіпертонічних кризів виняткове значення має єдиний чинник зриву авторегуляції мозкового кровообігу.
КЛІНІКА ГІПЕРТОНІЧНИХ КРИЗІВ. Як уже зазначалось, гіпертонічні кризи є проявом загострення гіпертонічної хвороби чи симптоматичної артеріальної гіпертензії, коли у момент різкого підвищення артеріального тиску розвивається гіперемія та набряк мозку, які супроводжуються появою загальномозкових і рідше вогнищевих симптомів, що зникають протягом доби. Гіпертонічний церебрально-судинний криз супроводжується, крім значного підйому артеріального тиску:
- головним болем,
- відчуттям важкості у голові,
- психомоторним збудженням,
- іноді потьмаренням свідомості,
- почервонінням обличчя,
- серцебиттям,
- затрудненням дихання,
- болем у ділянці серця,
- нудотою, блюванням,
- часом розвиваються епілептичні напади.
Спостерігаються також різко виражені дифузні вегетативні порушення:
- пітливість,
- відчуття похолодання кінцівок,
- зміна частоти дихання, пульсу,
- зміна кольору обличчя.
Виділяють три типи кризів у залежності від типу системної гемодинаміки:
1. гіперкінетичний тип - супроводжується збільшенням серцевого викиду зі зростанням серцевого індексу більше 4,5 л/хвґм2 при нормальному або дещо зниженому периферичному судинному опорі;
2. гіпокінетичний тип - супроводжується неадекватним зниженням серцевого викиду і зменшенням серцевого індексу до 2,8 л/хвґм2 при, відповідно, різкому зростанні загального периферичного опору;
3. еукінетичний тип - розвивається при нормальному серцевому викиді (серцевий індекс суттєво не змінюється) та помірно підвищеному загальному периферичному опорі.
Для адекватного лікування гіпертонічного кризу важливо виявити його основний механізм, а тому розпізнавання типу церебрально-судинного кризу є необхідним.
Клінічно гіпертонічний криз гіперкінетичного типу проявляється наступними ознаками:
1. характерним є швидкий розвиток кризу на фоні доброго самопочуття, без передвісників,
2. підвищується переважно систолічний тиск (більше 180-200 мм рт. ст.),
3. загальномозкові симптоми виражені різко: психомоторне збудження, різкий пульсуючий головний біль з нудотою та блюванням, мерехтіння мушок перед очима,
4. різко виражені вегетативні прояви: затруднене дихання, почервоніння чи блідість шкіри, поліурія, емоційна лабільність, жар та тремтіння у всьому тілі,
5. незначна тривалість кризу, до декількох годин,
6. розвивається не лише у хворих на гіпертонічну хворобу, але й при деяких формах симптоматичної артеріальної гіпертензії.
Особливості кризу гіпокінетичного типу:
1. поступовий розвиток на тлі тривалої гіпертензії, на пізніх стадіях гіпертонічної хвороби,
2. підвищується діастолічний тиск,
3. з'являються виражені зміни на ЕКГ: сповільнення внутрішлуночкової провідності, зниження сегменту ST,
4. при цій формі кризу існує велика небезпека розвитку ішемічного інсульту.
Клінічні особливості кризу еукінетичного типу:
1. швидкий розвиток,
2. підвищується і систолічний, і діастолічний тиск,
3. з'являються явища гострої недостатності лівого шлуночка, набряк легень.
Залежно від стану церебральної гемодинаміки, гіпертонічні кризи поділяють на:
1. гіперволемічний тип - пульсове кровонаповнення більше 0,12 Ома,
2. нормоволемічний тип - пульсове кровонаповнення коливається в межах 0,09-0,11 Ома,
3. гіповолемічний тип - пульсове кровонаповнення менше 0,08 Ома.
За тривалістю гіпертонічні кризи ділять на:
а) легкі - тривають до 1 години,
б) середньої важкості - тривають декілька годин,
в) важкі - тривають більше 5-6 годин, але не більше доби.
Критерії частоти:
а) при легких кризах: часті - більше 4 разів на місяць, середньої частоти - 3-4 рази на місяць, рідкі - 1-2 рази на місяць.
б) середньої важкості і важкі: часті - більше 5 разів на рік, середньої частоти - 3-5 разів на рік, рідкі - 1-2 рази на рік.
Вогнищевих симптомів ураження головного мозку при церебрально-судинних кризах здебільшого не буває, але можуть виявлятись ригідність потиличних м’язів, симптом Керніга, підвищення тиску спинномозкової рідини.
ДІАГНОСТИКА МПМК. При діагностуванні проминучих розладів мозкового кровообігу діагноз легкої транзиторної ішемічної атаки чи гіпертонічного кризу, коли симптоми порушення кровообігу тривають недовго, від декількох хвилин до години, не виникає затрудненнь. Проте, коли у хворого раптово з'являється загальномозкова та вогнищева симптоматика дизгемії і триває декілька годин, діагноз динамічного розладу мозкового кровообігу виставляється ретроспективно, уже після зникнення клінічних симптомів, так як у цьому випадку невідомо, чи не розвинеться інсульт. Оскільки транзиторна ішемічна атака чи гіпертонічний криз часто є першим проявом патології серцево-судинної системи, важливим є вияснення основного судинного захворювання, яке призвело до виникнення МПМК. З метою обстеження судинних хворих використовують наступні спеціальні методи обстеження:
1. Ультразвукова доплерографія - визначає наявність оклюзій чи стенозів у магістральних артеріях голови та шиї, у інтракраніальних судинах, а також стан колатерального кровотоку.
2. Реоенцефалографія з функціональними пробами виявляє асиметрію кровотоку, величину кровонаповнення, зміни судинного тонусу та еластичності судинної стінки.
3. Електроенцефалографія - виявляє дифузні і локальні зміни біопотенціалів мозку.
4. ЕКГ - визначають стан коронарних судин, порушення ритму серцевої діяльності тощо.
5. Рентгенографія шийного відділу хребта - виявляє симптоми остеохондрозу і аномалії розвитку хребта.
6. Детальне отоневрологічне обстеження - для виключення ураження лабіринту при вираженому вестибулярному синдромі.
7. Офтальмологічне обстеження - виявляє склеротичні чи інші (наприклад, гіпертонічні) зміни на очному дні.
8. Аналаз крові - включає дослідження реологічних властивостей крові, гемокоагуляції і виявляє підвищенняагрегації форменних елементів крові, в'язкості крові, гематокриту.
9. Біохімічне дослідження крові - виявляє протеїнемію, високий рівень холестерину, бета- та пребеталіпопротеїдів.
10. Церебральну ангіографію проводять у хворих зі схильністю до минущих порушень мозкового кровообігу в разі підозри на оклюзуючий процес (звуження, тромбоз), патологічну звивистість, аномалії розвитку екстракраніального відділу магістральних судин голови і дуги аорти, а також при аневризмах, ангіомах тощо.
ДИФЕРЕНЦІЙНА ДІАГНОСТИКА. МПМК диференціюють з наступними пароксизмальними станами:
1. Мігренозний криз,
2. Вестибулярний криз, як прояв хвороби Меньєра,
3. Вестибулярний криз при вегето-судинній дистонії,
4. Синкопальний стан,
5. Епілептичний напад,
6. Гіпертензивний криз (при пухлині ЗЧЯ, церебральному арахноїдиті, тощо).
ЛІКУВАННЯ. Госпіталізації підлягають хворі з:
а) важким церебрально-судинним кризом, який загрожує перейти в інсульт,
б) повторним кризом з вираженою вогнищевою симптоматикою,
в) важким гіпертонічним кризом при високих показниках артеріального тиску, що не піддаються зниженню,
г) коронарно-церебральним кризом з підозрою на інфаркт міокарда чи пролонгованим нападом стенокардії. Хворим із МПМК призначають ліжковий режим до закінчення гострого періоду і в наступні дні, залежно від загального стану і самопочуття хворого.
Основні принципи лікування МПМК такі:
1) нормалізація артеріального тиску;
2) своєчасне і адекватне відновлення мозкового і колатерального кровообігу;
3) покращення мікроциркуляції та реологічних властивостей крові, попередження агрегації форменних елементів крові,
4) зниження підвищеної згортальності крові;
5) зменшення проникності судинної стінки;
6) попередження набряку мозку і зниження внутрішньочерепної гіпертензії, поліпшення венозного відтоку крові;
7) поліпшення серцевої діяльності і нормалізація артеріального тиску;
8) покращення метаболізму нейронів;
9) усунення вегетативного синдрому.
Лікування гіпертонічних кризів:
1. При кризах любого типу застосовують:
універсальні гіпотензивні засоби:
клофелін 1 мл 0,01 % розчину внутрішньовенно на 20 мл ізотонічного розчину натрію хлориду;
дибазол 1% 2-4 мл внутрішньом'язово чи внутрішньовенно;
спазмолітики:
папаверину гідрохлорид 2% 2 мл внутрішньом'язово,
но-шпа 2% 2 мл внутрішньом'язово,
галідор 25% 2 мл внутрішньом'язово,
еуфілін 2,4% 10 мл внутрішньовенно на 20 мл фізрозчину.
кардіоселективні бетаадреноблокатори:
атенолол, атеносан по 25 мг-50 мг на добу,
ніфедипін 10-20 мг,
корінфар, кордипін по 10-20 мг під язик;
пролонговані:
корінфар ретард 10-20 мг двічі на добу,
адалат 20 мг 1-2 рази на добу,
норваск 5-10 мг на добу.
інгібітори АПФ:
капотен 25-50 мг,
ренітек, енап, еналапріл 5-10 мг.
2. При гіпертонічному гіперкінетичному кризі на догоспітальному етапі використовують пероральні гіпотензивні засоби у комбінації з діуретиками. Широко застосовують:
антагоністи кальцію - ніфедипін, адалат, кордарон, кордипін по 10-20 мг під язик, при цьому таблетку слід розжовувати. Уже через 10-20 хв атреріальний тиск знижується і досягає максимального зниження на 30-60 хв. При необхідності дозу можна повторити.
інгібітори АПФ - каптоприл (капотен) по 25-50 мг, його гіпотензивна дія проявляється через 15-30 хв,
клофелін 0,075-0,15 мг понижує артеріальний тиск через 30-60 хв, прийом препарату слід повторювати погодинно до сумарної дози 0,6 мг,
лабеталол по 200-400 мг викликає більш повільний гіпотензивний ефект,
При прийомі вищезгаданих ліків зниження артеріального тиску може призвести до артеріальної гіпотонії.
Невідкладну допомогу при неускладнених гіпертонічних кризах починають із введення:
дибазолу 1% розчин 2-4 мл та 2 мл 1% розчину лазиксу внутрішньовенно, з повторним введенням через 2-3 години;
клофеліну 1 мл 0,01% у 20 мл ізотонічного розчину натрію хлориду при внутрішньовенному (повільному) введенні можна досягти помірного зниження артеріального тиску. Однак препарат може викликати початкову пресорну реакцію;
рауседилу 1 мл 0,1% розчину (не володіє пресорною дією).
У разі, коли криз супроводжується тахікардією або різким порушенням ритму серцевої діяльності, слід використовувати
а) бетаадреноблокатори:
анаприлін 0,1% розчин 5 мл внутрішньовенно, потім у таблетках по 40 мг на добу, обзидан,
пропранолол 0,01% розчин 5 мл,
піндолол 5 мл 0,02% розчину в вену в 20 мл 5% розчину глюкози.
Протипокази: брадикардія, порушення атріовентрикулярної провідності,
б) антагоністи кальцію:
верапаміл 2 мл 0,25% розчину в 10 мл ізотонічного розчину натрію хлориду внутрішньовенно.
У випадках психомоторного збудженння призначають:
сибазон 2 мл 0,5% розчину внутрішньом'язово,
дроперидол 1 мл 0,25% розчину внутрішньом'язово,
піпольфен 1-2 мл 2,5% розчину внутрішньом'язово.
3. При гіпокінетичному гіпертонічному кризі застосовують
а) периферичні вазодилятатори:
натрію нітропрусид 0,05 г у 1000 мл 5% глюкози призначають внутрішньовенно крапельно зі швидкістю введення 0,25-10 мкг/кг/хв під ретельним контролем артеріального тиску (максимальний артеріальний тиск не повинен знижуватись менше 110 мм рт. ст.); інфузію препарату припиняють, якщо при швидкості введення 8 мкг/кг/хв гіпотензивний ефект не настає протягом 10 хв. Препарат протипоказаний, як і інші периферичні вазодилятатори, у випадках утруднення відтоку крові із вен мозку;
апресин 1 мл 2% розчину у 20 мл ізотонічного розчину хлориду натрію внутрішньовенно повільно,
діазоксид 20 мл 1,5% розчину внутрішньовенно протягом 10-30 с.
Апресин і діазоксид при супровідній патології ІХС, а також через зростання серцевого викиду після їх введення, необхідно поєднувати з b-адреноблокаторами.
б) антагоністи кальцію:
ніфедипін по 10-20 мг (1-2 драже) сублінгвально,
верапаміл 0,25% розчин 2 мл у 10 мл ізотонічного розчину натрію хлориду внутрішньовенно повільно.
4. При еукінетичному кризі застосовують клофелін, спазмолітики, антагоністи кальцію.
5. При усіх гіпертонічних кризах за гіпо- й еукінетичними типами центральної гемодинаміки у хворих з бурхливою психоемоційною й вегетативною реакцією показані внутрішньовенні крапельні інфузії:
аміназину по 1-2 мл 2,5% розчину в 100-200 мл ізотонічного розчину натрію хлориду внутрішньовенно крапельно із швидкістю 15-30 крапель за 1 хв; при недостатній ефективності повторюють інфузії аміназину (0,5-1 мл) внутрішньом’язово
сибазону 2 мл 0,5% розчину внутрішньом'язово,
піпольфену 2 мл 2,5% розчину внутрішньом'язово.
6. Гіпертонічний криз із симпатоадреналовою симптоматикою можна успішно лікувати
піроксаном по 2-3 мл 1% розчину внутрішньом’язово,
фентоламіном по 1 мл 0,5% розчину внутрішньовенно
тропафеном по 1 мл 1% розчину внутрішньом’язово або внутрішньовенно.
7. При гіпертонічних кризах з дуже високим артеріальним тиском (незалежно від типу гемодинаміки), які резистентні до вищезгаданих гіпотензивних засобів, а також в умовах загрози розвитку лівошлуночкової недостатності та набряку легень застосовують гангліоблокатори:
бензогексоній 0,5-1 мл 2,5% розчину внутрішньом'язово або підшкірно,
пентамін 1 мл 5% розчину внутрішньовенно крапельно на 200 мл 5% розчину глюкози.
Ці препарати вводять крапельно у вену, протягом 1-2 годин, понижуючи артеріальний тиск не більше ніж на 30%.
8. Для зниження внутрішньочерепного тиску та боротьби з набряком мозку хворим із гіпертонічним кризом вводять:
еуфілін або синтофілін 10 мл 2,4% розчину з лазиксом 2-4 мл 1% розчину в 10 мл ізотонічного розчину натрію хлориду.
9. Для підвищення стійкості мозку до набряку й гіпоксії використовують оксибутират натрію (20% розчин 10 мл внутрішньовенно в 10 мл 0,5% розчину глюкози).
10. Для профілактики гіпертонічних кризів використовують:
комбінацію антиадренергічних засобів, вазодилятаторів і діуретиків (адельфан, кристепін, трирезид К, тразитензин та ін.) в ефективних дозах (1-4 таблетки на добу),
антагоністи кальцію,
інгібітори ангіотензин-конвертуючого ферменту (капотен, еналаприл, раміприл та ін.),
бета-адреноблокатори.
ФАРМАКОТЕРАПІЯ ТРАНЗИТОРНИХ ІШЕМІЧНИХ АТАК.
1. Нормалізація артеріального тиску.
А) При серцевій недостатності й зниженні систолічного артеріального тиску нижче 120 мм рт. ст. призначають кардіотонічні засоби:
корглікон 1 мл 0, 06% розчину або
строфантин К 0,25 -1 мл 0,5% розчину внутрішньовенно в ізотонічному розчині хлориду натрію,
кордіамін 1 мл підшкірно або внутрішньом’язово,
сульфокамфокаїн 2 мл розчину внутрішньом’язово.
Б) Якщо артеріальний тиск значно знижений, призначають
кофеїн 1 мл 10% розчину підшкірно або внутрішньом’язово.
В) При колапсі вводять:
строфантин К 1 мл 0, 05% розчину
мезатон 1 мл 1% розчину та
преднізолон 60-120 мг в 200 мл ізотонічного розчину натрію хлориду чи 5% розчину глюкози внутрішньовенно.
Г) При тяжкій серцевій недостатності призначають
норадреналіну гідротартрат 2-4 мл 0,1% розчину внутрішньовенно крапельно в 1000 мл 5% розчину глюкози або
дофаміну 200 мг в 400 мл 5% розчину глюкози або 0,9% розчину натрію хлориду внутрішньовенно.
Д) Для посилення дії серцевих глікозидів їх рекомендується поєднувати з анаболічними стероїдами:
ретаболілом 50 мг внутрішньом’язово 1 раз у 5 днів 5 разів,
панангіном 1 драже тричі на добу
вітамінами групи В.
Е) При помірному підвищенні артеріального тиску (систолічний не більше 180 мм рт.ст.) призначають:
дибазол 2-4 мл 1% розчину внутрішньом'язово,
папаверину гідрохлорид 1-2 мл 2% розчину внутрішньом'язово,
но-шпу 2-4 мл 2% розчину внутрішньом'язово.
2) Для покращення мозкового кровообігу призначають вазоактивні препарати:
еуфілін 10 мл 2,4% розчину в 10 мл ізотонічного розчину натрію хлориду,
кавінтон 10-20 мг внутрішньовенно крапельно в 200 мл 0,9% розчину натрію хлориду,
інстенон 2 мл внутрішньовенно крапельно в 200 мл 5% розчину глюкози або струйно в 20 мл 40% розчину глюкози,
цинаризин дозою 0,025 г тричі на день
німотоп по 60 мг 4 рази на добу.
3) Для покращення мікроциркуляції і реологічних властивостей крові призначають:
пентоксифілін 5-10 мл внутрішньовенно крапельно в 250-500 мл ізотонічного розчину натрію хлориду,
реополіглюкін або реоглюман внутрішньовенно крапельно протягом 30-60 хв.
ксантинолу нікотинат 2 мл 15% розчину внутрішньом’язово або внутрішньовенно в 200 мл ізотонічного розчину натрію хлориду,
серміон 4-8 мг в 100-200 мл ізотонічного розчину натрію хлориду внутрішньовенно при супровідній артеріальній гіпертензії.
4. При тенденції до гіперкоагуляції або коли ТІА протікає з вираженою вогнищевою симптоматикою з метою попередження інсульту превентивно призначають
а) антикоагулянти прямої дії
гепарин по 5-10 тис. ОД підшкірно 2-4 рази на добу (продовжуючи час згортання у два рази) протягом 3-7 днів,
б) непрямої дії (знижуючи протромбіловий індекс до 50-40% в стаціонарі та до 55-60% в амбулаторних умовах, не допускаючи гематурії):
пелентан 0,1-0,3 г,
фенілін 0,015-0,03г,
синкумар 0,004г,
омефін 0,05г,
фепромарон 0,005г
двічі-тричі на добу протягом 2-3 тижнів з поступовим зниженням дози
в) антиагреганти:
ацетилсаліцилова кислота дозою 1 мг/кг ваги тіла 1 раз на добу,
трентал 5 мл 2% розчину внутрішньовенно крапельно або в таблетках по 0,2 (протипоказаний при інфаркті міокарда, не слід поєднувати з гепарином, не давати натще)
агапурин по 1 таблетці тричі на добу,
ксантинолу нікотинат 1-2 мл 15% розчину внутрішньом'язово
курантил по 0,025 г 2-3 рази на добу (протипоказаний при низькому артеріальному тиску, коронарній недостатності),
солкосерил 10-20 мл внутрішньовенно крапельно 5-7 днів,
тиклід (тиклопідин) по 0,25 г двічі на добу до 2-3 місяців,
плавікс (клопідогрель) 75 мг на добу,
пармідин 0,5 г тричі на добу,
танакан по 40 мг тричі на добу.
5. Для боротьби з набряком мозку застосовують:
гліцерин дозою 0,5-1,5 г/кг на добу всередину або внутрішньовенно крапельно дозою 50 мл 10% розчину в 200 мл ізотонічного розчину натрію хлориду,
ізосорбіт 1-2 г/кг крапельно у вигляді 50% розчину,
манітол 150-200 мл 10-20% розчину внутрішньовенно крапельно,
фуросемід 0,04-0,08 г вранці,
дихлотіазид 0,025-0,1 г вранці,
етакринову кислоту 0,05 г вранці,
лазикс 2 мл 1% розчину внутрішньом’язово або внутрішньовенно в 40 мл ізотонічного розчину натрію хлориду або з 10 мл 2,4% розчину еуфіліну,
тріампур 1-2 таблетки вранці,
дексон 4-8 мг внутрішньом’язово або внутрішньовенно,
альбумін людської сироватки дозою 50-100 мл 5% розчину внутрішньовенно крапельно,
антигістамінні засоби (супрастин, димедрол дозою 2 мл 1% розчину внутрішньом’язово).
6. Для покращання нейронального метаболізму призначають ноотропи:
ноотропіл 5-10 мл 20% розчину внутрішньовенно повільно або по 1 капсулі тричі на добу,
енцефабол (піридитол) по 1 драже тричі на добу,
інстенон 2 мл внутрішньовенно крапельно або внутрішньом'язово,
солкосерил 10-20 мл внутрішньовенно крапельно,
актовегін 2 мл внутрішньом'язово або 5-10 мл внутрішньовенно крапельно (протипоказаний при серцево-судинній недостатності, олігоурії, набряку легень),
церебролізин 1-5 мл 15% розчину внутрішньом'язово,
вітаміни групи В внутрішньом'язово,
АТФ 1мл внутрішньом'язово,
кокарбоксилаза 50-100 мг внутрішньом'язово.
7. Показана антиоксидантна терапія:
токоферола ацетат 1 мл внутрішньом'язово,
тіатріазолін 1 мл внутрішньом'язово,
емоксипін 3 мл внутрішньом'язово.
8. Симптоматична терапія:
а) при запамороченні - белоїд (беласпон, белатамінал) по 1 драже тричі на добу,
б) при блюванні та гикавці - аміназин (1 мл 2,5% розчину внутрішньом’язово), валідол (1 таблетка під язик), галоперидол (1,5-2 мг) через рот, або дроперидол (1-2 мл 0,25% розчину) внутрішньом’язово або 1 мл в 20 мл 40% розчину глюкози внутрішньовенно, сибазон (2-4 мл 0,5% розчину у вену), тіетилперазин (1 драже 2-3 рази на добу або 1-2 мл внутрішньом’язово), церукал (0,01 перорально або 2 мл внутрішньом’язово 0,5% розчину),
в) при інтенсивних цефалгіях - баралгін (спазган) по 5 мл внутрішньом’язово, внутрішньовенно, аналгін, седалгін, пенталгін, гірчичники на комірцеву зону,
г) для зменшення проникності судин - рутин (0,02 г), аскорбінову кислоту (0,25 г), аскорутин (1 таблетка), дицинон (0,25 г), кальцію глюконат (0,5 г), вікасол (0,015 г) тричі на добу всередину.
д) для усунення вегетативних розладів, ангіодистонічних порушень - седативні засоби та транквілізатори: бром з валеріаною, корвалол, інстенон перорально, димедрол, піпольфен, белоїд, белатамінал, валокордин, анаприлін, піроксан.
9. Хірургічне лікування призначають при повторних ТІА, зумовлених патологією магістральних судин голови в екстракраніальному відділі. Перед операцією проводять ультразвукову доплерографію екстра- та інтракраніальних судин голови, при необхідності - церебральну ангіографію. Покази до хірургічного лікування:
1) гемодинамічно значущий стеноз внутрішньої сонної артерії з повторними ТІА або з незначною залишковою органічною неврологічною симптоматикою;
2) патологічна звивистість внутрішньої сонної артерії;
3) гостре закупорення сонної артерії на шиї з вираженою вогнищевою симптоматикою без втрати свідомості в перші 6-12 годин;
4) атеросклеротичний стеноз, закупорення хребетних артерій на місці їх відходження або стискання хребетної артерії остеофітами;
5) закупорення підключичної артерії у проксимальному відділі.
ПРОФІЛАКТИКА МПМК включає своєчасну діагностику та лікування основного захворювання (атеросклерозу, гіпертонічної хвороби, серцевої патології, цукрового діабету, васкулітів) на тлі якого виникають МПМК, корекцію факторів ризику, які спричинюють прогресування судинної патології мозку (зловживання алкоголем, куріння, і особливо - поєднаня цих факторів, надлишкова вага тіла).
Важливу роль у профілактиці МПМК відіграють наступні фактори:
1. правильна організація режиму праці й відпочинку,
2. додержання режиму харчування. Дієту слід збагачувати вітамінами, калієм, магнієм, йодом. Кількість кухонної солі обмежують до 4-6 г на добу. Слід обмежити продукти, які збуджують центральну нервову систему: міцний чай, каву, какао, алкоголь, а також гострі закуски, приправи, копчені продукти;
3. вирішення соціальних проблем.
ПРАЦЕЗДАТНІСТЬ. При минущих порушеннях мозкового кровообігу хворі повинні бути визнані тимчасово непрацездатними. Питання про працездатність в майбутньому залежить від характеру перебігу основного судинного захворювання, ефективності лікування, особливостей умов праці. При частих повторних МПМК необхідно працевлаштувати хворого для виключення нервово-психічного та фізичного навантаження чи направити хворого на МСЕК для встановлення групи інвалідності.
ГОСТРА ГІПЕРТОНІЧНА ЕНЦЕФАЛОПАТІЯ
Гостра гіпертонічна енцефалопатія виникає здебільшого на тлі злоякісної артеріальної гіпертонії, ниркової гіпертонії, еклампсії, при підйомах систолічного артеріального тиску вище 200-270 мм рт. ст. і діастолічного - вище 120 мм рт. ст.
ПАТОГЕНЕЗ. Розвиток гострої гіпертонічної енцефалопатії пов’язують з інфільтраційним набряком і набуханням мозку у відповідь на збільшення мозкового кровообігу при високому артеріальному тиску із інтравазальними геморагіями і плазморагіями, які розвиваються у м’якій мозковій оболонці півкуль великого мозку і мозковому стовбурі (Ганнушкіна І. В., Лебедєва Н.В., 1987). Окрім того, набряк мозку призводить до зниження мозкового кровообігу з виникнення вогнищ розм’якшення паренхіми мозку і геморагій.
КЛІНІКА. Відмінною особливістю клініки гострої гіпертонічної енцефалопатії є швидкий розвиток, тривалий перебіг (більше доби), важкість стану хворого та резистентність до гіпотензивної терапії. Клінічна картина характеризується появою загальномозкових та вогнищевих симптомів, із значною перевагою перших.
1. Із загальномозкових проявів спостерігається наступна неврологічна симптоматика:
дифузний головний біль, тупого, розпираючого характеру, рідше він локалізується в потиличній ділянці. Нерідко біль іррадіює в очні яблука;
нудота, блювання;
відчуття шуму в голові та вухах;
запаморочення, переважно несистемного характеру;
розлади зору у вигляді яскравих плям, зірочок, спіралей, короткочасних випадінь поля зору або різким зниженням зору аж до сліпоти;
вегетативно-судинні розлади: гіперемія або блідість обличчя, біль у ділянці серця, серцебиття або брадикардія, сухість у роті, гіпергідроз;
розлади емоційно-психічної сфери: подразливість, занепокоєння.
У важких випадках спостерігають:
- порушення свідомості,
- оглушення,
- сонливість,
- психомоторне збудження,
- дезорієнтацію у просторі та часі,
- епілептичні напади,
- кома.
Можлива поява менінгеальних симптомів: ригідність потиличних м’язів, симптоми Керніга, Брудзинського. На очному дні виявляють застійні диски зорових нервів, стази, дрібні крововиливи, розширення вен, інколи - явища альбумінуричного ретиніту.
2. Із вогнищевих симптомів нерідко спостерігається:
затерпання кінцівок,
зниження больової чутливості в ділянці обличчя, язика;
анізорефлексія сухожилкових та периостальних рефлеків;
порушення чутливості за гемітипом,
координаційні розлади;
чіткі субкортикальні рефлекси: Марінеску-Радовічі, губний рефлекс Бехтерева.
Діагностика. Поперековий прокол виявляє значне підвищення внутрішньочерепного тиску - до 500-600 мм вод. ст. Кількість білка та клітинний склад ліквору не змінюються, однак інколи з’являється білково-клітинна дисоціація. На комп’ютерній томограмі спостерігають ознаки набряку тканини головного мозку. Характерні зміни біохімічних показників крові: гіперглікемія, гіперхолестеринемія, підвищення вмісту гістаміну, а також лейкоцитів.
Гостра гіпертонічна енцефалопатія частково або повністю регресує на фоні лікування протягом декількох діб, але інколи може закінчуватися летально.
ЛІКУВАННЯ. 1. Нормалізація артеріального тиску. При гострій гіпертонічній енцефалопатії не слід швидко і значно знижувати артеріальний тиск. Доцільно підтримувати його на рівні близько 150/100 мм рт. ст. Найкращими гіпотензивними препаратами для цього вважаються:
нітропрусид натрію внутрішньовенно під постійним контролем артеріального тиску зі швидкістю 8 мкг/кг за хвилину,
гангліоблокатори: пентамін 0,5-1 мл 5% розчину внутрішньом’язево або внутрішньовенно струйно,
арфонад 5 мл 0,5-1% розчину в 100 мл ізотонічного розчину натрію хлориду,
бензогексоній 1-2 мг 2,5% розчину внутрішньовенно.
2. Для боротьби з набряком мозку та зниження внутрішньочерепного тиску вводять
еуфілін 10 мл 2,4% розчину з лазиксом 2-4 мл 1% розчину в 10 мл ізотонічного розчину натрію хлориду внутрішньовенно,
альбумін людської сироватки 50-100 мл 5% розчину внутрішньовенно крапельно,
антигістамінні засоби: супрастин 2 мл 1% розчину
або димедрол 2 мл 1% розчину в 100 мл ізотонічного розчину натрію хлориду внутрішньовенно крапельно.
сульфат магнію 10-20 мл 25% розчину внутрішньом’язово.
3. Для зняття психомоторного збудження, епілептичних нападів:
дроперидол 1-2 мл 2,5% розчину в 20 мл ізотонічного розчину натрію хлориду внутрішньовенно струйно,
сибазон 2-4 мл 0,5% розчину внутрішньом’язово.
4. Симптоматична терапія:
при цефалгічному синдромі - аналгін, спазгам, седалгін, трамал, трамадол, піроксикам.
при блюванні та гикавці - церукал, галоперидол, аміназин, валідол;
Після нормалізації артеріального тиску переходять на звичні пероральні гіпотензивні препарати. Застосування спазмолітиків (папаверин, но-шпа) при гострій гіпертонічній енцефалопатії протипоказане.
|
СУДИННІ ЗАХВОРЮВАННЯ ГОЛОВНОГО ТА СПИННОГО МОЗКУ |
КЛАСИФІКАЦІЯ СУДИННИХ ЗАХВОРЮВАНЬ ГОЛОВНОГО ТА СПИННОГО МОЗКУ
Згідно із сучасною Міжнародною класифікацією хвороб Десятого перегляду (1995 рік), виділяють такі основні клінічні форми порушень мозкового кровообігу:
А. Початкові прояви недостатності кровопостачання мозку.
І. Початкові прояви недостатності кровопостачання головного мозку.
2. Початкові прояви недостатності кровопостачання спинного мозку.
Б. Гострі порушення мозкового кровообігу.
1. Минущі порушення мозкового кровообігу:
а) транзиторні ішемічні атаки;
б) гіпертонічні церебральні кризи.
2. Гостра гіпертонічна енцефалопатія.
3. Крововилив оболонковий:
а) підпавутинний (субарахноїдальний);
б) епі - та субдуральний.
4. Крововилив у мозок:
а) паренхіматозний;
б) паренхіматозно-субарахноїдальний;
в) шлуночковий.
5. Інфаркт мозку (неемболічний):
а) при патології магістральних артерій голови;
б) при патології внутрішньомозкових судин;
в) іншого генезу.
6. Інфаркт мозку емболічний:
а) кардіогенний;
б) іншого генезу.
В. Повільно прогресуючі порушення мозкового кровообігу.
1. Дисциркуляційна енцефалопатія.
2. Дисциркуляційна мієлопатія.
Г. Наслідки раніше перенесеного мозкового інсульту.
ПРИЧИНИ І ФАКТОРИ РИЗИКУ
До факторів ризику виникнення порушень мозкового кровообігу відносяться фізіологічні, поведінкові, а також фактори зовнішнього середовища, які збільшують ризик судинних захворювань нервової системи.
Фактори ризику - це не причина хвороби, вони лише відображають зв’язок з етіологічним чинником розвитку захворювання. Є багато причин, що викликають розлади мозкового кровообігу. Але найбільш частих причин є три:
1. Атеросклероз мозкових судин та загальний атеросклероз - він є причиною у 75 % випадків усіх гострих розладів мозкового кровообігу;
2. Гіпертонічна хвороба - частота артеріальної гіпертензії при інсульті становить 72 %;
3. Поєднання атеросклерозу з гіпертонічною хворобою.
Крім цих основних причин необхідно назвати інші, які можуть призвести до тих чи інших порушень мозкового кровообігу:
4. Симптоматична артеріальна гіпертензія (наприклад, при захворюванні нирок);
5. Хвороби серця, такі як уроджені та набуті вади, порушення ритму, ІХС, кардіосклероз, стенокардія, перенесений інфаркт міокарду тощо;
6. Інфекційні та інфекційно-алергічні васкуліти (при колагенозах, ревматизмі, люесі тощо);
7. Артеріальна гіпотонія;
8. Вазомоторні дистонії;
9. Захворювання крові (поліцитимія, лейкози, гемофілія тощо);
10. Захворювання нирок;
11. Захворювання ендокринних залоз (щитовидної, підшлункової, наднирників);
12. Цукровий діабет;
13. Токсичні ураження судин при екзогенних та ендогенних інтоксикаціях (наприклад, при гострій та хронічній нирковій чи печінковій недостатності, алкогольній інтоксикації, токсикозах другої половини вагітності);
14. Травматичні ураження судин при крововиливах (субдуральному, епідуральному, паренхіматозному, вентрикулярному);
15. Стиснення артерій та вен, особливо у шийному відділі хребта (при остеохондрозі);
16. Аномалії (вроджені та набуті) будови Вілізієва кола (оклюзії та стенози магістральних артерій голови і шиї, уроджені дефекти будови судин головного мозку типу аневризми, петлі, звуження, недорозвитку);
17. Пухлини головного мозку.
У дітей серед захворювань, що призводять до порушення мозкового кровообігу, на першому місці стоять хвороби крові, потім інтра- та постнатальні черепно-мозкові травми, інфекційно-алергічні васкуліти та уроджені аномалії мозкових судин. Причому, на різних етапах розвитку дитини етіологічне значення цих різноманітних факторів не однакове. Якщо на першому році життя дитини клінічно проявляються аномалії розвитку аретріальної чи венозної системи, то у дошкільному та шкільному віці важливе етіологічне значення набувають хвороби крові (лейкози, діатези, анемії), васкуліти (при ревматизмі, грипі, кору) та порушення гемодинаміки при вроджених і набутих вадах серця. У пубертатному періоді причиною дизгемій виявляється вегето-судинна дистонія.
Для реалізації згаданих причин розвитку порушень мозкового кровообігу необхідно їх поєднання з факторами ризику, серед яких основними являються:
вік хворого (чим старший вік, тим ймовірніший розвиток судинної патології);
стать (до 55-60 років смертність від судинної патології головного мозку більша у чоловіків, після 55-60 років - у жінок);
генетична схильність до серцевої та церебральної судинної патології;
зловживання нікотином та алкоголем;
гіперліпідемія та гіперглікемія;
артеріальна гіпертензія, яка є і причиною, і фактором ризику одночасно;
емоційні стреси;
гіподинамія, недостатня фізична активність;
метеозалежність (особливо у осіб з підвищеною лабільністю вегетативної нервової системи, коли зміни атмосферного тиску, вологості та радіації викликають різноманітні розлади мозкового кровообігу);
особливості конституції (пікнічна будова), режиму праці (робота, пов'язана з нервово-психічним напруженням), харчування (вживання багатої на вуглеводи їжі).
При поєднанні трьох і більше несприятливих факторів ймовірність виникнення інсульту зростає. Тому з урахуванням факторів ризику і факторів, які запобігають розвитку судинних уражень мозку, повинні будуватись раціональні методи індивідуальної і суспільної профілактики.
КРОВОПОСТАЧАННЯ ГОЛОВНОГО МОЗКУ
У фізіологічних умовах кожні 100 грам тканини головного мозку в стані спокою отримують 55-58 мл крові, споживають 3-5 мл кисню за хвилину. Тобто на головний мозок, вага якого у дорослої людини складає лише 2% від маси тіла, припадає 750-1000 мл крові, майже 20% всього кисню і приблизно стільки ж глюкози за хвилину. Постійне надходження кисню, глюкози необхідне для збереження енергетичного субстрату мозку, нормального функціонування нейронів, підтримання їх інтегративної функції (С.М.Віничук, 1999).
Головний мозок забезпечується кров’ю двома парними магістральними артеріями голови - внутрішніми сонними та хребетними. Дві третини крові доставляються в мозок внутрішніми сонними артеріями і одна третина - хребетними. Перші утворюють каротидну систему, другі - вертебрально-базилярну. Внутрішні сонні артерії є гілками загальної сонної артерії. Вони входять у порожнину черепа через внутрішній сонний отвір, вступають у кавернозний синус, де роблять S-подібний вигин. Ця частина внутрішньої сонної артерії отримала назву сифону, або кавернозної частини. Потім вона проходить через тверду мозкову оболонку і віддає першу гілку - очну артерію, яка разом із зоровим нервом через зоровий канал проходить у порожнину очниці. В подальшому від внутрішньої сонної артерії відходять ще задня сполучна артерія та передня ворсинчаста артерія. Латерально від перехрестя зорових нервів внутрішня сонна артерія розділяється на дві кінцеві гілки: передню і середню мозкові артерії. Передня мозкова артерія васкуляризує передній відділ лобної частки і внутрішню поверхню півкулі, середня мозкова артерія - значну частину кори лобної, тім’яної і скроневої часток, підкіркові ядра та більшу частину внутрішньої капсули.

Рис. 1.Система мозкових судин з найбільш важливими анастомозами (за С.М.Віничук, 1999).
Хребетні артерії відходять від підключичної артерії. Вони проходять до черепа через отвори в поперечних відростках перших шести шийних хребців і входять у порожнину черепа крізь великий потиличний отвір. У ділянці мозкового стовбуру (моста) обидві хребетні артерії зливаються в один спільний стовбур - базилярну артерію, яка поділяється на дві задні мозкові артерії. Вони живлять кров'ю середній мозок, міст, мозочок і потиличні частки півкуль великого мозку. Крім того, від хребетної артерії відходять дві спинномозкові артерії (передня і задня), а також задня нижня артерія мозочка.
Обидві передні мозкові артерії з’єднує передня сполучна артерія; задні сполучні артерії з’єднують середні та задні мозкові артерії. У результаті з'єднання між собою судин каротидного і вертебро-базилярного басейнів на нижній поверхні півкуль мозку утворюється замкнена система - артеріальне (вілізієве) коло великого мозку. Розрізняють чотири рівні колатерального артеріального кровопостачання головного мозку: система артеріального (вілізієвого) кола великого мозку ; система анастомозів на поверхні та всередині головного мозку - через капілярну сітку між гілками передньої, середньої та задньої мозкових артерій ; позачерепний рівень анастомозів - між гілками екстра- та інтракраніальних судин голови

Рис. 2. Система колатералей між внутрішніми сонними та між зовнішньою і внутрішньою сонними артеріями (за С.М.Віничук, 1999)
Колатеральне кровопостачання головного мозку має важливе значення в компенсації порушень кровообігу при закупоренні однієї з мозкових артерій. Разом з тим, численні анастомози між різними судинними басейнами можуть відігравати і негативну роль щодо самого головного мозку. Прикладом цього можуть бути церебральні синдроми “обкрадання “ (Steal syndrom).
Необхідно також зазначити, що в підкірковій ділянці анастомозів немає зовсім, внаслідок чого при ураженні однієї із артерій у ділянці, що кровопостачається нею, настають незворотні зміни тканини мозку.
Судини головного мозку залежно від їх функції розподіляються на декілька груп. Магістральні, або регіонарні, судини - це внутрішні сонні та хребетні артерії в екстракраніальному відділі, а також судини вілізієвого кола. Основне їх призначення - регуляція мозкового кровообігу при змінах системного артеріального тиску. Піальні артерії - судини з явно вираженою нутрітивною функцією. Розмір їх просвіту залежить від обмінних потреб тканини мозку. Головним регулятором тонусу цих судин є продукти метаболізму мозкової тканини, особливо вуглекислота, під впливом якої судини мозку розширюються. Внутрішньомозкові артерії та капіляри безпосередньо забезпечують одну із основних функцій серцево-судинної системи - обмін між кров’ю і тканиною мозку. Це “обмінні судини”. Венозна система виконує переважно дренажну функцію. Вона характеризується значно більшою ємкістю, порівняно з артеріальною системою. Тому вени мозку називають ще “ємкісними судинами”. Вони не залишаються пасивним елементом судинної системи головного мозку, а беруть участь у регуляції мозкового кровообігу.
Через поверхневі та глибокі вени мозку із судинних сплетень і глибоких відділів мозку відбувається відтік венозної крові в прямий (через велику вену Галена) та інші венозні синуси твердої мозкової оболонки. Із синусів кров відтікає у внутрішні яремні вени, потім у плечоголовні й у верхню порожнисту вену.
АВТОРЕГУЛЯЦІЯ МОЗКОВОГО КРОВООБІГУ
Серед соматичних органів головний мозок особливо чутливий до гіпоксії, найбільш уразливий при ішемії з декількох причин: по-перше, у зв’язку з високими енергетичними потребами тканини мозку; по-друге, через відсутність тканинного депо кисню; по-третє, у зв’язку з відсутністю резервних капілярів. Якщо величина мозкового кровотоку знижується до 35-40 мл на 100 г речовини мозку за хвилину, то через дефіцит кисню, що настає, порушується розщеплення глюкози, а це призводить до накопичення молочної кислоти, розвитку ацидозу, гемореологічних і мікроциркуляторних розладів, виникнення неврологічного дефіциту.
Адекватне кровопостачання головного мозку забезпечується механізмами авторегуляції. Термін “авторегуляція” мозкового кровообігу використовується для позначення спроможності гомеостатичних систем організму підтримувати тканинний мозковий кровотік на постійному рівні, незалежно від змін системного артеріального тиску, метаболізму, впливу вазоактивних факторів.
Регуляція мозкового кровообігу забезпечується комплексом міогенних, метаболічних і неврогенних механізмів. Роль міогенного фактора полягає в тому, що підвищення артеріального тиску викликає скорочення м'язового шару судин і, навпаки, зниження тиску крові викликає розслаблення м'язових волокон і розширення просвіту судин (ефект Остроумова-Бейліса). Міогенний механізм може реалізуватися при коливаннях систолічного тиску в діапазоні від 60-70 до 170-180 мм рт. ст. При зниженні його до 50 мм рт. ст., як і при значному підвищенні (понад 180 мм рт. ст.), з’являється пасивна залежність: тиск - мозковий кровотік, тобто виникає зрив реакції авторегуляції мозкового кровообігу.
Які ж механізми захищають головний мозок від надлишкової перфузії? Виявляється, що їх забезпечують внутрішні сонні та хребетні артерії. Вони не тільки регулюють об’єм надходження крові в мозкові судини, але й забезпечують постійність її притоку, незалежно від змін рівня загального артеріального тиску. Міогенний механізм авторегуляції включається миттєво, але він недовготривалий - від однієї секунди до двох хвилин. Потім він пригнічується змінами метаболізму.
Метаболічний механізм авторегуляції передбачає тісний взаємозв’язок кровопостачання мозку з його метаболізмом. Цю функцію забезпечують піальні артерії, які широко розгалужуються на поверхні мозку.
Однак ні міогенний, ні метаболічний механізми окремо не можуть пояснити складних процесів регуляції тонусу мозкових судин і забезпечити підтримку мозкового кровотоку на постійному рівні. Мабуть, механізми авторегуляції здійснюються за рахунок взаємодії двох факторів: міогенного рефлексу судинної стінки у відповідь на зміни перфузійного тиску та дії метаболітів мозкової тканини, таких як О2 і СО2
У регуляції мозкового кровотоку бере участь і неврогенний механізм, але значення його остаточно не вивчено. Вважають, що цей механізм забезпечується в основному судинними нервами.
Авторегуляція мозкового кровообігу - легко вразливий механізм, який може порушуватися при гіпоксії, гіперкапнії, різкому підвищенні або зниженні артеріального тиску. Зрив реакції авторегуляції - це стан, при якому тканинний мозковий кровотік пасивно залежить від системного артеріального тиску. Це може супроводжуватися синдромами “надлишкової перфузії” (luxury perfusion syndrome) та “реактивної гіперемії”.
ПОЧАТКОВІ ПРОЯВИ НЕДОСТАТНОСТІ КРОВОПОСТАЧАННЯ ГОЛОВНОГО МОЗКУ
Початкові прояви недостатності кровопостачання мозку - це ранні компенсовані дисциркуляційні енцефалопатії, які не супроводжуються органічною неврологічною симптоматикою і є проявом загальної судинної патології.
Початкові прояви недостатності кровопостачання мозку (ППНКМ) виділені у самостійну форму цереброваскулярної патології у рамках існуючої в Україні класифікації судинних захворювань нервової системи. Це має принципове значення, оскільки своєчасно встановлений діагноз забезпечує більш високу ефективність лікувальних і профілактичних заходів.
ЕТІОЛОГІЯ. Початкові прояви недостатності кровопостачання мозку розвиваються на тлі системних судинних захворювань:
церебрального атеросклерозу,
артеріальної гіпертонії,
вегетативно-судинної дистонії.
ПАТОГЕНЕЗ. Підвищена реактивність судинної системи, неадекватні гемодинамічні реакції, дисфункція надсегментарних центрів гіпоталамічної зони та довгастого мозку маніфестує вегетативно-судинними пароксизмами, астенією та іншими неврологічними порушеннями регіонального та загального характеру.
У патогенезі ППНКМ значну роль відіграють наступні механізми:
а) зміни кардіогемодинаміки,
б) порушення серцевої діяльності,
в) наявність тісних цереброкардіальних взаємозв’язків,
г) дистонічні зміни судин головного мозку,
д) ангіопарез зі сповільненням кровотоку,
е) порушенням венозного відтоку,
є) патологія магістральних артерій голови
- стеноз внутрішніх сонних,
- стеноз хребетних артерій,
- стенози судин вілізієвого кола,
ж) порушення реологічних властивостей крові та мікроциркуляції,
з) порушення нейронального метаболізму,
и) порушення функціонального стану головного мозку.
КЛІНІКА. Виділяють три варіанти клінічного перебігу ППНКМ:
а) доклінічний,
б) клінічний,
в) пароксизмальний.
Доклінічний (безсимптомний) варіант перебігу характеризується ознаками вегетативно-судинної дистонії:
1. акроціанозом,
2. акрогіпергідрозом,
3. стійким червоним дермографізмом,
4. блідістю або почервонінням шкіри,
5. тремтінням пальців рук, повік,
6. пожвавленням сухожилкових рефлексів,
7. нестабільністю артеріального тиску.
Скарги з'являються лише при фізичних та емоційних навантаженнях, а ознаки недостатності мозкового кровопостачання діагностується лише при функціональних пробах:
1. зміни біоелектричної активності головного мозку, гіперсинхронний і десинхронний типи ЕЕГ;
2. на реоенцефалограмах - підвищення або зниження тонусу судинної стінки, лабільність пульсових хвиль, міжпівкульну асиметрію, утруднення венозного відтоку;
3. на ЕКГ - синусова аритмія, порушення фази деполяризиції, зміщення сегмента ST і зубця Т;
4. зміни біохімічних показників характеризуються збільшенням вмісту холестерину, тригліцеридів, бета-ліпопротеїдів.
Клінічний (перманентний) варіант перебігу ППНКМ проявляється суб’єктивними ознаками недостатності кровопостачання мозку. Найчастіше хворі скаржаться на:
1. зниження розумової працездатності,
2. головний біль,
3. запаморочення,
4. шум у голові,
5. розлади пам’яті.
Підставою для встановлення діагнозу може бути тільки поєднання названих двох або більше суб’єктивних симптомів, які відносно довго існують і часто повторюються (не рідше одного разу на тиждень протягом останніх 3-х місяців). Характерне посилення цих скарг під час розумового напруження, особливо в умовах гіпоксії, перевтоми, поганого сну. Після відпочинку стан хворого покращується або повністю нормалізується. Вогнищевої неврологічної симптоматики у таких хворих не спостерігають, але можуть виявлятися:
- субкортикальні рефлекси,
- асиметрія черевних рефлексів,
- пожвавлення сухожилкових та периостальних рефлексів.
У хворих знаходять ознаки загального судинного захворювання:
- коронарокардіосклероз,
- гіпертрофію лівого шлуночка серця,
- зміни судин очного дна (ангіопатія),
- симптоми атеросклеротичного ураження інших ділянок.
Діагноз підтверджується також змінами біопотенціалів мозку, реоенцефалографічних (РЕГ), доплерографічних, біохімічних показників.
Пароксизмальний перебіг ППНКМ зустрічається переважно у хворих з вегетативно-судинною дистонією, артеріальною гіпертензією і значно рідше - при атеросклерозі. Домінуючими в клінічній картині є вегетативно-судинні пароксизми типу:
- цефалгічних,
- вестибулярних,
- синкопальних,
- симпатико-адреналових,
- вагоінсулярних,
- змішаних.
Пароксизмальні розлади в більшості випадків є проявом дисфункції надсегментарного рівня вегетативної нервової системи, зокрема, утворів лімбіко-ретикулярного комплексу.
ДІАГНОЗ ППНКМ встановлюють на підставі скарг, клінічної картини захворювання, а також за допомогою електрофізіологічних і лабораторних методів дослідження. Має значення виявлення симптомів загального судинного захворювання: атеросклерозу, артеріальної гіпертензії, вегетативно-судинної дистонії.
ЛІКУВАННЯ хворих з ППНКМ має особливе значення, оскільки неврологічні розлади на цій стадії захворювання зворотні, а тому своєчасна терапія є одночасно і профілактикою гострих порушень мозкового кровообігу. Розроблена система поетапного лікування хворих: поліклініка - стаціонар - курорт - поліклініка, яка включає диспансерний нагляд. На кожному з етапів застосовуються сучасні схеми обстеження та лікування хворих з урахуванням варіанту клінічного перебігу та загального судинного захворювання.
Важливими є наступні аспекти лікування:
- Нормалізація режиму праці та відпочинку:
а) необхідно усунути різні психоемоційні фактори,
б) забезпечити повноцінний сон і відпочинок,
- Дотримання режиму харчування:
а) необхідно уникати їжі, багатої тваринними жирами, холестерином, сіллю;
б) споживати молочно-рослинну їжу, рибу, відварене м’ясо.
- Рекомендоване санаторно-курортне лікування, ЛФК, масаж.
- Медикаментозне лікування спрямовують на терапію основного судинного захворювання. Показані наступні групи препаратів:
1. Седативні - бром, ново-пасіт, саносан, персен, валеріана.
2. Малі транквілізатори - феназепам, гідазепам, трансен.
3. Тонізуючі засоби при пониженому артеріальному тиску - кофеїн, пантокрин, настоянка китайського лимонника, настоянка женьшеню
4. Вазоактивні препарати, що покращують мозковий кровообіг - кавінтон, інстенон.
5. Ноотропні засоби, які покращують нейрональний метаболізм - ноотропіл, пірацетам, церебролізин, актовегін, енцефабол тощо.
6. Антиагреганти при гемореологічних порушеннях - курантил, трентал, агапурин, серміон.
7. Спазмолітики та гіпотензивні препарати - дибазол, папаверин, еуфілін, платифілін, клофелін.
8. Антагоністи кальцію - ніфедипін, ділтіазем.
9. Ліпотропні засоби - метіонін, ліпостабіл, цетаміфен, поліспонін, клофібрат, місклерон, лінетол, ловастатин, зокор.
Якщо у хворого є виражені симптоми гіпертонічної хвороби, ІХС, атеросклерозу, цукрового діабету, то це зумовлює призначення додаткових медикаментозних комбінацій, згідно рекомендацій кардіолога, ендокринолога та ін.
З фізіотерапевтичних методів лікування слід призначити:
1. електрофорез спазмолітиків чи аналгетиків на комірцеву зону,
2. масаж шийного відділу хребта,
3. рефлексотерапію,
4. електросон.
ПРОФІЛАКТИКА. Систему заходів первинної профілактики спрямована на запобігання розвитку судинного захворювання головного мозку: усунення факторів ризику, поліпшення умов праці, побуту, здоровий спосіб життя. Вторинна профілактика передбачає раннє виявлення, облік хворих з ППНКМ, своєчасне їх лікування з метою попередження розвитку цереброваскулярної патології головного мозку. Лікування хворих можливо проводити в умовах денних стаціонарів з застосуванням немедикаментозних методів терапії. Велику роль у профілактиці ППНКМ відіграють диспансеризація хворих, планові неврологічні профогляди.
Згідно із сучасною Міжнародною класифікацією хвороб Десятого перегляду (1995 рік), виділяють такі основні клінічні форми порушень мозкового кровообігу:
А. Початкові прояви недостатності кровопостачання мозку.
І. Початкові прояви недостатності кровопостачання головного мозку.
2. Початкові прояви недостатності кровопостачання спинного мозку.
Б. Гострі порушення мозкового кровообігу.
1. Минущі порушення мозкового кровообігу:
а) транзиторні ішемічні атаки;
б) гіпертонічні церебральні кризи.
2. Гостра гіпертонічна енцефалопатія.
3. Крововилив оболонковий:
а) підпавутинний (субарахноїдальний);
б) епі - та субдуральний.
4. Крововилив у мозок:
а) паренхіматозний;
б) паренхіматозно-субарахноїдальний;
в) шлуночковий.
5. Інфаркт мозку (неемболічний):
а) при патології магістральних артерій голови;
б) при патології внутрішньомозкових судин;
в) іншого генезу.
6. Інфаркт мозку емболічний:
а) кардіогенний;
б) іншого генезу.
В. Повільно прогресуючі порушення мозкового кровообігу.
1. Дисциркуляційна енцефалопатія.
2. Дисциркуляційна мієлопатія.
Г. Наслідки раніше перенесеного мозкового інсульту.
ПРИЧИНИ І ФАКТОРИ РИЗИКУ
До факторів ризику виникнення порушень мозкового кровообігу відносяться фізіологічні, поведінкові, а також фактори зовнішнього середовища, які збільшують ризик судинних захворювань нервової системи.
Фактори ризику - це не причина хвороби, вони лише відображають зв’язок з етіологічним чинником розвитку захворювання. Є багато причин, що викликають розлади мозкового кровообігу. Але найбільш частих причин є три:
1. Атеросклероз мозкових судин та загальний атеросклероз - він є причиною у 75 % випадків усіх гострих розладів мозкового кровообігу;
2. Гіпертонічна хвороба - частота артеріальної гіпертензії при інсульті становить 72 %;
3. Поєднання атеросклерозу з гіпертонічною хворобою.
Крім цих основних причин необхідно назвати інші, які можуть призвести до тих чи інших порушень мозкового кровообігу:
4. Симптоматична артеріальна гіпертензія (наприклад, при захворюванні нирок);
5. Хвороби серця, такі як уроджені та набуті вади, порушення ритму, ІХС, кардіосклероз, стенокардія, перенесений інфаркт міокарду тощо;
6. Інфекційні та інфекційно-алергічні васкуліти (при колагенозах, ревматизмі, люесі тощо);
7. Артеріальна гіпотонія;
8. Вазомоторні дистонії;
9. Захворювання крові (поліцитимія, лейкози, гемофілія тощо);
10. Захворювання нирок;
11. Захворювання ендокринних залоз (щитовидної, підшлункової, наднирників);
12. Цукровий діабет;
13. Токсичні ураження судин при екзогенних та ендогенних інтоксикаціях (наприклад, при гострій та хронічній нирковій чи печінковій недостатності, алкогольній інтоксикації, токсикозах другої половини вагітності);
14. Травматичні ураження судин при крововиливах (субдуральному, епідуральному, паренхіматозному, вентрикулярному);
15. Стиснення артерій та вен, особливо у шийному відділі хребта (при остеохондрозі);
16. Аномалії (вроджені та набуті) будови Вілізієва кола (оклюзії та стенози магістральних артерій голови і шиї, уроджені дефекти будови судин головного мозку типу аневризми, петлі, звуження, недорозвитку);
17. Пухлини головного мозку.
У дітей серед захворювань, що призводять до порушення мозкового кровообігу, на першому місці стоять хвороби крові, потім інтра- та постнатальні черепно-мозкові травми, інфекційно-алергічні васкуліти та уроджені аномалії мозкових судин. Причому, на різних етапах розвитку дитини етіологічне значення цих різноманітних факторів не однакове. Якщо на першому році життя дитини клінічно проявляються аномалії розвитку аретріальної чи венозної системи, то у дошкільному та шкільному віці важливе етіологічне значення набувають хвороби крові (лейкози, діатези, анемії), васкуліти (при ревматизмі, грипі, кору) та порушення гемодинаміки при вроджених і набутих вадах серця. У пубертатному періоді причиною дизгемій виявляється вегето-судинна дистонія.
Для реалізації згаданих причин розвитку порушень мозкового кровообігу необхідно їх поєднання з факторами ризику, серед яких основними являються:
вік хворого (чим старший вік, тим ймовірніший розвиток судинної патології);
стать (до 55-60 років смертність від судинної патології головного мозку більша у чоловіків, після 55-60 років - у жінок);
генетична схильність до серцевої та церебральної судинної патології;
зловживання нікотином та алкоголем;
гіперліпідемія та гіперглікемія;
артеріальна гіпертензія, яка є і причиною, і фактором ризику одночасно;
емоційні стреси;
гіподинамія, недостатня фізична активність;
метеозалежність (особливо у осіб з підвищеною лабільністю вегетативної нервової системи, коли зміни атмосферного тиску, вологості та радіації викликають різноманітні розлади мозкового кровообігу);
особливості конституції (пікнічна будова), режиму праці (робота, пов'язана з нервово-психічним напруженням), харчування (вживання багатої на вуглеводи їжі).
При поєднанні трьох і більше несприятливих факторів ймовірність виникнення інсульту зростає. Тому з урахуванням факторів ризику і факторів, які запобігають розвитку судинних уражень мозку, повинні будуватись раціональні методи індивідуальної і суспільної профілактики.
КРОВОПОСТАЧАННЯ ГОЛОВНОГО МОЗКУ
У фізіологічних умовах кожні 100 грам тканини головного мозку в стані спокою отримують 55-58 мл крові, споживають 3-5 мл кисню за хвилину. Тобто на головний мозок, вага якого у дорослої людини складає лише 2% від маси тіла, припадає 750-1000 мл крові, майже 20% всього кисню і приблизно стільки ж глюкози за хвилину. Постійне надходження кисню, глюкози необхідне для збереження енергетичного субстрату мозку, нормального функціонування нейронів, підтримання їх інтегративної функції (С.М.Віничук, 1999).
Головний мозок забезпечується кров’ю двома парними магістральними артеріями голови - внутрішніми сонними та хребетними. Дві третини крові доставляються в мозок внутрішніми сонними артеріями і одна третина - хребетними. Перші утворюють каротидну систему, другі - вертебрально-базилярну. Внутрішні сонні артерії є гілками загальної сонної артерії. Вони входять у порожнину черепа через внутрішній сонний отвір, вступають у кавернозний синус, де роблять S-подібний вигин. Ця частина внутрішньої сонної артерії отримала назву сифону, або кавернозної частини. Потім вона проходить через тверду мозкову оболонку і віддає першу гілку - очну артерію, яка разом із зоровим нервом через зоровий канал проходить у порожнину очниці. В подальшому від внутрішньої сонної артерії відходять ще задня сполучна артерія та передня ворсинчаста артерія. Латерально від перехрестя зорових нервів внутрішня сонна артерія розділяється на дві кінцеві гілки: передню і середню мозкові артерії. Передня мозкова артерія васкуляризує передній відділ лобної частки і внутрішню поверхню півкулі, середня мозкова артерія - значну частину кори лобної, тім’яної і скроневої часток, підкіркові ядра та більшу частину внутрішньої капсули.

Рис. 1.Система мозкових судин з найбільш важливими анастомозами (за С.М.Віничук, 1999).
Хребетні артерії відходять від підключичної артерії. Вони проходять до черепа через отвори в поперечних відростках перших шести шийних хребців і входять у порожнину черепа крізь великий потиличний отвір. У ділянці мозкового стовбуру (моста) обидві хребетні артерії зливаються в один спільний стовбур - базилярну артерію, яка поділяється на дві задні мозкові артерії. Вони живлять кров'ю середній мозок, міст, мозочок і потиличні частки півкуль великого мозку. Крім того, від хребетної артерії відходять дві спинномозкові артерії (передня і задня), а також задня нижня артерія мозочка.
Обидві передні мозкові артерії з’єднує передня сполучна артерія; задні сполучні артерії з’єднують середні та задні мозкові артерії. У результаті з'єднання між собою судин каротидного і вертебро-базилярного басейнів на нижній поверхні півкуль мозку утворюється замкнена система - артеріальне (вілізієве) коло великого мозку. Розрізняють чотири рівні колатерального артеріального кровопостачання головного мозку: система артеріального (вілізієвого) кола великого мозку ; система анастомозів на поверхні та всередині головного мозку - через капілярну сітку між гілками передньої, середньої та задньої мозкових артерій ; позачерепний рівень анастомозів - між гілками екстра- та інтракраніальних судин голови

Рис. 2. Система колатералей між внутрішніми сонними та між зовнішньою і внутрішньою сонними артеріями (за С.М.Віничук, 1999)
Колатеральне кровопостачання головного мозку має важливе значення в компенсації порушень кровообігу при закупоренні однієї з мозкових артерій. Разом з тим, численні анастомози між різними судинними басейнами можуть відігравати і негативну роль щодо самого головного мозку. Прикладом цього можуть бути церебральні синдроми “обкрадання “ (Steal syndrom).
Необхідно також зазначити, що в підкірковій ділянці анастомозів немає зовсім, внаслідок чого при ураженні однієї із артерій у ділянці, що кровопостачається нею, настають незворотні зміни тканини мозку.
Судини головного мозку залежно від їх функції розподіляються на декілька груп. Магістральні, або регіонарні, судини - це внутрішні сонні та хребетні артерії в екстракраніальному відділі, а також судини вілізієвого кола. Основне їх призначення - регуляція мозкового кровообігу при змінах системного артеріального тиску. Піальні артерії - судини з явно вираженою нутрітивною функцією. Розмір їх просвіту залежить від обмінних потреб тканини мозку. Головним регулятором тонусу цих судин є продукти метаболізму мозкової тканини, особливо вуглекислота, під впливом якої судини мозку розширюються. Внутрішньомозкові артерії та капіляри безпосередньо забезпечують одну із основних функцій серцево-судинної системи - обмін між кров’ю і тканиною мозку. Це “обмінні судини”. Венозна система виконує переважно дренажну функцію. Вона характеризується значно більшою ємкістю, порівняно з артеріальною системою. Тому вени мозку називають ще “ємкісними судинами”. Вони не залишаються пасивним елементом судинної системи головного мозку, а беруть участь у регуляції мозкового кровообігу.
Через поверхневі та глибокі вени мозку із судинних сплетень і глибоких відділів мозку відбувається відтік венозної крові в прямий (через велику вену Галена) та інші венозні синуси твердої мозкової оболонки. Із синусів кров відтікає у внутрішні яремні вени, потім у плечоголовні й у верхню порожнисту вену.
АВТОРЕГУЛЯЦІЯ МОЗКОВОГО КРОВООБІГУ
Серед соматичних органів головний мозок особливо чутливий до гіпоксії, найбільш уразливий при ішемії з декількох причин: по-перше, у зв’язку з високими енергетичними потребами тканини мозку; по-друге, через відсутність тканинного депо кисню; по-третє, у зв’язку з відсутністю резервних капілярів. Якщо величина мозкового кровотоку знижується до 35-40 мл на 100 г речовини мозку за хвилину, то через дефіцит кисню, що настає, порушується розщеплення глюкози, а це призводить до накопичення молочної кислоти, розвитку ацидозу, гемореологічних і мікроциркуляторних розладів, виникнення неврологічного дефіциту.
Адекватне кровопостачання головного мозку забезпечується механізмами авторегуляції. Термін “авторегуляція” мозкового кровообігу використовується для позначення спроможності гомеостатичних систем організму підтримувати тканинний мозковий кровотік на постійному рівні, незалежно від змін системного артеріального тиску, метаболізму, впливу вазоактивних факторів.
Регуляція мозкового кровообігу забезпечується комплексом міогенних, метаболічних і неврогенних механізмів. Роль міогенного фактора полягає в тому, що підвищення артеріального тиску викликає скорочення м'язового шару судин і, навпаки, зниження тиску крові викликає розслаблення м'язових волокон і розширення просвіту судин (ефект Остроумова-Бейліса). Міогенний механізм може реалізуватися при коливаннях систолічного тиску в діапазоні від 60-70 до 170-180 мм рт. ст. При зниженні його до 50 мм рт. ст., як і при значному підвищенні (понад 180 мм рт. ст.), з’являється пасивна залежність: тиск - мозковий кровотік, тобто виникає зрив реакції авторегуляції мозкового кровообігу.
Які ж механізми захищають головний мозок від надлишкової перфузії? Виявляється, що їх забезпечують внутрішні сонні та хребетні артерії. Вони не тільки регулюють об’єм надходження крові в мозкові судини, але й забезпечують постійність її притоку, незалежно від змін рівня загального артеріального тиску. Міогенний механізм авторегуляції включається миттєво, але він недовготривалий - від однієї секунди до двох хвилин. Потім він пригнічується змінами метаболізму.
Метаболічний механізм авторегуляції передбачає тісний взаємозв’язок кровопостачання мозку з його метаболізмом. Цю функцію забезпечують піальні артерії, які широко розгалужуються на поверхні мозку.
Однак ні міогенний, ні метаболічний механізми окремо не можуть пояснити складних процесів регуляції тонусу мозкових судин і забезпечити підтримку мозкового кровотоку на постійному рівні. Мабуть, механізми авторегуляції здійснюються за рахунок взаємодії двох факторів: міогенного рефлексу судинної стінки у відповідь на зміни перфузійного тиску та дії метаболітів мозкової тканини, таких як О2 і СО2
У регуляції мозкового кровотоку бере участь і неврогенний механізм, але значення його остаточно не вивчено. Вважають, що цей механізм забезпечується в основному судинними нервами.
Авторегуляція мозкового кровообігу - легко вразливий механізм, який може порушуватися при гіпоксії, гіперкапнії, різкому підвищенні або зниженні артеріального тиску. Зрив реакції авторегуляції - це стан, при якому тканинний мозковий кровотік пасивно залежить від системного артеріального тиску. Це може супроводжуватися синдромами “надлишкової перфузії” (luxury perfusion syndrome) та “реактивної гіперемії”.
ПОЧАТКОВІ ПРОЯВИ НЕДОСТАТНОСТІ КРОВОПОСТАЧАННЯ ГОЛОВНОГО МОЗКУ
Початкові прояви недостатності кровопостачання мозку - це ранні компенсовані дисциркуляційні енцефалопатії, які не супроводжуються органічною неврологічною симптоматикою і є проявом загальної судинної патології.
Початкові прояви недостатності кровопостачання мозку (ППНКМ) виділені у самостійну форму цереброваскулярної патології у рамках існуючої в Україні класифікації судинних захворювань нервової системи. Це має принципове значення, оскільки своєчасно встановлений діагноз забезпечує більш високу ефективність лікувальних і профілактичних заходів.
ЕТІОЛОГІЯ. Початкові прояви недостатності кровопостачання мозку розвиваються на тлі системних судинних захворювань:
церебрального атеросклерозу,
артеріальної гіпертонії,
вегетативно-судинної дистонії.
ПАТОГЕНЕЗ. Підвищена реактивність судинної системи, неадекватні гемодинамічні реакції, дисфункція надсегментарних центрів гіпоталамічної зони та довгастого мозку маніфестує вегетативно-судинними пароксизмами, астенією та іншими неврологічними порушеннями регіонального та загального характеру.
У патогенезі ППНКМ значну роль відіграють наступні механізми:
а) зміни кардіогемодинаміки,
б) порушення серцевої діяльності,
в) наявність тісних цереброкардіальних взаємозв’язків,
г) дистонічні зміни судин головного мозку,
д) ангіопарез зі сповільненням кровотоку,
е) порушенням венозного відтоку,
є) патологія магістральних артерій голови
- стеноз внутрішніх сонних,
- стеноз хребетних артерій,
- стенози судин вілізієвого кола,
ж) порушення реологічних властивостей крові та мікроциркуляції,
з) порушення нейронального метаболізму,
и) порушення функціонального стану головного мозку.
КЛІНІКА. Виділяють три варіанти клінічного перебігу ППНКМ:
а) доклінічний,
б) клінічний,
в) пароксизмальний.
Доклінічний (безсимптомний) варіант перебігу характеризується ознаками вегетативно-судинної дистонії:
1. акроціанозом,
2. акрогіпергідрозом,
3. стійким червоним дермографізмом,
4. блідістю або почервонінням шкіри,
5. тремтінням пальців рук, повік,
6. пожвавленням сухожилкових рефлексів,
7. нестабільністю артеріального тиску.
Скарги з'являються лише при фізичних та емоційних навантаженнях, а ознаки недостатності мозкового кровопостачання діагностується лише при функціональних пробах:
1. зміни біоелектричної активності головного мозку, гіперсинхронний і десинхронний типи ЕЕГ;
2. на реоенцефалограмах - підвищення або зниження тонусу судинної стінки, лабільність пульсових хвиль, міжпівкульну асиметрію, утруднення венозного відтоку;
3. на ЕКГ - синусова аритмія, порушення фази деполяризиції, зміщення сегмента ST і зубця Т;
4. зміни біохімічних показників характеризуються збільшенням вмісту холестерину, тригліцеридів, бета-ліпопротеїдів.
Клінічний (перманентний) варіант перебігу ППНКМ проявляється суб’єктивними ознаками недостатності кровопостачання мозку. Найчастіше хворі скаржаться на:
1. зниження розумової працездатності,
2. головний біль,
3. запаморочення,
4. шум у голові,
5. розлади пам’яті.
Підставою для встановлення діагнозу може бути тільки поєднання названих двох або більше суб’єктивних симптомів, які відносно довго існують і часто повторюються (не рідше одного разу на тиждень протягом останніх 3-х місяців). Характерне посилення цих скарг під час розумового напруження, особливо в умовах гіпоксії, перевтоми, поганого сну. Після відпочинку стан хворого покращується або повністю нормалізується. Вогнищевої неврологічної симптоматики у таких хворих не спостерігають, але можуть виявлятися:
- субкортикальні рефлекси,
- асиметрія черевних рефлексів,
- пожвавлення сухожилкових та периостальних рефлексів.
У хворих знаходять ознаки загального судинного захворювання:
- коронарокардіосклероз,
- гіпертрофію лівого шлуночка серця,
- зміни судин очного дна (ангіопатія),
- симптоми атеросклеротичного ураження інших ділянок.
Діагноз підтверджується також змінами біопотенціалів мозку, реоенцефалографічних (РЕГ), доплерографічних, біохімічних показників.
Пароксизмальний перебіг ППНКМ зустрічається переважно у хворих з вегетативно-судинною дистонією, артеріальною гіпертензією і значно рідше - при атеросклерозі. Домінуючими в клінічній картині є вегетативно-судинні пароксизми типу:
- цефалгічних,
- вестибулярних,
- синкопальних,
- симпатико-адреналових,
- вагоінсулярних,
- змішаних.
Пароксизмальні розлади в більшості випадків є проявом дисфункції надсегментарного рівня вегетативної нервової системи, зокрема, утворів лімбіко-ретикулярного комплексу.
ДІАГНОЗ ППНКМ встановлюють на підставі скарг, клінічної картини захворювання, а також за допомогою електрофізіологічних і лабораторних методів дослідження. Має значення виявлення симптомів загального судинного захворювання: атеросклерозу, артеріальної гіпертензії, вегетативно-судинної дистонії.
ЛІКУВАННЯ хворих з ППНКМ має особливе значення, оскільки неврологічні розлади на цій стадії захворювання зворотні, а тому своєчасна терапія є одночасно і профілактикою гострих порушень мозкового кровообігу. Розроблена система поетапного лікування хворих: поліклініка - стаціонар - курорт - поліклініка, яка включає диспансерний нагляд. На кожному з етапів застосовуються сучасні схеми обстеження та лікування хворих з урахуванням варіанту клінічного перебігу та загального судинного захворювання.
Важливими є наступні аспекти лікування:
- Нормалізація режиму праці та відпочинку:
а) необхідно усунути різні психоемоційні фактори,
б) забезпечити повноцінний сон і відпочинок,
- Дотримання режиму харчування:
а) необхідно уникати їжі, багатої тваринними жирами, холестерином, сіллю;
б) споживати молочно-рослинну їжу, рибу, відварене м’ясо.
- Рекомендоване санаторно-курортне лікування, ЛФК, масаж.
- Медикаментозне лікування спрямовують на терапію основного судинного захворювання. Показані наступні групи препаратів:
1. Седативні - бром, ново-пасіт, саносан, персен, валеріана.
2. Малі транквілізатори - феназепам, гідазепам, трансен.
3. Тонізуючі засоби при пониженому артеріальному тиску - кофеїн, пантокрин, настоянка китайського лимонника, настоянка женьшеню
4. Вазоактивні препарати, що покращують мозковий кровообіг - кавінтон, інстенон.
5. Ноотропні засоби, які покращують нейрональний метаболізм - ноотропіл, пірацетам, церебролізин, актовегін, енцефабол тощо.
6. Антиагреганти при гемореологічних порушеннях - курантил, трентал, агапурин, серміон.
7. Спазмолітики та гіпотензивні препарати - дибазол, папаверин, еуфілін, платифілін, клофелін.
8. Антагоністи кальцію - ніфедипін, ділтіазем.
9. Ліпотропні засоби - метіонін, ліпостабіл, цетаміфен, поліспонін, клофібрат, місклерон, лінетол, ловастатин, зокор.
Якщо у хворого є виражені симптоми гіпертонічної хвороби, ІХС, атеросклерозу, цукрового діабету, то це зумовлює призначення додаткових медикаментозних комбінацій, згідно рекомендацій кардіолога, ендокринолога та ін.
З фізіотерапевтичних методів лікування слід призначити:
1. електрофорез спазмолітиків чи аналгетиків на комірцеву зону,
2. масаж шийного відділу хребта,
3. рефлексотерапію,
4. електросон.
ПРОФІЛАКТИКА. Систему заходів первинної профілактики спрямована на запобігання розвитку судинного захворювання головного мозку: усунення факторів ризику, поліпшення умов праці, побуту, здоровий спосіб життя. Вторинна профілактика передбачає раннє виявлення, облік хворих з ППНКМ, своєчасне їх лікування з метою попередження розвитку цереброваскулярної патології головного мозку. Лікування хворих можливо проводити в умовах денних стаціонарів з застосуванням немедикаментозних методів терапії. Велику роль у профілактиці ППНКМ відіграють диспансеризація хворих, планові неврологічні профогляди.
|
Здоров'я |
Здоров'я - це фiзичне, духовне i соцiальне благополуччя, а не лише вiдсутнiсть хвороб або фiзичних вад
|
Нервная система является мишенью токсичных веществ |
Биологические эффекты токсических соединений
http://toxicology.narod.ru/book.html
Американским институтом гигиены подсчитано, что из 588 токсичных соединений 28% главным образом
действуют на нервную систему. Эта чувствительность возникает из-за сложного строения
нервной системы и ее первостепенной функции для всего организма. Повышенная
чувствительность в период развития плода отражает продолжительный период, требующийся
для сортирования клеток, запланированного истощения и создания соответствующего
взаимодействия. К тому же, так как клетки нервной системы существенным образом не
размножаются после рождения, повреждение, приводящее к гибели клетки или потери
функции, является кумулятивным и может вызвать появление симптомов через много лет
после незначительного воздействия. Открытие веществ, которые могут вызывать появление
симптомов Паркинсонизма, привели к размышлению о том, что хроническое воздействие
веществ из окружающей среды является причиной увеличения встречаемости этих симптомов и
других заболеваний нервной системы. На сегодняшний день произведена оценка влияния
70000 коммерческих химических соединений на нервную систему.
Центральная нервная система (головной и спиной мозг) управляют периферической
нервной системой и управляет ее функциями. Периферическая нервная система является
запутанной сетью, содержащей в себе большое разнообразие потенциальных сайтов для
воздействия токсичных веществ. Центральная нервная система защищается от заурядных
воздействий с помощью специализированных, тесно соединенных эндотелиальных клеток,
выстилающих кровяные капилляры. Сетчатка глаза и некоторые компоненты периферической
нервной системы также защищены. Этот барьер более эффективен для заряженных соединений
и менее эффективен для липофильных веществ. При рождении этот барьер формируется не
полностью, и у недоношенных детей может быть разрушен с помощью веществ, которые
позднее проникнуть не смогут.
Нейроны выполняют основные функции нервной системы. Найдено большое
разнообразие нейронов, которые выполняют специализированные функции. Основные
биосинтетические функции клетки, такие как синтез белков, происходят в теле клетки.
Передаваемая информация принимается дендритами. Когда эта информация достигает
достаточного уровня, она передается по- средством электрического импульса по аксону.
Аксоны формируют разветвления на конце, которые соединяются с другими нейронами или
мышечными клетками, которые принимают этот импульс.
Нейроны обычно имеют избыток отрицательного заряда на внутренней стороне. Этот
заряд нейрона поддерживается благодаря ионным насосам, для работы которых необходима
энергия (АТФ). Самым важным насосом является натрий-калиевый АТФ-зависимый насос,
который поддерживает концентрацию калия снаружи клетки приблизительно в 20 раз выше,
чем внутри, а концентрация натрия внутри составляет только одну десятую концентрации
снаружи.
Концентрация хлорида снаружи выше, чем внутри. Из-за дифференцированного
заряда возникает электрический потенциал, равный приблизительно 70 мВ. Так как
разноименные заряды разделены маленьким расстоянием, то электрическое поле достаточно
велико, порядка 100 кВ/см. Особенностью аксона является высокая частота натриевых
канальцев в плазматической мембране. Конформация этих белков (канальцев) зависит от
электрического поля. При обычном потенциале они находятся в закрытом состоянии и не
дают ионам натрия входить и выходить из клетки. Однако когда вольтаж возрастает до
критического уровня (~30 мВ), обеспечивается движение катионов через каналец, белок
которого находится в открытой конформации. Когда в клетку поступает достаточная
концентрация натрия, полярность в данном натриевом канальце изменяется на
противоположную. Каналец закрывается и остается короткое время в инактивированном
состоянии. Тем временем, изменившееся напряжение открывает калиевый каналец,
позволяющий ионам калия выходить из клетки, таким образом, помогая восстанавливать
первоначальный потенциал, а затем он закрывается. В пределах короткого промежутка
времени, миллисекунды или около того, каналец восстанавливает способность передавать
потенциал действия. Это означает, что аксон способен передавать тысячу импульсов в
секунду. Абсолютное количество ионов, переносимых во внутрь и наружу, мало по
сравнению с общим количеством в клетке.
Аксоны очень разнообразны по длине: они могут быть короткими (менее 1 мм) или
очень длинными (более 1 м). Когда потенциал достигает разветвления на конце аксона,
импульс может перейти на другой нейрон или на мышечные клетки посредством синапса. Эта
передача происходит с использованием ионных канальцев, конформация которых зависит от
лиганда. Канальцы являются рецепторами для маленьких молекул – нейропереносчиков.
Связывание лиганда заставляет их перейти от закрытого в открытое состояние.
Активированные нейропередатчиками ионные канальцы в синапсах в открытом состоянии
позволяют перемещаться ионам, тем самым, изменяя потенциал мембраны.
Хорошо изученный вид синапса, когда он выполняет роль нейромышечного
соединения, используя для этого ацетилхолин как нейропередатчик. В соединении на
плазматической мембране (постсинаптическом терминале) мышечных клеток найдено огромное
количество ацетилхолиновых рецепторов, расположенных напротив пресинаптического
терминала аксона. Когда потенциал достигает конца аксона, открываются потенциал-
зависимые кальциевые канальцы на плазматической мембране, позволяя ионам кальция
устремляться в цитоплазму. Концентрация кальция снаружи клетки 1-2 мМ, а в
цитоплазме 0,1 мкМ. Ионы кальция индуцируют миграцию маленьких цитоплазматических
пузырьков, каждый из которых содержит порядка 10 тыс. молекул ацетилхолина, к
пресинаптической мембране. Молекулы ацетилхолина, высвободившись из пузырька, быстро
диффундируют в постсинаптическую область и в течение 0,1 мсек активируют рецепторы.
Ацетилхолиновые рецепторы быстро открываются (1 млсек), способствуя движению катионов
(особенно натрия), которые деполяризуют постсинаптическую мембрану и затем закрываются.
еполяризация открывает натриевые канальцы, распространяющие потенциал, который
деполяризует целую плазматическую мембрану мышечной клетки. Это открывает кальциевые
канальцы в плазматической мембране, а затем в саркоплазматической сети. Затем ионы
кальция вызывают сокращение мускулатуры.
Эта система предназначена не только для превращения сигнала из нейрона в
мышечную активность, но также для предотвращения сверхактивности. Ацетилхолин,
производимый потенциалом нейрона, обычно не вызывает продолжительную стимуляцию
мышечной ткани, так как он быстро удаляется из синаптической трещины. Однако нейроны
имеют специализированные транспортеры, предназначенные для возращения освобожденных
нейропередатчиков, так как большинство из них могут быть возвращены в пузырьки и снова
участвовать в цикле. Этот процесс может иметь затруднения, когда в нейрон может
попадать токсикант, близкий по структуре с нейропередатчиком, что впоследствие может
привести к нарушению нейрона. В случае ацетилхолина, нейромышечное соединение также
содержит ацетилхолинэстеразу, которая гидролизует сложный эфир, образуя ацетат и холин.
Функцию нейромедиаторов выполняют многие маленькие молекулы, включая аминокислоты,
пептиды и другие разнообразные соединения. Нейропередатчик связывается с ионным
канальцем в постсинаптической мембране, тем самым, обеспечивая движение
ионов.
Ацетилхолиновые рецепторы также найдены в синапсе между нейронами и центральной
не рвной системой. Как уже было сказано ранее, ацетилхолиновым рецептором в
нейромышечном соединении является катионовый каналец, который обеспечивает
деполяризацию мембраны в открытом состоянии. Это приводит к открыванию натриевых
канальцев, которые распространяют деполяризацию. Катионовые канальцы, которые
связываются с другими нейропередатчиками, такими как серотонин или глутамат, обладают
такой же функцией. Но некоторые лиганд-зависимые канальцы специфичны для перемещения
хлорид-ионов. Когда они открыты, хлорид-ионы заходят в клетку в результате градиента
концентрации и таким образом увеличивают поляризацию. Если открыто несколько
катионовых канальцев, но их недостаточно для достижения порога, потенциал не будет
перемещаться. Хлоридные канальцы являются ингибиторами, и если эти канальцы будут
блокированы стрихнином, то могут возникнуть конвульсии и смерть.
Рецепторы нейропередатчиков обычно не функционируют как отдельная молекула
белка. Они являются специфичными мультисубъединичными комплексами, чаще всего из
неодинаковых мономеров. Более того, каждый вид субъединиц может существовать в
нескольких формах, образованных отличающимися генами или в результате альтернативного
сплайсинга. Показательным примером является ацетилхолиновый рецептор. Рецепторы,
располагающиеся в постсинаптической мембране нейромышечншго соединения, являются
чувствительными к никотину, поэтому они известны как никотиновый субтип. Другой вид
ацетилхолинового рецептора является намного более чувствительным к искусственному
лиганду, мускариновой кислоте, поэтому он известен как мускариновый субтип. Такое
разнообразие помогает объяснить различающуюся чувствительность рецепторов к токсичным
агентам. Например, яд курраре инактивирует никотиновые рецепторы, в то время как
атропин инактивирует мускариновые рецепторы.
Токсины, влияющие на возбуждение.
Глутаминовая кислота является важнейшим передатчиком возбуждения в нервной
системе. Некоторые субтипы глутаминовых канальцев обнаруживались в экспериментах с
искусственными аналогами глутаминовой кислоты. Около 30 лет назад было обнаружено, что
введение глутаминовой кислоты или некоторых ее аналогов новорожденным крысам может
привести к смерти некоторых нейронов. Последующие исследования показали, что когда эти
нейропередатчики были введены в мозг, близлежайшие нейроны погибли, хотя аксонам,
берущим начало из клеток, находящихся снаружи этого окружения, не был причинен вред.
Эта работа породила идею о том, что высокие уровни стимуляторов возбуждения могут быть
вредоносными. Эти исследования привели также к размышлению о том, что хроническое
воздействие агентов окружающей среды, аналогов нейропереносчиков, может приводить к
заболеваниям, связанным с разрушением нервной системы, таким как болезнь Паркинсона и
болезнь Альцгеймера.
Нейролатеризм, известный с давних времен и характеризующийся частичным
параличем, является результатом воздействия токсинов возбуждения. Эта болезнь
обнаружена по всему миру, включая Европу, но сейчас в большинстве случаев она
встречается в очень бедных странах, в частности в Индии, Бангладеш и Эфиопии. Причина
заболевания заключается в горохе из бобовых Lathyrus savita. Это выносливое,
дикорастущее растение, буйно растущее независимо от погодных условий. Их зерна содержат
(порядка 0,5% от веса) необычную аминокислоту β-оксалиламиноаланин, которая
является потенциальным лигандом для АМРА субтипа глутаминового рецептора. Побеги,
которые содержат такой же уровень аминокислоты, также употребляются в пищу. После
употребления порядка 100 г/день зерен в течение нескольких лет, у некоторых людей
обнаруживаются ранние симптомы латиризма. Последующее употребление приводит к
необратимой слабости в ногах с болями и судоргами, а так же с последующими трудностями
при хождении. Продолжительное употребление в пищу приводит к смерти, но механизм этого
не известен.
Другим аналогом нейропереносчика, содержащимся в пищевых продуктах и
разрушающим нервную систему, является домоиковая кислота. Большие дозы этого вещества,
введенные крысам или обезьянам, вызывают апоплексический удар. У людей это вещество в
низких дозах вызывает диарею и потерю памяти. Домоиковая кислота аккумулируется в
ракообразных, которые питаются диатомовыми водорослями, синтезирующими это вещество во
время цветения. Поэтому перед употреблением в пищу ракообразные проходят тестирование
на содержание домоиковой кислоты. Это является предупредительной мерой. Такими
анализами занимается аналитическая химия, но это достаточно сложная задача, так как
существует одиннадцать изомеров этого соединения. Недавно для анализа стали применять
биохимические методы с использование клонированных рецепторов. Это позволило определять
активность образца без определения отдельных изомеров.
Многие высокотоксичные вещества, вызывающие невропатологии у людей,
синтезируются водорослями и могут аккумулироваться в рыбах и моллюсках. Некоторые из
них подавляют возбуждение в результате связывания с ионными канальцами аксонов, которые
обеспечивают передачу электрических импульсов и их инактивацию.
Однако некоторые из таких веществ могут использоваться в фармакологии, вызывая
гиперполяризацию и ингибируя передачу электрических импульсов. Бензодиазопины
являются популярными транквилизаторами, подавляющими беспокойство. Они связываются с
GABA рецепторами, хлоридными канальцами и увеличивают ионный поток, таким образом,
увеличивая натуральное ингибирование активности. Эти соединения являются эффективными,
имеют высокий терапевтический индекс и не вызывают привыкания. Однако некоторые
вещества в этом классе имеют высокую гипнотическую активность и могут вызывать
кратковременную потерю памяти. Одним из таких веществ является флунитразепам, который
не одобрен в США к использованию по этой причине.
Тяжелые металлы. Ртуть попадает в окружающую среду по нескольким
механизмам. Существенное количество попадает из минералов. Такое же количество (порядка
5 млрд г в год) поступает в результате горения ископаемого топлива, которое содержит
ртуть в концентрации 1ppm.
Ионы ртути могут метилироваться микроорганизмами и накапливаться в липидах.
Недавно внимание заострилось на содержании ртути в организме человека. Ртуть может
воздействовать в виде ионной и метилированной формы, а также в виде паров. Соли ртути
являются растворимыми, поэтому они чаще всего воздействуют на почки. Вдыхание паров
ртути вызывает воспаление легких. Ранние симптомы включают: усталость, уменьшение
концентрации внимания, потеря аппетита и тахикардия. Сильное воздействие может
приводить к спазмам, потери памяти, повышенной возбудимости, депрессии и галлюцинациям.
Метилированная ртуть накапливается в коре головного мозга. У плода метилированная форма
ртути накапливается в 20 раз интенсивнее, чем ионы ртути, что было показано
воздействием ртутью на беременных животных. К тому же концентрация ртути у плода в два
раза выше, чем у матери, а ртуть нарушает функции мозга у новорожденных. Воздействие
ртути в зрелом возрасте приводит к целому спектру симптомов, включая потерю
чувствительности, слуха и зрения, а в некоторых случаях даже к смерти.
Воздействие ртути на человека является вездесущим. Горение и добыча ископаемых
приводит к выбросам ртути в воздух. Некоторые люди получают высокую концентрацию через
краску (особенно дети) или пищу, приготовленную в керамической посуде, покрытой
глазурью, которая содержит ртуть.
У старых людей порядка 95% ртути в организме сосредоточено в костях, где в
течение жизни накапливается 200-500 мг ртути. Основная часть находится в красных
кровяных тельцах, что укорачивает их жизнь. Почки также накапливают ртуть, в результате
чего разрушаются проксимальные трубочки, что приводит к фиброзу. Уменьшение выделения
уриковой кислоты является результатом ослабления функций почек. Уриковая кислота
кристаллизуется и вызывает подагру. Ртуть также может приводить к нарушению
репродуктивной функции, включая стерилизацию, а также может вызывать смерть
новорожденных.
Нервная система является наиболее серьезной мишенью воздействия ртути. Сильное
воздействие приводит к разрушению мозга (энцефалопатии), характеризующееся
раздражительностью, вялостью, потерей аппетита, атаксией и даже эпилепсией. Наиболее
чувствительными являются дети. Исследования показали линейное уменьшение коэффициента
IQ от содержания ртути в крови в диапазоне 0,05-0,35 мкг/мл.
Токсины микроорганизмов. Люди подвергаются воздействию огромного
количества токсинов, вырабатываемых бактериями, которые специфично воздействуют на
разнообразные ткани. Токсины холеры, столбняка, дифтерии и ботулизма имеют схожие
механизмы воздействия. Они все синтезируются как одинарные полипептидные цепи, которые
способны формировать димеры, связанные дисульфидными мостиками. Тяжелая цепь в димере
отвечает за тканеспецифичность и за проникновение токсина в клетку. Внутри клетки
дисульфидные мостики разрушаются, после чего легкая цепь становится активированной.
Легкие белковые цепи у столбняка и ботулизма являются цинк-зависимыми. Они приводят к
нарушению секреции нейропереносчиков, которые обеспечивают взаимодействие с
плазматической мембраной в синапсе. В случае ботулизма отсутствие секреции
нейропереносчиков приводит к частичной парализации конечностей, так как токсин
действует на спинной мозг. Для сравнения, при столбняке возникает спастическая
парализация. Известно семь изоформ токсина ботулизма, которые различаются по
протеолитической специфичности. Однако три изоформы взаимодействуют с одним и тем же
белком, но разрезают его в разных местах. Видовые различия в чувствительности к
ботулизму (человек и мышь в 1000 раз более чувствительны, чем крыса) определяются
аминокислотными последовательностями в белках.
Яды. Хищники должны обладать методами поимки и обездвиживания своих
жертв. Многие используют для этой цели яды. Змеи вводят своим жертвам различные
деградирующие ферменты, включая фосфолипазы, протеазы и нуклеазы. Наиболее
эффективными обездвиживающими жертву компонентами являются небольшие белковые токсины
(порядка 7 кДа), которые связывают и инактивируют ацетилхолиновые рецепторы в
нейромышечных соединениях. Соединения этого класса имеют очень высокое сродство к
рецептору в диапазоне 0,01-1 нМ.
Вместо ингибирования ацетилхолинового рецептора, яд африканской древесной змеи
содержит пептидный компонент, который связывает и инактивирует ацетилхолинэстеразу.
Этот яд также содержит токсин, инактивирующий ворота калиевых канальцев, которые
деполяризуют аксон между импульсами.
Яды, которые воздействуют на ионные канальцы, часто состоят из смеси
компонентов, одни из которых блокируют определенные канальцы в открытом состоянии, а
другие - в закрытом. Яды актиний и пчел содержат пептиды, которые действуют на калиевые
канальцы, а так же пептиды, которые действуют на натриевые канальцы. Морские улитки
обездвиживают своих жертв (включая рыб по размерам больших, чем они сами) концентратами
пептидов, которые содержат компоненты действующие на калиевые, натриевые и кальциевые
канальцы, а так же другие пептидные ингредиенты, являющиеся нейротоксинами. Многие
токсины ядов достаточно специфичны и поэтому нашли широкое применение для использования
в экспериментах по изучению активностей ионных канальцев нервной системы млекопитающих,
включая человека.
Инсектициды. При производстве достаточного количества пищи для
растущего населения мы стали зависимыми от разнообразных инсектицидов. Они, как
правило, воздействуют на нервную систему и, следовательно, их действие протекает
быстро. Главной целью инсектицидов являются хлоридные канальцы (γ-
аминобутариковая кислота, циклодиены), натриевые канальцы (ДДТ) и ацетилхолинэстераза
(органофосфаты). Широкое применение этих веществ привело к развитию устойчивости
насекомых. Одиночные точечные мутации, повышающие устойчивость к циклодиенам, найдены у
некоторых видов (тараканы, москиты, комнатные мухи, плодовые мушки, алейродиды, хрущак
каштановый). Точечные мутации, повышающие устойчивость натриевых канальцев к ДДТ,
найдены у шести видов (комнатные мухи, москиты, тараканы, тля персиковая, моль
капустная, табачная листовертка-почкоед). Одна из нескольких дополнительных точечных
мутаций может также привести к суперустойчивости.
К счастью для нас, наша нервная система является нечувствительной к действию
таких инсектицидов как циклодиены и ДДТ. Однако мы очень чувствительны к
органофосфатам, которые первоначально разрабатывались как отравляющие вещества для
ведения войны. Органофосфаты синтезируются в виде тиоформы (R3P=S), которая является
относительно стабильной. Когда это соединение попадает в насекомое (или в человека),
оно переходит в оксоформу (R3P=O), которая быстро взаимодействует с
ацетилхолинэстеразой. Эти соединения вызывают смерть не только при вдыхании, но и при
взаимодействии с кожным покровом. Изучение биохимии ацетилхолинэстеразы демонстрирует,
что активные сайты остатков серина участвуют в гидролизе ацетилхолина, образуя
интермедиат О-ацетилсерин, который быстро гидролизуется. Таким образом, органофосфаты
инактивируют ферменты, тем самым, замедляя гидролиз.
Злоупотребление наркотиками. Ядра accumbens были открыты как своего
рода центры удовольствия в мозге, где рост уровня допамина-нейропереносчика
воспринимался как удовольствие (эйфория, блаженство). Множество признаков указывает на
злоупотребление наркотиками (включая никотин), как на стимуляторы уровня допамина в
организме, который (уровень) отвечает за чувства удовольствия, вызываемые наркотиками.
Экспериментальные животные будут добровольно сами принимать эти наркотики, что говорит
о взникновении привыкания к наркотическим препаратам. У людей и животных привыкание или
уменьшение чувствительности к таким агентам происходит так, что требуются для получения
соизмеримого удовольствия большие дозы. Дозы наркотика могут стократно возрастать, что
выходит далеко за пределы того, что изначально являлось летальным воздействием.
Окончательное прекращение потребления наркотиков впоследствие вызывает дисфорию (в
противоположность эйфории), так как тело реадаптируется к нехватке экзогенных агентов.
Наркоманы в это время идут на то, чтобы продолжать принятие наркотиков в еще больших
дозах. Реабилитация наркоманов – это долгий процесс, обычно длящийся долгие годы.
Наркотическая зависимость была сравнима в масштабах с хроническими заболеваниями,
такими, как: диабет, астма и повышенное кровяное давление. Многие исследования в
области злоупотребления наркотиками направлены на понимание молекулярной основы
действия наркотика, толерантности организма и реакцию отказа от наркотиков на их
воздействие. Один из подходов к пониманию действия наркотиков был направлен на поиск их
рецепторов. Это первый шаг в понимании путей сигнальной трансдукции. Последние работы
указывают на важность серотониновых путей в возбуждении при наркотическом воздействии,
а также на важность глутаматовых путей, особенно рецепторов NMDA, в развитии тяги к
большему количеству наркотиков.
Фармакологические свойства опиоидов известны с древних времен. Выделение
наиболее активного компонента - морфина было впервые описано в 1803. Героин
(диацетилморфин), который имеет более высокую скорость проникновения в мозг, был
синтезирован в 1874. Морфин и его активные природные аналоги, такие как кодеин,
вызывают не только эйфорию, но также являются хорошими анальгетиками и высоко
эффективны в борьбе с диареей. Много усилий было положено на попытки сделать
производные этих соединений, которые вызывают только обезболивание без эйфории, но до
сих пор только с ограниченным успехом. Однако был разработан эффективный антагонист
(для лечения передозировок), такой же долгоживущий, хотя гораздо менее
эффективный, производное (метадон), которое полезно в реабилитации. Несмотря на то, что
он не вызывает эйфории (преимущество в лечении), он достаточно силен, чтобы избежать
синдромов ломки. Допустимо прописывать его для раковых больных в целях облегчения
боли, что также устраняет потребность в марихуане.
Изучение рецепторов привело к выявлению трех основных подтипов рецепторов
морфия, которыми оказались G-белки (Gi). Они сдерживают образование аденил-циклазы в
целевых нейронах, таким образом, увеличивая проводимость каналов калия, уменьшая
проводимость каналов кальция и вызывая гиперполяризованное состояние. Как именно это
приводит к обезболиванию неясно; пациенты, находящиеся на лечении для избавления от
наркотической зависимости, говорят, что боль не ушла и даже не уменьшилась, они просто
больше не воспринимают ее как нечто, вызывающее отвращение. Эндогенные лиганды для
рецепторов, два из которых являются пентопептидами, выведенными из предшественников,
были обнаружены и названы эндорфинами (эндогенный морфин).
Амфетамин был впервые синтезирован в 1887. Он относится к фармокологически
активным компонентам некоторых растений Восточной Африки и Китая и известен своими
целебными свойствами. Раньше этот препарат прописывался в таблетках для лечения
нарколепсии (внезапный сон) в 1935 и был отдан военным в 1940-ых для поддержания боевой
готовности. В 50-ые и 60-ые годы он принимался студентами и дальнобойщиками для
поддержания активности без сна и отдыха. Препарат медленно поглощается при оральном
принятии, но когда вводится внутривенно или (особенно метамфетамин) ингаляцией, то
вызывает чувство удовольствия, ведущее к злоупотреблению «скоростными чудачествами».
Агенты класса амфетамина перемещаются допаминергическими нейронами, препятствуя
реабсорбции допамина и ускоряя выбрасывание допамина из внутриклеточных пазух. Так как
действие препарата проходит быстро, то лица, злоупотребляющие наркотиками, могут
принимать дозы с двух часовыми интервалами в течение нескольких дней, а
потом «ломаются» (спят в течение долгого периода). Привыкание возникает быстро, требуя
увеличения доз, а последующее воздержание характеризуется вялостью, депрессией и, в
основном, неприятными чувствами. Продолжительное употребление может вызвать
галлюцинации и психозы, напоминающие параноидную шизофрению. Амфетамины запрещены для
занятий спортом, потому что они улучшают исполнение. Но его производные все еще
используются для борьбы с потерей веса для улучшения аппетита (включая
фенолпропаноламин в Дексатриме и в Риталине) и для лечения гиперактивного дефицита
внимания у детей.
Кокаин впервые был обнаружен в кустарнике Южной Америки. В период
завоевания этого континента, испанцы впервые наложили запрет на привычку местных
жителей жевать листья этого растения, но затем заметили, что рабы работали усерднее и
дольше, когда им позволили жевать листья. Кокаин был добавлен в Кока-колу, производимую
в 1886 г., пока он не был устранен в 1906 г. Позднее напитки с кокаином продавались в
качестве альтернативы алкоголю как часть движения за трезвость. В 1914 г. федеральное
правительство США установило запрет на продажу кокаина и опиума, как составляющих
лекарственных препаратов, в аптеках. Такая практика ни к чему хорошему не привела. По
оценкам экспертов в США насчитывается около полмиллиона наркоманов. Для достижения
желаемого эффекта важен способ введения, обычно это ингаляции или внутривенные
инъекции. Эйфория от кокаина длится в течение получаса, гораздо меньшее время, чем от
амфетамина, а с увеличе нием дозы ведет к агрессии. Так же, как и с амфетамином,
основа достижения удовольствия заключается в уменьшении реабсорбции допамина через
дофаминергические нейроны. Недавно также было сообщено о роли серотонина в развитии
наркотического эффекта. В больших концентрациях, однако, кокаин может также подавлять
определенный рецепторы нейропереносчиков и даже блокировать аксонные натриевые каналы.
Это способность была задействована в разработке производных, таких как прокаин и
лидокаин, которые широко используются как местные анастетики.
Один из наиболее часто употребляемых наркотиков получен из растения марихуаны.
Основным составляющим марихуаны является Δ9-тетрагидроканнабинол (ТНС):
ТНС
Поглощение достаточного количества ТНС обычно вызывает чувство эйфории, которое может
длиться несколько часов. Оно может сопровождаться беспорядочными мыслительными
процессами и психомоторными проявлениями (координация, время реакции), которые длятся
полдня, так что следует воздержаться от вождения автомобиля. Уменьшение
чувствительности к доставляющим удовольствие эффектам приходит с повторяющимися
высокими дозами за короткие интервалы времени. Однако невозможно продемонстрировать
психическую зависимость на животных или людях в соответствии с условиями обычного
употребления. Употребление сильных антагонистов показало, что могут появиться симптомы
ломки, однако такие симптомы обычно незаметны, потому что время полужизни ТНС в крови
достаточно высоко (приблизительно день).
Недавно с помощью радиоактивного лиганда рецепторы для ТНС были определены как
члены надсемества G-белков. Это привело к идентификации эндогенного лиганда, названного
анандамидом (санскрит для «блаженства»), который оказался производным арахидоновой
кислоты – компонента липидной мембраны. Любопытно, что анандамид является растворимым
липидом, он не хранится в везикуле, подобно другим нейропереносчикам. Это позволяет
предположить существование другого класса лигандов. Рецепторы ТНС обнаружены в двух
изоформах, одни – в центральной нервной системе, и другие – в клетках иммунной
системы, такие как макрофаги, потенциально обеспечивающие основу для некоторых реакций,
которые могут влиять на иммунные функции из-за употребления марихуаны. Связанный с
рецепторами ТНС уменьшает производство сАМР в нейронах, приводя к уменьшению активности
кальциевых и калиевых каналов. Как именно это приводит к возникновению удовольствия
неясно, но недавно было показано, что введение ТНС крысам приводит к высвобождению
допамина в ядрах accumbens, подобно высвобождению эндрофинов.
http://toxicology.narod.ru/book.html
Американским институтом гигиены подсчитано, что из 588 токсичных соединений 28% главным образом
действуют на нервную систему. Эта чувствительность возникает из-за сложного строения
нервной системы и ее первостепенной функции для всего организма. Повышенная
чувствительность в период развития плода отражает продолжительный период, требующийся
для сортирования клеток, запланированного истощения и создания соответствующего
взаимодействия. К тому же, так как клетки нервной системы существенным образом не
размножаются после рождения, повреждение, приводящее к гибели клетки или потери
функции, является кумулятивным и может вызвать появление симптомов через много лет
после незначительного воздействия. Открытие веществ, которые могут вызывать появление
симптомов Паркинсонизма, привели к размышлению о том, что хроническое воздействие
веществ из окружающей среды является причиной увеличения встречаемости этих симптомов и
других заболеваний нервной системы. На сегодняшний день произведена оценка влияния
70000 коммерческих химических соединений на нервную систему.
Центральная нервная система (головной и спиной мозг) управляют периферической
нервной системой и управляет ее функциями. Периферическая нервная система является
запутанной сетью, содержащей в себе большое разнообразие потенциальных сайтов для
воздействия токсичных веществ. Центральная нервная система защищается от заурядных
воздействий с помощью специализированных, тесно соединенных эндотелиальных клеток,
выстилающих кровяные капилляры. Сетчатка глаза и некоторые компоненты периферической
нервной системы также защищены. Этот барьер более эффективен для заряженных соединений
и менее эффективен для липофильных веществ. При рождении этот барьер формируется не
полностью, и у недоношенных детей может быть разрушен с помощью веществ, которые
позднее проникнуть не смогут.
Нейроны выполняют основные функции нервной системы. Найдено большое
разнообразие нейронов, которые выполняют специализированные функции. Основные
биосинтетические функции клетки, такие как синтез белков, происходят в теле клетки.
Передаваемая информация принимается дендритами. Когда эта информация достигает
достаточного уровня, она передается по- средством электрического импульса по аксону.
Аксоны формируют разветвления на конце, которые соединяются с другими нейронами или
мышечными клетками, которые принимают этот импульс.
Нейроны обычно имеют избыток отрицательного заряда на внутренней стороне. Этот
заряд нейрона поддерживается благодаря ионным насосам, для работы которых необходима
энергия (АТФ). Самым важным насосом является натрий-калиевый АТФ-зависимый насос,
который поддерживает концентрацию калия снаружи клетки приблизительно в 20 раз выше,
чем внутри, а концентрация натрия внутри составляет только одну десятую концентрации
снаружи.
Концентрация хлорида снаружи выше, чем внутри. Из-за дифференцированного
заряда возникает электрический потенциал, равный приблизительно 70 мВ. Так как
разноименные заряды разделены маленьким расстоянием, то электрическое поле достаточно
велико, порядка 100 кВ/см. Особенностью аксона является высокая частота натриевых
канальцев в плазматической мембране. Конформация этих белков (канальцев) зависит от
электрического поля. При обычном потенциале они находятся в закрытом состоянии и не
дают ионам натрия входить и выходить из клетки. Однако когда вольтаж возрастает до
критического уровня (~30 мВ), обеспечивается движение катионов через каналец, белок
которого находится в открытой конформации. Когда в клетку поступает достаточная
концентрация натрия, полярность в данном натриевом канальце изменяется на
противоположную. Каналец закрывается и остается короткое время в инактивированном
состоянии. Тем временем, изменившееся напряжение открывает калиевый каналец,
позволяющий ионам калия выходить из клетки, таким образом, помогая восстанавливать
первоначальный потенциал, а затем он закрывается. В пределах короткого промежутка
времени, миллисекунды или около того, каналец восстанавливает способность передавать
потенциал действия. Это означает, что аксон способен передавать тысячу импульсов в
секунду. Абсолютное количество ионов, переносимых во внутрь и наружу, мало по
сравнению с общим количеством в клетке.
Аксоны очень разнообразны по длине: они могут быть короткими (менее 1 мм) или
очень длинными (более 1 м). Когда потенциал достигает разветвления на конце аксона,
импульс может перейти на другой нейрон или на мышечные клетки посредством синапса. Эта
передача происходит с использованием ионных канальцев, конформация которых зависит от
лиганда. Канальцы являются рецепторами для маленьких молекул – нейропереносчиков.
Связывание лиганда заставляет их перейти от закрытого в открытое состояние.
Активированные нейропередатчиками ионные канальцы в синапсах в открытом состоянии
позволяют перемещаться ионам, тем самым, изменяя потенциал мембраны.
Хорошо изученный вид синапса, когда он выполняет роль нейромышечного
соединения, используя для этого ацетилхолин как нейропередатчик. В соединении на
плазматической мембране (постсинаптическом терминале) мышечных клеток найдено огромное
количество ацетилхолиновых рецепторов, расположенных напротив пресинаптического
терминала аксона. Когда потенциал достигает конца аксона, открываются потенциал-
зависимые кальциевые канальцы на плазматической мембране, позволяя ионам кальция
устремляться в цитоплазму. Концентрация кальция снаружи клетки 1-2 мМ, а в
цитоплазме 0,1 мкМ. Ионы кальция индуцируют миграцию маленьких цитоплазматических
пузырьков, каждый из которых содержит порядка 10 тыс. молекул ацетилхолина, к
пресинаптической мембране. Молекулы ацетилхолина, высвободившись из пузырька, быстро
диффундируют в постсинаптическую область и в течение 0,1 мсек активируют рецепторы.
Ацетилхолиновые рецепторы быстро открываются (1 млсек), способствуя движению катионов
(особенно натрия), которые деполяризуют постсинаптическую мембрану и затем закрываются.
еполяризация открывает натриевые канальцы, распространяющие потенциал, который
деполяризует целую плазматическую мембрану мышечной клетки. Это открывает кальциевые
канальцы в плазматической мембране, а затем в саркоплазматической сети. Затем ионы
кальция вызывают сокращение мускулатуры.
Эта система предназначена не только для превращения сигнала из нейрона в
мышечную активность, но также для предотвращения сверхактивности. Ацетилхолин,
производимый потенциалом нейрона, обычно не вызывает продолжительную стимуляцию
мышечной ткани, так как он быстро удаляется из синаптической трещины. Однако нейроны
имеют специализированные транспортеры, предназначенные для возращения освобожденных
нейропередатчиков, так как большинство из них могут быть возвращены в пузырьки и снова
участвовать в цикле. Этот процесс может иметь затруднения, когда в нейрон может
попадать токсикант, близкий по структуре с нейропередатчиком, что впоследствие может
привести к нарушению нейрона. В случае ацетилхолина, нейромышечное соединение также
содержит ацетилхолинэстеразу, которая гидролизует сложный эфир, образуя ацетат и холин.
Функцию нейромедиаторов выполняют многие маленькие молекулы, включая аминокислоты,
пептиды и другие разнообразные соединения. Нейропередатчик связывается с ионным
канальцем в постсинаптической мембране, тем самым, обеспечивая движение
ионов.
Ацетилхолиновые рецепторы также найдены в синапсе между нейронами и центральной
не рвной системой. Как уже было сказано ранее, ацетилхолиновым рецептором в
нейромышечном соединении является катионовый каналец, который обеспечивает
деполяризацию мембраны в открытом состоянии. Это приводит к открыванию натриевых
канальцев, которые распространяют деполяризацию. Катионовые канальцы, которые
связываются с другими нейропередатчиками, такими как серотонин или глутамат, обладают
такой же функцией. Но некоторые лиганд-зависимые канальцы специфичны для перемещения
хлорид-ионов. Когда они открыты, хлорид-ионы заходят в клетку в результате градиента
концентрации и таким образом увеличивают поляризацию. Если открыто несколько
катионовых канальцев, но их недостаточно для достижения порога, потенциал не будет
перемещаться. Хлоридные канальцы являются ингибиторами, и если эти канальцы будут
блокированы стрихнином, то могут возникнуть конвульсии и смерть.
Рецепторы нейропередатчиков обычно не функционируют как отдельная молекула
белка. Они являются специфичными мультисубъединичными комплексами, чаще всего из
неодинаковых мономеров. Более того, каждый вид субъединиц может существовать в
нескольких формах, образованных отличающимися генами или в результате альтернативного
сплайсинга. Показательным примером является ацетилхолиновый рецептор. Рецепторы,
располагающиеся в постсинаптической мембране нейромышечншго соединения, являются
чувствительными к никотину, поэтому они известны как никотиновый субтип. Другой вид
ацетилхолинового рецептора является намного более чувствительным к искусственному
лиганду, мускариновой кислоте, поэтому он известен как мускариновый субтип. Такое
разнообразие помогает объяснить различающуюся чувствительность рецепторов к токсичным
агентам. Например, яд курраре инактивирует никотиновые рецепторы, в то время как
атропин инактивирует мускариновые рецепторы.
Токсины, влияющие на возбуждение.
Глутаминовая кислота является важнейшим передатчиком возбуждения в нервной
системе. Некоторые субтипы глутаминовых канальцев обнаруживались в экспериментах с
искусственными аналогами глутаминовой кислоты. Около 30 лет назад было обнаружено, что
введение глутаминовой кислоты или некоторых ее аналогов новорожденным крысам может
привести к смерти некоторых нейронов. Последующие исследования показали, что когда эти
нейропередатчики были введены в мозг, близлежайшие нейроны погибли, хотя аксонам,
берущим начало из клеток, находящихся снаружи этого окружения, не был причинен вред.
Эта работа породила идею о том, что высокие уровни стимуляторов возбуждения могут быть
вредоносными. Эти исследования привели также к размышлению о том, что хроническое
воздействие агентов окружающей среды, аналогов нейропереносчиков, может приводить к
заболеваниям, связанным с разрушением нервной системы, таким как болезнь Паркинсона и
болезнь Альцгеймера.
Нейролатеризм, известный с давних времен и характеризующийся частичным
параличем, является результатом воздействия токсинов возбуждения. Эта болезнь
обнаружена по всему миру, включая Европу, но сейчас в большинстве случаев она
встречается в очень бедных странах, в частности в Индии, Бангладеш и Эфиопии. Причина
заболевания заключается в горохе из бобовых Lathyrus savita. Это выносливое,
дикорастущее растение, буйно растущее независимо от погодных условий. Их зерна содержат
(порядка 0,5% от веса) необычную аминокислоту β-оксалиламиноаланин, которая
является потенциальным лигандом для АМРА субтипа глутаминового рецептора. Побеги,
которые содержат такой же уровень аминокислоты, также употребляются в пищу. После
употребления порядка 100 г/день зерен в течение нескольких лет, у некоторых людей
обнаруживаются ранние симптомы латиризма. Последующее употребление приводит к
необратимой слабости в ногах с болями и судоргами, а так же с последующими трудностями
при хождении. Продолжительное употребление в пищу приводит к смерти, но механизм этого
не известен.
Другим аналогом нейропереносчика, содержащимся в пищевых продуктах и
разрушающим нервную систему, является домоиковая кислота. Большие дозы этого вещества,
введенные крысам или обезьянам, вызывают апоплексический удар. У людей это вещество в
низких дозах вызывает диарею и потерю памяти. Домоиковая кислота аккумулируется в
ракообразных, которые питаются диатомовыми водорослями, синтезирующими это вещество во
время цветения. Поэтому перед употреблением в пищу ракообразные проходят тестирование
на содержание домоиковой кислоты. Это является предупредительной мерой. Такими
анализами занимается аналитическая химия, но это достаточно сложная задача, так как
существует одиннадцать изомеров этого соединения. Недавно для анализа стали применять
биохимические методы с использование клонированных рецепторов. Это позволило определять
активность образца без определения отдельных изомеров.
Многие высокотоксичные вещества, вызывающие невропатологии у людей,
синтезируются водорослями и могут аккумулироваться в рыбах и моллюсках. Некоторые из
них подавляют возбуждение в результате связывания с ионными канальцами аксонов, которые
обеспечивают передачу электрических импульсов и их инактивацию.
Однако некоторые из таких веществ могут использоваться в фармакологии, вызывая
гиперполяризацию и ингибируя передачу электрических импульсов. Бензодиазопины
являются популярными транквилизаторами, подавляющими беспокойство. Они связываются с
GABA рецепторами, хлоридными канальцами и увеличивают ионный поток, таким образом,
увеличивая натуральное ингибирование активности. Эти соединения являются эффективными,
имеют высокий терапевтический индекс и не вызывают привыкания. Однако некоторые
вещества в этом классе имеют высокую гипнотическую активность и могут вызывать
кратковременную потерю памяти. Одним из таких веществ является флунитразепам, который
не одобрен в США к использованию по этой причине.
Тяжелые металлы. Ртуть попадает в окружающую среду по нескольким
механизмам. Существенное количество попадает из минералов. Такое же количество (порядка
5 млрд г в год) поступает в результате горения ископаемого топлива, которое содержит
ртуть в концентрации 1ppm.
Ионы ртути могут метилироваться микроорганизмами и накапливаться в липидах.
Недавно внимание заострилось на содержании ртути в организме человека. Ртуть может
воздействовать в виде ионной и метилированной формы, а также в виде паров. Соли ртути
являются растворимыми, поэтому они чаще всего воздействуют на почки. Вдыхание паров
ртути вызывает воспаление легких. Ранние симптомы включают: усталость, уменьшение
концентрации внимания, потеря аппетита и тахикардия. Сильное воздействие может
приводить к спазмам, потери памяти, повышенной возбудимости, депрессии и галлюцинациям.
Метилированная ртуть накапливается в коре головного мозга. У плода метилированная форма
ртути накапливается в 20 раз интенсивнее, чем ионы ртути, что было показано
воздействием ртутью на беременных животных. К тому же концентрация ртути у плода в два
раза выше, чем у матери, а ртуть нарушает функции мозга у новорожденных. Воздействие
ртути в зрелом возрасте приводит к целому спектру симптомов, включая потерю
чувствительности, слуха и зрения, а в некоторых случаях даже к смерти.
Воздействие ртути на человека является вездесущим. Горение и добыча ископаемых
приводит к выбросам ртути в воздух. Некоторые люди получают высокую концентрацию через
краску (особенно дети) или пищу, приготовленную в керамической посуде, покрытой
глазурью, которая содержит ртуть.
У старых людей порядка 95% ртути в организме сосредоточено в костях, где в
течение жизни накапливается 200-500 мг ртути. Основная часть находится в красных
кровяных тельцах, что укорачивает их жизнь. Почки также накапливают ртуть, в результате
чего разрушаются проксимальные трубочки, что приводит к фиброзу. Уменьшение выделения
уриковой кислоты является результатом ослабления функций почек. Уриковая кислота
кристаллизуется и вызывает подагру. Ртуть также может приводить к нарушению
репродуктивной функции, включая стерилизацию, а также может вызывать смерть
новорожденных.
Нервная система является наиболее серьезной мишенью воздействия ртути. Сильное
воздействие приводит к разрушению мозга (энцефалопатии), характеризующееся
раздражительностью, вялостью, потерей аппетита, атаксией и даже эпилепсией. Наиболее
чувствительными являются дети. Исследования показали линейное уменьшение коэффициента
IQ от содержания ртути в крови в диапазоне 0,05-0,35 мкг/мл.
Токсины микроорганизмов. Люди подвергаются воздействию огромного
количества токсинов, вырабатываемых бактериями, которые специфично воздействуют на
разнообразные ткани. Токсины холеры, столбняка, дифтерии и ботулизма имеют схожие
механизмы воздействия. Они все синтезируются как одинарные полипептидные цепи, которые
способны формировать димеры, связанные дисульфидными мостиками. Тяжелая цепь в димере
отвечает за тканеспецифичность и за проникновение токсина в клетку. Внутри клетки
дисульфидные мостики разрушаются, после чего легкая цепь становится активированной.
Легкие белковые цепи у столбняка и ботулизма являются цинк-зависимыми. Они приводят к
нарушению секреции нейропереносчиков, которые обеспечивают взаимодействие с
плазматической мембраной в синапсе. В случае ботулизма отсутствие секреции
нейропереносчиков приводит к частичной парализации конечностей, так как токсин
действует на спинной мозг. Для сравнения, при столбняке возникает спастическая
парализация. Известно семь изоформ токсина ботулизма, которые различаются по
протеолитической специфичности. Однако три изоформы взаимодействуют с одним и тем же
белком, но разрезают его в разных местах. Видовые различия в чувствительности к
ботулизму (человек и мышь в 1000 раз более чувствительны, чем крыса) определяются
аминокислотными последовательностями в белках.
Яды. Хищники должны обладать методами поимки и обездвиживания своих
жертв. Многие используют для этой цели яды. Змеи вводят своим жертвам различные
деградирующие ферменты, включая фосфолипазы, протеазы и нуклеазы. Наиболее
эффективными обездвиживающими жертву компонентами являются небольшие белковые токсины
(порядка 7 кДа), которые связывают и инактивируют ацетилхолиновые рецепторы в
нейромышечных соединениях. Соединения этого класса имеют очень высокое сродство к
рецептору в диапазоне 0,01-1 нМ.
Вместо ингибирования ацетилхолинового рецептора, яд африканской древесной змеи
содержит пептидный компонент, который связывает и инактивирует ацетилхолинэстеразу.
Этот яд также содержит токсин, инактивирующий ворота калиевых канальцев, которые
деполяризуют аксон между импульсами.
Яды, которые воздействуют на ионные канальцы, часто состоят из смеси
компонентов, одни из которых блокируют определенные канальцы в открытом состоянии, а
другие - в закрытом. Яды актиний и пчел содержат пептиды, которые действуют на калиевые
канальцы, а так же пептиды, которые действуют на натриевые канальцы. Морские улитки
обездвиживают своих жертв (включая рыб по размерам больших, чем они сами) концентратами
пептидов, которые содержат компоненты действующие на калиевые, натриевые и кальциевые
канальцы, а так же другие пептидные ингредиенты, являющиеся нейротоксинами. Многие
токсины ядов достаточно специфичны и поэтому нашли широкое применение для использования
в экспериментах по изучению активностей ионных канальцев нервной системы млекопитающих,
включая человека.
Инсектициды. При производстве достаточного количества пищи для
растущего населения мы стали зависимыми от разнообразных инсектицидов. Они, как
правило, воздействуют на нервную систему и, следовательно, их действие протекает
быстро. Главной целью инсектицидов являются хлоридные канальцы (γ-
аминобутариковая кислота, циклодиены), натриевые канальцы (ДДТ) и ацетилхолинэстераза
(органофосфаты). Широкое применение этих веществ привело к развитию устойчивости
насекомых. Одиночные точечные мутации, повышающие устойчивость к циклодиенам, найдены у
некоторых видов (тараканы, москиты, комнатные мухи, плодовые мушки, алейродиды, хрущак
каштановый). Точечные мутации, повышающие устойчивость натриевых канальцев к ДДТ,
найдены у шести видов (комнатные мухи, москиты, тараканы, тля персиковая, моль
капустная, табачная листовертка-почкоед). Одна из нескольких дополнительных точечных
мутаций может также привести к суперустойчивости.
К счастью для нас, наша нервная система является нечувствительной к действию
таких инсектицидов как циклодиены и ДДТ. Однако мы очень чувствительны к
органофосфатам, которые первоначально разрабатывались как отравляющие вещества для
ведения войны. Органофосфаты синтезируются в виде тиоформы (R3P=S), которая является
относительно стабильной. Когда это соединение попадает в насекомое (или в человека),
оно переходит в оксоформу (R3P=O), которая быстро взаимодействует с
ацетилхолинэстеразой. Эти соединения вызывают смерть не только при вдыхании, но и при
взаимодействии с кожным покровом. Изучение биохимии ацетилхолинэстеразы демонстрирует,
что активные сайты остатков серина участвуют в гидролизе ацетилхолина, образуя
интермедиат О-ацетилсерин, который быстро гидролизуется. Таким образом, органофосфаты
инактивируют ферменты, тем самым, замедляя гидролиз.
Злоупотребление наркотиками. Ядра accumbens были открыты как своего
рода центры удовольствия в мозге, где рост уровня допамина-нейропереносчика
воспринимался как удовольствие (эйфория, блаженство). Множество признаков указывает на
злоупотребление наркотиками (включая никотин), как на стимуляторы уровня допамина в
организме, который (уровень) отвечает за чувства удовольствия, вызываемые наркотиками.
Экспериментальные животные будут добровольно сами принимать эти наркотики, что говорит
о взникновении привыкания к наркотическим препаратам. У людей и животных привыкание или
уменьшение чувствительности к таким агентам происходит так, что требуются для получения
соизмеримого удовольствия большие дозы. Дозы наркотика могут стократно возрастать, что
выходит далеко за пределы того, что изначально являлось летальным воздействием.
Окончательное прекращение потребления наркотиков впоследствие вызывает дисфорию (в
противоположность эйфории), так как тело реадаптируется к нехватке экзогенных агентов.
Наркоманы в это время идут на то, чтобы продолжать принятие наркотиков в еще больших
дозах. Реабилитация наркоманов – это долгий процесс, обычно длящийся долгие годы.
Наркотическая зависимость была сравнима в масштабах с хроническими заболеваниями,
такими, как: диабет, астма и повышенное кровяное давление. Многие исследования в
области злоупотребления наркотиками направлены на понимание молекулярной основы
действия наркотика, толерантности организма и реакцию отказа от наркотиков на их
воздействие. Один из подходов к пониманию действия наркотиков был направлен на поиск их
рецепторов. Это первый шаг в понимании путей сигнальной трансдукции. Последние работы
указывают на важность серотониновых путей в возбуждении при наркотическом воздействии,
а также на важность глутаматовых путей, особенно рецепторов NMDA, в развитии тяги к
большему количеству наркотиков.
Фармакологические свойства опиоидов известны с древних времен. Выделение
наиболее активного компонента - морфина было впервые описано в 1803. Героин
(диацетилморфин), который имеет более высокую скорость проникновения в мозг, был
синтезирован в 1874. Морфин и его активные природные аналоги, такие как кодеин,
вызывают не только эйфорию, но также являются хорошими анальгетиками и высоко
эффективны в борьбе с диареей. Много усилий было положено на попытки сделать
производные этих соединений, которые вызывают только обезболивание без эйфории, но до
сих пор только с ограниченным успехом. Однако был разработан эффективный антагонист
(для лечения передозировок), такой же долгоживущий, хотя гораздо менее
эффективный, производное (метадон), которое полезно в реабилитации. Несмотря на то, что
он не вызывает эйфории (преимущество в лечении), он достаточно силен, чтобы избежать
синдромов ломки. Допустимо прописывать его для раковых больных в целях облегчения
боли, что также устраняет потребность в марихуане.
Изучение рецепторов привело к выявлению трех основных подтипов рецепторов
морфия, которыми оказались G-белки (Gi). Они сдерживают образование аденил-циклазы в
целевых нейронах, таким образом, увеличивая проводимость каналов калия, уменьшая
проводимость каналов кальция и вызывая гиперполяризованное состояние. Как именно это
приводит к обезболиванию неясно; пациенты, находящиеся на лечении для избавления от
наркотической зависимости, говорят, что боль не ушла и даже не уменьшилась, они просто
больше не воспринимают ее как нечто, вызывающее отвращение. Эндогенные лиганды для
рецепторов, два из которых являются пентопептидами, выведенными из предшественников,
были обнаружены и названы эндорфинами (эндогенный морфин).
Амфетамин был впервые синтезирован в 1887. Он относится к фармокологически
активным компонентам некоторых растений Восточной Африки и Китая и известен своими
целебными свойствами. Раньше этот препарат прописывался в таблетках для лечения
нарколепсии (внезапный сон) в 1935 и был отдан военным в 1940-ых для поддержания боевой
готовности. В 50-ые и 60-ые годы он принимался студентами и дальнобойщиками для
поддержания активности без сна и отдыха. Препарат медленно поглощается при оральном
принятии, но когда вводится внутривенно или (особенно метамфетамин) ингаляцией, то
вызывает чувство удовольствия, ведущее к злоупотреблению «скоростными чудачествами».
Агенты класса амфетамина перемещаются допаминергическими нейронами, препятствуя
реабсорбции допамина и ускоряя выбрасывание допамина из внутриклеточных пазух. Так как
действие препарата проходит быстро, то лица, злоупотребляющие наркотиками, могут
принимать дозы с двух часовыми интервалами в течение нескольких дней, а
потом «ломаются» (спят в течение долгого периода). Привыкание возникает быстро, требуя
увеличения доз, а последующее воздержание характеризуется вялостью, депрессией и, в
основном, неприятными чувствами. Продолжительное употребление может вызвать
галлюцинации и психозы, напоминающие параноидную шизофрению. Амфетамины запрещены для
занятий спортом, потому что они улучшают исполнение. Но его производные все еще
используются для борьбы с потерей веса для улучшения аппетита (включая
фенолпропаноламин в Дексатриме и в Риталине) и для лечения гиперактивного дефицита
внимания у детей.
Кокаин впервые был обнаружен в кустарнике Южной Америки. В период
завоевания этого континента, испанцы впервые наложили запрет на привычку местных
жителей жевать листья этого растения, но затем заметили, что рабы работали усерднее и
дольше, когда им позволили жевать листья. Кокаин был добавлен в Кока-колу, производимую
в 1886 г., пока он не был устранен в 1906 г. Позднее напитки с кокаином продавались в
качестве альтернативы алкоголю как часть движения за трезвость. В 1914 г. федеральное
правительство США установило запрет на продажу кокаина и опиума, как составляющих
лекарственных препаратов, в аптеках. Такая практика ни к чему хорошему не привела. По
оценкам экспертов в США насчитывается около полмиллиона наркоманов. Для достижения
желаемого эффекта важен способ введения, обычно это ингаляции или внутривенные
инъекции. Эйфория от кокаина длится в течение получаса, гораздо меньшее время, чем от
амфетамина, а с увеличе нием дозы ведет к агрессии. Так же, как и с амфетамином,
основа достижения удовольствия заключается в уменьшении реабсорбции допамина через
дофаминергические нейроны. Недавно также было сообщено о роли серотонина в развитии
наркотического эффекта. В больших концентрациях, однако, кокаин может также подавлять
определенный рецепторы нейропереносчиков и даже блокировать аксонные натриевые каналы.
Это способность была задействована в разработке производных, таких как прокаин и
лидокаин, которые широко используются как местные анастетики.
Один из наиболее часто употребляемых наркотиков получен из растения марихуаны.
Основным составляющим марихуаны является Δ9-тетрагидроканнабинол (ТНС):
ТНС
Поглощение достаточного количества ТНС обычно вызывает чувство эйфории, которое может
длиться несколько часов. Оно может сопровождаться беспорядочными мыслительными
процессами и психомоторными проявлениями (координация, время реакции), которые длятся
полдня, так что следует воздержаться от вождения автомобиля. Уменьшение
чувствительности к доставляющим удовольствие эффектам приходит с повторяющимися
высокими дозами за короткие интервалы времени. Однако невозможно продемонстрировать
психическую зависимость на животных или людях в соответствии с условиями обычного
употребления. Употребление сильных антагонистов показало, что могут появиться симптомы
ломки, однако такие симптомы обычно незаметны, потому что время полужизни ТНС в крови
достаточно высоко (приблизительно день).
Недавно с помощью радиоактивного лиганда рецепторы для ТНС были определены как
члены надсемества G-белков. Это привело к идентификации эндогенного лиганда, названного
анандамидом (санскрит для «блаженства»), который оказался производным арахидоновой
кислоты – компонента липидной мембраны. Любопытно, что анандамид является растворимым
липидом, он не хранится в везикуле, подобно другим нейропереносчикам. Это позволяет
предположить существование другого класса лигандов. Рецепторы ТНС обнаружены в двух
изоформах, одни – в центральной нервной системе, и другие – в клетках иммунной
системы, такие как макрофаги, потенциально обеспечивающие основу для некоторых реакций,
которые могут влиять на иммунные функции из-за употребления марихуаны. Связанный с
рецепторами ТНС уменьшает производство сАМР в нейронах, приводя к уменьшению активности
кальциевых и калиевых каналов. Как именно это приводит к возникновению удовольствия
неясно, но недавно было показано, что введение ТНС крысам приводит к высвобождению
допамина в ядрах accumbens, подобно высвобождению эндрофинов.
|
Особенности диагностики и лечения полинейропатии, вызванной отравлением грибами |
В. М. Енин, заведующий отделением ГБО; В. Л. Кузьменко, заведующий отделением реанимации; Г. Н. Манза, врач-анестезиолог, медико-санитарная часть Государственной акционерной холдинговой компании «Черноморский судостроительный завод», г. Николаев
В 1987 году в Николаевской области были зарегистрированы тяжелые полинейропатии, возникающие после приема в пищу съедобных грибов: рыжиков и лисичек. Цель данной публикации — привлечь внимание врачей различных специальностей к нерешенной клинической и токсикологической проблеме, масштаб которой увеличивается из года в год. По нашим данным, в 2002 году в Николаевской области заболели около 200 человек, длительность временной нетрудоспособности колебалась от 30 до 90 дней. Учитывая стоимость лекарственных препаратов, немедикаментозных расходов и трудопотерь, экономический ущерб, связанный с лечением этого заболевания, достаточно значителен.
Клиническая картина
Заболевание, как правило, начинается в утренние часы с парестезий и болей в стопах, затем в кистях рук, интенсивность боли быстро нарастает до нестерпимой. У некоторых больных в процесс вовлекаются кончик носа, ушные раковины, бывают боли в зубах и зуд десен в области верхней челюсти, непродолжительная заложенность носа. Процесс распространяется в проксимальном направлении: на ногах — до коленных суставов, на руках — до плечевого пояса. При прогрессировании заболевания появляются отеки стоп, нижней трети голеней, кистей, у некоторых больных — трофические язвы, мацерация кожи в связи с тем, что они, пытаясь уменьшить боль, принимали холодные водные ванночки для рук и ног. У других заболевших наблюдаются атрофические изменения кожи, преимущественно кистей. Страх прикосновения к предметам в связи с возникающей болью приводит к вынужденному положению рук и ног. Отмечаются болезненность при пальпации кожных покровов конечностей и при надавливании точек выхода второй ветви тройничного нерва, гиперестезия кожи по типу высоких носков и чулок, нарушение проприоцептивной чувствительности, снижение мышечных тонуса и силы, гипотрофия мышц конечностей. Коленные и брюшные рефлексы сохранены, иногда усилены, симметричны. Иногда на протяжении наблюдения до двух раз и более отслаивается эпидермис кистей и стоп, а также отмечаются мозаичная пигментация, гиперкератоз, бледность кожных покровов лица, умеренная тахикардия, нормотермия. Снижается аппетит, нарушается сон, развивается тяжелая невротизация.
У 30 больных проведены реовазографические исследования дистального кровотока на стопах реографической приставкой РГ-4-02. При отсутствии отеков реографический индекс (РИ) был в пределах нормы (0,7-1,2), при отеке снижался в соответствии с его выраженностью. У всех больных отмечались признаки повышения артериального тонуса.
Транскутанное определение парциального давления кислорода (рО2) проведено у 25 больных. При удовлетворительной пульсации всех артерий стопы рО2 на ее тыле колебалось от 5 до 46 мм рт. ст., а на уровне третьего межреберья по срединно-ключичной линии — от 52 до 76 мм рт. ст. Измерения проводили монитором ТСН-2 фирмы «Радиометр». Приведенные данные свидетельствуют о нарушении гемодинамики и транспорта кислорода в дистальных отделах конечностей и возможном участии ишемии и гипоксии в формировании полинейропатии.
В 2002 году под нашим наблюдением находилось 133 больных (табл.1 и 2).
Способы кулинарной обработки грибов не влияли на развитие заболевания и выраженность клинических проявлений. Яд оставался термостабилен, не разрушался при варке, жарении, сушке и мариновании. Хранение сушеных и консервированных грибов не уменьшает вероятности отравления и тяжести клинических проявлений. При кипячении яд может возгоняться с паром. Мы наблюдали отравление парами, вдыхаемыми поваром из котла во время приготовления грибов. Зарегистрировано заболевание полинейропатией грудного ребенка, находившегося на естественном вскармливании.
Тяжесть течения заболевания не зависит от сопутствующего приема алкоголя. Индивидуальная чувствительность к яду выражается по-разному. При прочих равных условиях у некоторых больных развивается тяжелое заболевание, а у других прием в пищу грибов остается без последствий. Вместе с тем, преморбидный статус влияет на течение полинейропатии. Более тяжело и длительно она протекает у пожилых женщин, пациентов с дефицитом питания, а также у больных с хроническими заболеваниями почек и гипопротеинемией. При попытке объяснить индивидуальную чувствительность к яду мы обратили внимание на то, что среди заболевших было 69,9% женщин, в основном фертильного возраста. Среди мужчин, существенных колебаний по возрасту не было, что, по нашему мнению, может свидетельствовать о протекторной роли андрогенов в отношении данного токсина, а также об участии каталазы и алкогольдегидрогеназы в инактивации яда. Алкогольдегидрогеназа — редуцируемый фермент, более активный у мужчин, каталаза присутствует у мужчин в больших количествах в связи с преобладанием мышечной массы. Другой причиной избирательного поражения полинейропатией может быть то, что не все, присутствующие за одним столом, съедали грибы, адсорбировавшие яд. Следующим объяснением индивидуальной чувствительности к яду является доказанное деление людей на быстрых и медленных инактиваторов изониазида. У первых последствия токсикологических воздействий менее выражены или вообще не проявляются (Я. Ю. Попелянский, 1989).
Время от приема в пищу грибов до первых проявлений нейропатии непостоянно. В прошлые годы оно составляло от 4 до 21 дня, в 2002 году — 1,5-4 дня. Отмечалось повторное употребление грибов. Мы наблюдали два случая летальных исходов пожилых одиноких женщин, которые ели лисички в выходные дни, а через неделю их обнаружили мертвыми у себя дома. Можно предположить, что причиной их смерти стала дегидратация. Зафиксирован и падеж домашней птицы, кошек и собак, которым были скормлены остатки грибов.
Замечено, что в весенний период при употреблении в пищу рыжих грибов полинейропатии возникали крайне редко. Вместе с тем, появились сведения, что полинейропатии развивались не только в связи с приемом в пищу рыжиков и лисичек, но и других грибов. Все эти грибы собирали в лесопосадках, заброшенных фруктовых садах, вблизи автомобильных и железных дорог, что, на наш взгляд, не указывает на причину отравления, а отражает только места сбора грибов.
В Николаевской области первые случаи заболеваний зарегистрированы в северных районах: Первомайском, Кривоозерском, Доманевском. В дальнейшем «география отравлений» распространилась на Братский район, а в 2002 году к югу — Веселиновский, Еланецкий, Новобугский и район ж/д станции Колосовка.
Так как большинство медицинских работников не осведомлено о возможности развития полинейропатий в связи с приемом в пищу грибов, первые случаи заболевания связывали с перенесенным гриппом, нервным или физическим перенапряжением, остеохондрозом и другими причинами. Больные лечились у врачей различных специальностей: терапевтов, анестезиологов, невропатологов, токсикологов, что не способствовало накоплению информации по данному заболеванию, затягивало начало рациональной терапии и активной профилактики. Отсутствие данных об этиологии и патогенезе заболевания приводило, в лучшем случае, к проведению недифференцированной терапии полинейропатий (Я. Ю. Попелянский, 1989; В. А. Яворская, Л. Н. Пустовид, 2000).
Данный симптомокомплекс следует рассматривать как сенсорно-моторно-вегетативное поражение. Сохранение коленного и брюшных рефлексов, эффективность плазмафереза на ранних стадиях заболевания может свидетельствовать о демиелинизации со свойственными ей аутоиммунными процессами и минимальными аксональными повреждениями. Подтверждением данного предположения могут служить сроки и полнота восстановления нарушенных функций после перенесенного заболевания.
Несмотря на то, что во всех случаях заболевания отмечена связь с приемом в пищу грибов, роль последних в возникновении заболевания остается неясной. Вместе с тем, как правило, грибы собирали опытные грибники, неоднократно употреблявшие в пищу аналогичные грибы без каких-либо последствий.
В литературе имеется информация об отравлениях белыми грибами и маслятами, собранными в районах промышленной загазованности. Известно, что многие съедобные грибы в определенные периоды накапливают в плодовых телах продукты автолитического разложения. Особенности биологии грибов, расположение мицелия в 10-сантиметровом слое почвы, гетеротрофный характер их питания может способствовать накоплению в них любых ксенобиотиков, в том числе и ядохимикатов (Н. С. Орлов и соавт., 1990).
Ориентируясь на места сбора грибов: лесополосы, близ полей с зерновыми культурами и подсолнечником, а также в связи с тем, что при употреблении в пищу идентичных грибов в весеннее время отравления крайне редки, мы предположили, что веществом, вызывающим отравление, может быть один из ядов, применяемых для борьбы с грызунами. Косвенным подтверждением этого предположения может служить то, что приблизительно в одно и то же время с появлением заболевания в области исчезли суслики. Вместе с тем, количество мышей не уменьшилось, что может иметь следующее объяснение: мыши размножаются более интенсивно, имеют 6-8 пометов в год по 6-10 мышат, а суслики — 1 помет в год по 4-8 животных.
С переходом на селе к фермерским формам хозяйствования усилилась борьба со всеми видами потерь, в том числе с наносимыми грызунами, но контроль за побочными действиями ядохимикатов, их реализацией и правилами применения значительно снизился. Появление первых отравлений в северных районах области и постепенное их распространение к югу может быть объяснено тем, что в северных районах более интенсивное производство зерновых и подсолнечника. Очевидно, получившие яд мыши мигрируют в расположенные рядом с полями лесополосы и заброшенные сады, где и погибают. Продукты их разложения в комплексе с ядохимикатами поглощают грибы. Предполагаемый путь поступления яда в организм человека объясняет причину того, почему не у всех употреблявших в пищу грибы, которые раньше считались съедобными, появляются признаки отравлений. Отравление могут вызывать только грибы, проросшие в непосредственной близости от тушки погибшего животного или приманки с ядом. Сами по себе грибы не являются ядовитыми.
Употребление в пищу любых рыжих грибов, собранных в сосновых лесах, расположенных на юге области, не вызывает нейропатий. Это объясняется отсутствием вблизи этих лесов зерновых и подсолнечниковых плантаций, следовательно, и необходимости травить грызунов. Осенние отравления могут быть связаны с тем, что борьба с грызунами начинается тогда, когда созревают зерновые, ближе к осени. Привлечение в качестве объяснения мутации грибов, вследствие радиационных или токсических воздействий, приводящих к образованию ядов в грибах, не выдерживает критики с точки зрения классической биологии.
Поиск в доступной литературе и Интернете сведений о грибах, способных вызвать полинейропатию, напоминающую описанную выше, оказались безрезультатными. При отравлении паутинником оранжево-рыжим возможны нейропатии, однако в сочетании с желудочно-кишечными расстройствами, а яд ореланин — термолабильный пептид — разрушается при кипячении и высыхании. Информации о подобных отравлениях в других странах нет, создается впечатление, что данная проблема является сугубо нашим национальным бедствием.
Мнение по указанной проблеме сертифицированного специалиста по ядам Х. Щелкунов (Майями, штат Флорида, США) следующее: «Проблема в том, что в США вряд ли кто ест дикие грибы, и поэтому знания о грибных отравлениях ограничены. Наибольший опыт мы имеем с грибами иритантами кишечника и сталкивались с несколькими случаями отравлений амонитами. Отравления возникают только у эмигрантов из Восточной Европы».
Информации о веществах, способных вызывать полинейропатию, достаточно. Несмотря на многие общие симптомы, характеризующие полинейропатию, каждая из них несет определенную клиническую окраску, характерную для вызвавшего ее вещества. Мы предположили возможную связь ядохимикатов с развитием полинейропатии, провели анализ свойств и токсического действия различных ядов, применяемых для дератизации.
Препаратов, содержащих мышьяк, на рынке в настоящее время нет. Несмотря на то, что для клиники отравления препаратами мышьяка характерна полинейропатия, отравления мышьяком всегда сопровождаются желудочно-кишечными расстройствами.
Крысид, как правило, в полевых условиях не применяется и является малотоксичным для человека.
Кумариновые производные приводят к смерти грызунов в связи с развившейся гипокоагуляцией.
Микробиологические препараты при термической обработке разрушаются, в связи с чем не могут рассматриваться как способные вызвать нейропатию.
Для углекислого бария характерен понос, дегидратация и судороги.
Наибольшее распространение для применения в полевых условиях получил фосфид цинка, без ограничения продаваемый на рынках и в магазинах бытовой химии.
Фосфид цинка (Zn3P2) не растворим в воде и спирте, слабо растворим в щелочах и маслах, хорошо растворим даже в слабых кислотах. При реакции с кислотами выделяется фосфористый водород, который является действующим началом этого яда: Zn3P2+6НСl=3ZnCl2+2РН3. Фосфористый водород — газообразное соединение. Содержание его в воздухе в дозе 0,01 мг/л — опасно при условии длительной экспозиции. Концентрация 1,5 мг/л является смертельной при вдыхании на протяжении 5-10 минут. Фосфористый водород нарушает обмен веществ и является ядом для нервной системы и крови. В желудке животных и человека под влиянием соляной кислоты образуется фосфористый водород и хлористый цинк. Последний безвреден для животных. Летальная доза фосфида цинка для крысы равна 75-150 мг/кг, мыши — 150-200 мг/кг, суслика — 20-24 мг/кг. Летальный исход наблюдается только при одномоментном введении летальной дозы. Повторное введение сублетальных доз не вызывает гибели животных.
Приведенные данные позволяют предположить, что наиболее вероятным ядом, вызывающим полинейропатию, является фосфид цинка.
Лечение
Подавляющее количество заболевших со средней и легкой степенью заболевания прошли лечение в ЦРБ. В областной токсикологический центр направляли больных с тяжелыми формами заболевания, без видимого улучшения на протяжении 3-4 дней с начала лечения. Терапию, проводимую по поводу данного заболевания, следует рассматривать как недифференцированную. Как правило, применяли глюкокортикоиды в дозе 100-150 мг в сутки, витамины группы В, берлитион по 600-1200 мг в сутки внутривенно капельно, антигистаминные препараты, детоксикационную терапию (кристаллоиды, 5% глюкозу, неогемодез 0,7 мл/кг/сутки, микроциркуляторные и энергетические плазмозаменители, реосорбилакт 0,3 мл/кг/сутки). Кроме того, назначали ненаркотические аналгетики, снотворные. При переводе в областной токсикологический центр сохраняли преемственность начатой медикаментозной терапии. Дополнительно назначали L-лизин эсцинат по 5 г 2 раза в сутки внутривенно; Эрбисол по 2 г внутримышечно вечером № 20; некоторым больным проведен плазмаферез. Ограничения в проведении плазмафереза связаны с поздними сроками поступления больных и экономическими соображениями. Всем больным с тяжелым течением полинейропатии применяли ГБО в режиме 1,25 атмосферы по 60 минут, длительность колебалась от 8 до 12 сеансов. Режимы ниже 1,25 атмосферы были малоэффективными. Сеансы проводили в барокамерах ОКА-МТ и БЛКС 3-01. Длительность курса зависела от выраженности регресса клинических проявлений. После 2-4 сеансов ГБО интенсивность болей уменьшалась, больные начинали самостоятельно передвигаться. С этого момента к терапии добавляли прозерин или галантамин, внутрисосудистую лазеротерапию № 7, ежедневно гелий-неоновым лазером АЛОУ-2 мощностью 2 мВт по 30 минут. Все больные выписаны для амбулаторного лечения после четко наметившейся тенденции к выздоровлению.
Профилактика
Методы санитарно-просветительной работы с целью профилактики данного заболевания с использованием газет, радио и телевидения не эффективны, среди заболевших преобладают лица с низкими доходами.
Об изменении традиции сбора и употребления в пищу дикорастущих грибов можно говорить только при условии улучшения благосостояния населения.
На количество заболевших может положительно повлиять упорядочение реализации и применения ядохимикатов, а также мероприятия по дератизации, категорический запрет свободной продажи таких сильнодействующих ядов, как фосфид цинка.
Выводы
Попытка исследовать частную проблему — причину возникновения полинейропатий после приема в пищу съедобных грибов, очерчивает широкий круг экологических проблем. Неразумное применение ядохимикатов приносит не только вред здоровью людей, но и значительные экономические потери, нарушает равновесие в биоценозах.
В литературе по дезинфекции, дезинсекции и дератизации приводятся сведения о значительном ущербе, наносимом мышевидными грызунами народному хозяйству. Вместе с тем, по некоторым данным, потери, связанные с элементарной бесхозяйственностью, значительно превосходят те, которые списывают на вредителей сельскохозяйственных культур (А. А. Любищев). Представляется, что нарушения в биоценозе в связи с затравкой грызунов выглядят следующим образом: погибших или заболевших грызунов и остатки приманок поедают хищные птицы, лисы, куницы и ласки, которые в естественных условиях регулируют количество грызунов в природе, а последние, не имея врагов, интенсивно размножаются. Следует думать, что упорядочение применения ядохимикатов будет способствовать природному равновесию.
В 1987 году в Николаевской области были зарегистрированы тяжелые полинейропатии, возникающие после приема в пищу съедобных грибов: рыжиков и лисичек. Цель данной публикации — привлечь внимание врачей различных специальностей к нерешенной клинической и токсикологической проблеме, масштаб которой увеличивается из года в год. По нашим данным, в 2002 году в Николаевской области заболели около 200 человек, длительность временной нетрудоспособности колебалась от 30 до 90 дней. Учитывая стоимость лекарственных препаратов, немедикаментозных расходов и трудопотерь, экономический ущерб, связанный с лечением этого заболевания, достаточно значителен.
Клиническая картина
Заболевание, как правило, начинается в утренние часы с парестезий и болей в стопах, затем в кистях рук, интенсивность боли быстро нарастает до нестерпимой. У некоторых больных в процесс вовлекаются кончик носа, ушные раковины, бывают боли в зубах и зуд десен в области верхней челюсти, непродолжительная заложенность носа. Процесс распространяется в проксимальном направлении: на ногах — до коленных суставов, на руках — до плечевого пояса. При прогрессировании заболевания появляются отеки стоп, нижней трети голеней, кистей, у некоторых больных — трофические язвы, мацерация кожи в связи с тем, что они, пытаясь уменьшить боль, принимали холодные водные ванночки для рук и ног. У других заболевших наблюдаются атрофические изменения кожи, преимущественно кистей. Страх прикосновения к предметам в связи с возникающей болью приводит к вынужденному положению рук и ног. Отмечаются болезненность при пальпации кожных покровов конечностей и при надавливании точек выхода второй ветви тройничного нерва, гиперестезия кожи по типу высоких носков и чулок, нарушение проприоцептивной чувствительности, снижение мышечных тонуса и силы, гипотрофия мышц конечностей. Коленные и брюшные рефлексы сохранены, иногда усилены, симметричны. Иногда на протяжении наблюдения до двух раз и более отслаивается эпидермис кистей и стоп, а также отмечаются мозаичная пигментация, гиперкератоз, бледность кожных покровов лица, умеренная тахикардия, нормотермия. Снижается аппетит, нарушается сон, развивается тяжелая невротизация.
У 30 больных проведены реовазографические исследования дистального кровотока на стопах реографической приставкой РГ-4-02. При отсутствии отеков реографический индекс (РИ) был в пределах нормы (0,7-1,2), при отеке снижался в соответствии с его выраженностью. У всех больных отмечались признаки повышения артериального тонуса.
Транскутанное определение парциального давления кислорода (рО2) проведено у 25 больных. При удовлетворительной пульсации всех артерий стопы рО2 на ее тыле колебалось от 5 до 46 мм рт. ст., а на уровне третьего межреберья по срединно-ключичной линии — от 52 до 76 мм рт. ст. Измерения проводили монитором ТСН-2 фирмы «Радиометр». Приведенные данные свидетельствуют о нарушении гемодинамики и транспорта кислорода в дистальных отделах конечностей и возможном участии ишемии и гипоксии в формировании полинейропатии.
В 2002 году под нашим наблюдением находилось 133 больных (табл.1 и 2).
Способы кулинарной обработки грибов не влияли на развитие заболевания и выраженность клинических проявлений. Яд оставался термостабилен, не разрушался при варке, жарении, сушке и мариновании. Хранение сушеных и консервированных грибов не уменьшает вероятности отравления и тяжести клинических проявлений. При кипячении яд может возгоняться с паром. Мы наблюдали отравление парами, вдыхаемыми поваром из котла во время приготовления грибов. Зарегистрировано заболевание полинейропатией грудного ребенка, находившегося на естественном вскармливании.
Тяжесть течения заболевания не зависит от сопутствующего приема алкоголя. Индивидуальная чувствительность к яду выражается по-разному. При прочих равных условиях у некоторых больных развивается тяжелое заболевание, а у других прием в пищу грибов остается без последствий. Вместе с тем, преморбидный статус влияет на течение полинейропатии. Более тяжело и длительно она протекает у пожилых женщин, пациентов с дефицитом питания, а также у больных с хроническими заболеваниями почек и гипопротеинемией. При попытке объяснить индивидуальную чувствительность к яду мы обратили внимание на то, что среди заболевших было 69,9% женщин, в основном фертильного возраста. Среди мужчин, существенных колебаний по возрасту не было, что, по нашему мнению, может свидетельствовать о протекторной роли андрогенов в отношении данного токсина, а также об участии каталазы и алкогольдегидрогеназы в инактивации яда. Алкогольдегидрогеназа — редуцируемый фермент, более активный у мужчин, каталаза присутствует у мужчин в больших количествах в связи с преобладанием мышечной массы. Другой причиной избирательного поражения полинейропатией может быть то, что не все, присутствующие за одним столом, съедали грибы, адсорбировавшие яд. Следующим объяснением индивидуальной чувствительности к яду является доказанное деление людей на быстрых и медленных инактиваторов изониазида. У первых последствия токсикологических воздействий менее выражены или вообще не проявляются (Я. Ю. Попелянский, 1989).
Время от приема в пищу грибов до первых проявлений нейропатии непостоянно. В прошлые годы оно составляло от 4 до 21 дня, в 2002 году — 1,5-4 дня. Отмечалось повторное употребление грибов. Мы наблюдали два случая летальных исходов пожилых одиноких женщин, которые ели лисички в выходные дни, а через неделю их обнаружили мертвыми у себя дома. Можно предположить, что причиной их смерти стала дегидратация. Зафиксирован и падеж домашней птицы, кошек и собак, которым были скормлены остатки грибов.
Замечено, что в весенний период при употреблении в пищу рыжих грибов полинейропатии возникали крайне редко. Вместе с тем, появились сведения, что полинейропатии развивались не только в связи с приемом в пищу рыжиков и лисичек, но и других грибов. Все эти грибы собирали в лесопосадках, заброшенных фруктовых садах, вблизи автомобильных и железных дорог, что, на наш взгляд, не указывает на причину отравления, а отражает только места сбора грибов.
В Николаевской области первые случаи заболеваний зарегистрированы в северных районах: Первомайском, Кривоозерском, Доманевском. В дальнейшем «география отравлений» распространилась на Братский район, а в 2002 году к югу — Веселиновский, Еланецкий, Новобугский и район ж/д станции Колосовка.
Так как большинство медицинских работников не осведомлено о возможности развития полинейропатий в связи с приемом в пищу грибов, первые случаи заболевания связывали с перенесенным гриппом, нервным или физическим перенапряжением, остеохондрозом и другими причинами. Больные лечились у врачей различных специальностей: терапевтов, анестезиологов, невропатологов, токсикологов, что не способствовало накоплению информации по данному заболеванию, затягивало начало рациональной терапии и активной профилактики. Отсутствие данных об этиологии и патогенезе заболевания приводило, в лучшем случае, к проведению недифференцированной терапии полинейропатий (Я. Ю. Попелянский, 1989; В. А. Яворская, Л. Н. Пустовид, 2000).
Данный симптомокомплекс следует рассматривать как сенсорно-моторно-вегетативное поражение. Сохранение коленного и брюшных рефлексов, эффективность плазмафереза на ранних стадиях заболевания может свидетельствовать о демиелинизации со свойственными ей аутоиммунными процессами и минимальными аксональными повреждениями. Подтверждением данного предположения могут служить сроки и полнота восстановления нарушенных функций после перенесенного заболевания.
Несмотря на то, что во всех случаях заболевания отмечена связь с приемом в пищу грибов, роль последних в возникновении заболевания остается неясной. Вместе с тем, как правило, грибы собирали опытные грибники, неоднократно употреблявшие в пищу аналогичные грибы без каких-либо последствий.
В литературе имеется информация об отравлениях белыми грибами и маслятами, собранными в районах промышленной загазованности. Известно, что многие съедобные грибы в определенные периоды накапливают в плодовых телах продукты автолитического разложения. Особенности биологии грибов, расположение мицелия в 10-сантиметровом слое почвы, гетеротрофный характер их питания может способствовать накоплению в них любых ксенобиотиков, в том числе и ядохимикатов (Н. С. Орлов и соавт., 1990).
Ориентируясь на места сбора грибов: лесополосы, близ полей с зерновыми культурами и подсолнечником, а также в связи с тем, что при употреблении в пищу идентичных грибов в весеннее время отравления крайне редки, мы предположили, что веществом, вызывающим отравление, может быть один из ядов, применяемых для борьбы с грызунами. Косвенным подтверждением этого предположения может служить то, что приблизительно в одно и то же время с появлением заболевания в области исчезли суслики. Вместе с тем, количество мышей не уменьшилось, что может иметь следующее объяснение: мыши размножаются более интенсивно, имеют 6-8 пометов в год по 6-10 мышат, а суслики — 1 помет в год по 4-8 животных.
С переходом на селе к фермерским формам хозяйствования усилилась борьба со всеми видами потерь, в том числе с наносимыми грызунами, но контроль за побочными действиями ядохимикатов, их реализацией и правилами применения значительно снизился. Появление первых отравлений в северных районах области и постепенное их распространение к югу может быть объяснено тем, что в северных районах более интенсивное производство зерновых и подсолнечника. Очевидно, получившие яд мыши мигрируют в расположенные рядом с полями лесополосы и заброшенные сады, где и погибают. Продукты их разложения в комплексе с ядохимикатами поглощают грибы. Предполагаемый путь поступления яда в организм человека объясняет причину того, почему не у всех употреблявших в пищу грибы, которые раньше считались съедобными, появляются признаки отравлений. Отравление могут вызывать только грибы, проросшие в непосредственной близости от тушки погибшего животного или приманки с ядом. Сами по себе грибы не являются ядовитыми.
Употребление в пищу любых рыжих грибов, собранных в сосновых лесах, расположенных на юге области, не вызывает нейропатий. Это объясняется отсутствием вблизи этих лесов зерновых и подсолнечниковых плантаций, следовательно, и необходимости травить грызунов. Осенние отравления могут быть связаны с тем, что борьба с грызунами начинается тогда, когда созревают зерновые, ближе к осени. Привлечение в качестве объяснения мутации грибов, вследствие радиационных или токсических воздействий, приводящих к образованию ядов в грибах, не выдерживает критики с точки зрения классической биологии.
Поиск в доступной литературе и Интернете сведений о грибах, способных вызвать полинейропатию, напоминающую описанную выше, оказались безрезультатными. При отравлении паутинником оранжево-рыжим возможны нейропатии, однако в сочетании с желудочно-кишечными расстройствами, а яд ореланин — термолабильный пептид — разрушается при кипячении и высыхании. Информации о подобных отравлениях в других странах нет, создается впечатление, что данная проблема является сугубо нашим национальным бедствием.
Мнение по указанной проблеме сертифицированного специалиста по ядам Х. Щелкунов (Майями, штат Флорида, США) следующее: «Проблема в том, что в США вряд ли кто ест дикие грибы, и поэтому знания о грибных отравлениях ограничены. Наибольший опыт мы имеем с грибами иритантами кишечника и сталкивались с несколькими случаями отравлений амонитами. Отравления возникают только у эмигрантов из Восточной Европы».
Информации о веществах, способных вызывать полинейропатию, достаточно. Несмотря на многие общие симптомы, характеризующие полинейропатию, каждая из них несет определенную клиническую окраску, характерную для вызвавшего ее вещества. Мы предположили возможную связь ядохимикатов с развитием полинейропатии, провели анализ свойств и токсического действия различных ядов, применяемых для дератизации.
Препаратов, содержащих мышьяк, на рынке в настоящее время нет. Несмотря на то, что для клиники отравления препаратами мышьяка характерна полинейропатия, отравления мышьяком всегда сопровождаются желудочно-кишечными расстройствами.
Крысид, как правило, в полевых условиях не применяется и является малотоксичным для человека.
Кумариновые производные приводят к смерти грызунов в связи с развившейся гипокоагуляцией.
Микробиологические препараты при термической обработке разрушаются, в связи с чем не могут рассматриваться как способные вызвать нейропатию.
Для углекислого бария характерен понос, дегидратация и судороги.
Наибольшее распространение для применения в полевых условиях получил фосфид цинка, без ограничения продаваемый на рынках и в магазинах бытовой химии.
Фосфид цинка (Zn3P2) не растворим в воде и спирте, слабо растворим в щелочах и маслах, хорошо растворим даже в слабых кислотах. При реакции с кислотами выделяется фосфористый водород, который является действующим началом этого яда: Zn3P2+6НСl=3ZnCl2+2РН3. Фосфористый водород — газообразное соединение. Содержание его в воздухе в дозе 0,01 мг/л — опасно при условии длительной экспозиции. Концентрация 1,5 мг/л является смертельной при вдыхании на протяжении 5-10 минут. Фосфористый водород нарушает обмен веществ и является ядом для нервной системы и крови. В желудке животных и человека под влиянием соляной кислоты образуется фосфористый водород и хлористый цинк. Последний безвреден для животных. Летальная доза фосфида цинка для крысы равна 75-150 мг/кг, мыши — 150-200 мг/кг, суслика — 20-24 мг/кг. Летальный исход наблюдается только при одномоментном введении летальной дозы. Повторное введение сублетальных доз не вызывает гибели животных.
Приведенные данные позволяют предположить, что наиболее вероятным ядом, вызывающим полинейропатию, является фосфид цинка.
Лечение
Подавляющее количество заболевших со средней и легкой степенью заболевания прошли лечение в ЦРБ. В областной токсикологический центр направляли больных с тяжелыми формами заболевания, без видимого улучшения на протяжении 3-4 дней с начала лечения. Терапию, проводимую по поводу данного заболевания, следует рассматривать как недифференцированную. Как правило, применяли глюкокортикоиды в дозе 100-150 мг в сутки, витамины группы В, берлитион по 600-1200 мг в сутки внутривенно капельно, антигистаминные препараты, детоксикационную терапию (кристаллоиды, 5% глюкозу, неогемодез 0,7 мл/кг/сутки, микроциркуляторные и энергетические плазмозаменители, реосорбилакт 0,3 мл/кг/сутки). Кроме того, назначали ненаркотические аналгетики, снотворные. При переводе в областной токсикологический центр сохраняли преемственность начатой медикаментозной терапии. Дополнительно назначали L-лизин эсцинат по 5 г 2 раза в сутки внутривенно; Эрбисол по 2 г внутримышечно вечером № 20; некоторым больным проведен плазмаферез. Ограничения в проведении плазмафереза связаны с поздними сроками поступления больных и экономическими соображениями. Всем больным с тяжелым течением полинейропатии применяли ГБО в режиме 1,25 атмосферы по 60 минут, длительность колебалась от 8 до 12 сеансов. Режимы ниже 1,25 атмосферы были малоэффективными. Сеансы проводили в барокамерах ОКА-МТ и БЛКС 3-01. Длительность курса зависела от выраженности регресса клинических проявлений. После 2-4 сеансов ГБО интенсивность болей уменьшалась, больные начинали самостоятельно передвигаться. С этого момента к терапии добавляли прозерин или галантамин, внутрисосудистую лазеротерапию № 7, ежедневно гелий-неоновым лазером АЛОУ-2 мощностью 2 мВт по 30 минут. Все больные выписаны для амбулаторного лечения после четко наметившейся тенденции к выздоровлению.
Профилактика
Методы санитарно-просветительной работы с целью профилактики данного заболевания с использованием газет, радио и телевидения не эффективны, среди заболевших преобладают лица с низкими доходами.
Об изменении традиции сбора и употребления в пищу дикорастущих грибов можно говорить только при условии улучшения благосостояния населения.
На количество заболевших может положительно повлиять упорядочение реализации и применения ядохимикатов, а также мероприятия по дератизации, категорический запрет свободной продажи таких сильнодействующих ядов, как фосфид цинка.
Выводы
Попытка исследовать частную проблему — причину возникновения полинейропатий после приема в пищу съедобных грибов, очерчивает широкий круг экологических проблем. Неразумное применение ядохимикатов приносит не только вред здоровью людей, но и значительные экономические потери, нарушает равновесие в биоценозах.
В литературе по дезинфекции, дезинсекции и дератизации приводятся сведения о значительном ущербе, наносимом мышевидными грызунами народному хозяйству. Вместе с тем, по некоторым данным, потери, связанные с элементарной бесхозяйственностью, значительно превосходят те, которые списывают на вредителей сельскохозяйственных культур (А. А. Любищев). Представляется, что нарушения в биоценозе в связи с затравкой грызунов выглядят следующим образом: погибших или заболевших грызунов и остатки приманок поедают хищные птицы, лисы, куницы и ласки, которые в естественных условиях регулируют количество грызунов в природе, а последние, не имея врагов, интенсивно размножаются. Следует думать, что упорядочение применения ядохимикатов будет способствовать природному равновесию.
|
Полинейропатия |
http://lekmed.ru/info/literatyra/polineiropatiya.html
http://humbio.ru/humbio/har_nevr/00157d94.htm
Полинейропатия (ПНП) — это заболевание всего организма со специфической реализацией патологического процесса на уровне периферической нервной системы. Множественное поражение периферических нервов представляет собой преимущественно дистальный, симметричный моторно-сенсорный процесс, связанный с экзогенной интоксикацией либо с эндогенными метаболическими нарушениями, и проявляющийся периферическими параличами, чувствительными, трофическими и вегетативно-сосудистыми расстройствами.
В основе болезненного процесса лежат дистрофические, токсические, обменные, ишемические и механические факторы, приводящие к развитию изменений соединительно-тканного интерстиция, миелиновой оболочки, осевого цилиндра. Вовлечение в процесс наряду с периферическими нервами корешков спинного мозга является маркером полирадикулонейропатии (ПРНП). Поражение же отдельных нервов в различных частях тела носит название множественный мононеврит.
http://humbio.ru/humbio/har_nevr/00157d94.htm
Полинейропатия (ПНП) — это заболевание всего организма со специфической реализацией патологического процесса на уровне периферической нервной системы. Множественное поражение периферических нервов представляет собой преимущественно дистальный, симметричный моторно-сенсорный процесс, связанный с экзогенной интоксикацией либо с эндогенными метаболическими нарушениями, и проявляющийся периферическими параличами, чувствительными, трофическими и вегетативно-сосудистыми расстройствами.
В основе болезненного процесса лежат дистрофические, токсические, обменные, ишемические и механические факторы, приводящие к развитию изменений соединительно-тканного интерстиция, миелиновой оболочки, осевого цилиндра. Вовлечение в процесс наряду с периферическими нервами корешков спинного мозга является маркером полирадикулонейропатии (ПРНП). Поражение же отдельных нервов в различных частях тела носит название множественный мононеврит.
|
Паразиты человека |
http://www.argo-shop.com.ua/library.php?id_cot=3687&full_id=267
http://glists.narod.ru/001.htm
Вирусы и микробы.
Вирусы и микробы это внутриклеточные паразиты. Мы знаем вирусы гриппа, гепатита, полиомиелита, герпеса, лимфогранулематоза, СПИДа и т.д. Вирусы и микробы могут и не воздействовать на организм человека, а могут вызвать смертельные заболевания.
Вирусы и микробы подразделяют на инфекционные, которые разрушают клетки, и опухолеродные, которые не разрушают клетки, но превращают их в опухолевые.
Инфекционные вирусы и микробы вызывают в организме человека бессимптомные (скрытые) и явные инфекции той или иной степени тяжести.
Проникают вирусы в организм через слизистые оболочки и кожу. Здоровье этих рубежей организма имеет большое значение. Чем более они ослаблены, тем более уязвим организм человека.<
Простейшие - слизевики, грибки.
Проникают простейшие в организм, как и вирусы, через кожу и слизистые оболочки. Развиваться начинают там, где имеются соответствующие условия.
Например, наличие слизи в гайморовых пазухах головы будет способствовать развитию гноеродных бактерий; сдвиг кислотно-щелочного баланса кожи в гнилостную сторону будет способствовать появлению грибковых заболеваний кожи; подавление нормальной микрофлоры дрожжами будет способствовать возникновению дисбактериозов; изменение кислой среды толстого кишечника на гнилостную будет способствовать возникновению патогенной микрофлоры, которая образует слизь, полипы и т.д.
Простейшие паразиты (хламидии) могут внедрятся в стенки кровеносных сосудов и вызывать их разрушение, инфаркт миокарда и ряд других серьезных заболеваний (воспаление половых органов, бесплодие, воспаление поджелудочной железы, печени и т.д.). Взгляните на свой язык и вы увидите белый налет - это грибы кандиды, а если они есть на языке, то и далее простираются по стенкам пищевода, кишечника и слизистых других полостей.
Чистя зубы, не пытайтесь снять налет с языка - безуспешно. И знайте, каждый раз, когда вы принимаете антибиотики, то способствуете росту этой инфекции. Токсины грибков оказывают токсическое действие на печень.
Опыт мировых паразитологов показывает, что любое заболевание всегда начинали лечить с избавлением от паразитов. Медики - паразитологи объявили сегодня патогенную микрофлору нашего организма безобидным существом, но ученые, изучающие эту проблему, доказывают обратное.
Паразитические черви - гельминты.
Локализация гельминтов в теле человека может быть весьма разнообразной. Интенсивность заражения также очень различна - от единичных экземпляров до сотен и тысяч. Число видов, одновременно паразитирующих в организме, может колебаться от 1 до 16 и больше.
Вид глистов, которые могут обитать в организме человека, может быть крайне различен.
Паразитические черви могут обитать в любой части человеческого организма: в органах (эхинококк в печени), под кожей (дракунулез), в желудочно-кишечном тракте (аскариды, острицы, цепни и т.д.).
Глисты, нематоды и огромное количество амеб (они образуют слизь) в гораздо большем количестве распространены среди населения, чем утверждает традиционная медицина. Высокая концентрация паразитов наблюдается в коммерческих свитых продуктах (бекон, ветчина, сосиски, колбасы, свиные отбивные и т.д.).
Самый быстрый способ проникновения личинок паразитов в наше организм - это зараженные продукты питания: плохо вымытые фрукты и овощи, недожаренное и недоваренное мясо. Существует еще один путь паразитического заражения - от наших домашних животных. В организме большинства животных живет несколько видов паразитов, и их яйца часто попадают в окружающую среду через испражнения животного. От испражнений они переходят в шерсть животного, и человек может заразиться, когда он гладит, обнимает или целует своего любимца или даже через воздух. Это особенно опасно для маленьких детей, которые любят своих животных, а также для беременных женщин или больных, чья иммунная система уже ослаблена.
Паразиты получают самое лучшее питание. Они потребляют все самое питательное из меню своего хозяина, оставляя ему лишь крохи. У многих людей, ведущих здоровый образ жизни и правильно питающихся, не наблюдается значительных улучшений состояния здоровья из-за наличия у них паразитов. Оздоровление организма с помощью питания, упражнений, закаливающих процедур без предварительного избавления организма от паразитов дает гораздо меньший эффект. Некоторые специалисты утверждают, что паразиты являются главной причиной тучности, поскольку они лишают организм необходимых питательных веществ, оставляя ему только пустые калории. Организм начинает требовать все больше пищи, поскольку ему не хватает витаминов и минералов.
Признаки паразитарных инвазий
Запор
Понос
Газы и вздутие
Гастрокишечный синдром
Аллергия
Проблемная кожа
Анемия
Гранулемы
Нервозность
Нарушение сна
Скрежетание зубами
Хроническая усталость
Иммунные нарушения
Онкология
Запор.
Глисты, благодаря своей форме и большим размерам, могут механически закрывать некоторые протоки, просвет кишок. Обильная глистная инвазия может закрыть общие желчные и кишечные протоки, что приводит к редким и затрудненным испражнениям.
Понос.
Ряд паразитов, особенно протозойные, производят гормоноподобные вещества, ведущие к потере натрия и хлоридов, что, в свою очередь, приводит к частым водянистым испражнениям. Таким образом, понос при паразитической инфекции является функцией паразита, а не попыткой организма избавиться от присутствующей в нем инфекции или неправильного питания.
Газы и вздутие.
Многие паразиты проживает в верхней тонкой кишке, где вызванное ими воспаление приводит к вздутию и газам. Проблема может усугубляться при потреблении трудноперевариваемых продуктов. Постоянное вздутие брюшных органов часто является признаком присутствия тайных паразитов. Эти гастрокишечные симптомы могут проявляться с переменной силой в течение долгих месяцев и даже лет, если не выгнать паразитов из организма.
Гастрокишечный синдром.
Паразиты могут раздражать и вызвать воспаление стенок кишечника, что ведет к целому ряду гастрокишечных симптомов и незначительному усвоению жизненно необходимых питательных и особенно жировых веществ. Такое малое усвоение питательных веществ ведет к твердому калу и избытку жира в кале.
Боли в суставах и мышцах. Известно, что паразиты могут перемещаться по организму человека с целью оседания в наиболее удобных для их жизни местах, например, в суставной жидкости и в мышцах. Когда это происходит, человек испытывает боли, которые часто считают следствием артрита. Боли и воспаления суставов и мышц являются также результатом травмирования тканей, причиненного некоторыми паразитами, либо иммунной реакцией организма на их присутствие.
Аллергия.
Паразиты могут раздражать, а иногда даже и пробивать оболочку кишок, что повышает риск проникновения в них крупных непереваренных молекул. Это может активизировать иммунный отклик организма в виде производства повышенных доз эозинофилов - одного из типов защитных клеток организма. Эозинофилы могут способствовать воспалению тканей организма, что приводит к аллергической реакции. Паразиты вызывают также повышенное производство организмом иммуноглобулина Е.
Проблемная кожа.
Кишечные паразиты могут вызывать крапивницу, сыпи, экзему и другие кожные реакции аллергического характера. Язвы кожи, опухоли и болячки, папилломы и дермититы могут быть результатом присутствия простейших микроорганизмов.
Анемия.
Некоторые виды кишечных глистов присасываются к слизистой оболочке кишок и высасывают питательные вещества у хозяина. Находясь в организме в большом количестве, они могут вызвать достаточно большую потерю крови, что приводит к недостатку железа (анемии). Анемию вызывает трихомонада и другие микропаразиты, которые питаются клетками крови.
Трихомонада может питаться сперматозоидами, что вызывает импотенцию.
Гранулемы.
Гранулемы - это опухолеобразные массы, обволакивающие разрушенные яйца паразитов. Чаще всего они образуются на стенках толстой и прямой кишки, но могут образовываться также в легких, печени, брюшной полости, в матке.
Нервозность.
Отходы обмена веществ и токсические вещества паразитов могут раздражать центральную нервную систему. Беспокойство и нервозность часто являются результатом систематического заражения паразитами.
Нарушение сна.
Частое пробуждение среди ночи, особенно между 2 и 3 часами ночи, тоже могут являться результатом попыток организма избавиться от токсических веществ через печень. Биоритмологически эти часы ночи управляются печению. Нарушение сна могут быть спровоцированы также ночным выходом некоторых паразитов через задний проход, что приводит к неприятным болезненным ощущениям и зуду. Одна из причин геморроя - развитие паразитов (остриц) под слизистой оболочкой прямой кишки.
Скрежетание зубами.
Бруксизм - ненормальное скрежетание зубами, сжатие зубов и трение ими часто сопровождает паразитические инфекции. Эти симптомы особенно заметны у спящих детей. Бруксизм может быть откликом нервной системы на инородный раздражитель.
Хроническая усталость.
Симптомы хронической усталости включают в себя слабость, жалобы на гриппоподобные и эмоциональные симптомы могут быть вызваны паразитами, которые создают анемию, интоксикацию, недостаток питательных веществ в организме из-за плохого всасывания белков, углеводов, жиров и особенно витаминов А и В12.
Иммунные нарушения.
Паразиты ослабляют иммунную систему, понижая выделение иммуноглобулина А. Их присутствие постоянно стимулирует реакцию системы и со временем может ослабить этот жизненно важный иммунный механизм, открывая путь проникновению в организм бактериальных и вирусных инфекций. В число ярких признаков присутствия паразитов в организме могут входить также следующие нарушения: увеличение веса, чрезмерный голод, потеря веса, плохой привкус во рту и запах изо рта, астма, диабет, эпилепсия, прыщи, мигрени и даже самые частые причины смерти: сердечные заболевания и рак.
Онкология.
Как стало теперь известно, разнообразные виды онкологических заболеваний - это "дело рук" всевозможных паразитов - от грибков и трихомонад до глистов. Американцы установили, что заболевание вызывается трематодами, достигающими головного и спинного мозга и размножающимися там.
Глисты или гельминты - черви-паразиты
Среди червей имеется большое количество (более 260 видов) паразитических форм, которые принадлежат к подтипам плоских и круглых червей. Паразитические черви издавна известны под научным термином «гельминты», в связи с чем отрасль паразитологии, изучающая их, получила название гельминтологии. С термином «гельминты» по значению совпадает слово «глисты», происходящее от латинского корня, что означает «скользкий».
Представители возбудителей паразитарных болезней относятся к царству животных. Они паразитируют на других живых существах (растения, грибы, животные), поэтому и возникла наука паразитология, занимающаяся изучением всех паразитарных организмов. Это — общая паразитология, а уже из нее выделилась гельминтология, т. е. наука, занимающаяся изучением заболеваний, вызванных паразитическими червями. Их более 260 видов, 70 из которых распространены в России. В связи с нарастающими процессами миграции народонаселения в мире в России значительно увеличивается разнообразие видов гельминтов, паразитирующих у людей. Возрастает опасность завоза глистных инвазий, не свойственных для России. К их числу относятся распространенные в странах Юго-Восточной Азии, Африки, Латинской Америки шистозомы и филляриозы.
Для развития паразитических червей обязательно нужен хозяин, т. е. то существо, организм которого является постоянным или временным местообитанием паразита и одновременно служит источником его питания. Хозяева паразитов делятся на промежуточных (в них гельминт проходит личиночные стадии) и окончательных (в них и только в них гельминт становится половозрелым, инвазионным).
По строению и форме глисты подразделяются на две группы: круглые глисты (нематоды) и плоские. Плоские глисты делятся на цестод (ленточных червей) и трематод.
Трематоды отличаются плоской листовидной формой тела и имеют одну или две присоски. Эти глисты бывают как очень маленьких размеров (1-3 мм), так и довольно крупных (более 10 см).
Цестоды - глисты обладающие удлиненным телом, похожим на ленту, состоящим из головки, шейки и отдельных члеников. Эти паразиты достигают длины более 10 м. Число члеников этих глистов колеблется от 12 до 1000.
Головкой цестода присасывается к тканям организма хозяина. За головкой тело червя сужается, это место получило название шейки. От шейки один за другим нарастают членики, постепенно увеличивая длину паразита. Старые постепенно оказываются в самом конце тела гельминта, а самый молодой членик всегда находится возле шейки.
Нематоды - глисты имеющие удлиненное тело нитевидной формы и круглое поперечное сечение. Длина нематод колеблется от 1 мм до 1 м. Изредка встречаются особи и гораздо большей - длины (8-10 м).
Особенности биологии глистов и разные пути их распространения позволяют разделить их на три следующие группы: биогельминты, геогельминты и контактные гельминты.
Гельминтологи выявили и изучили более 12 тыс. видов глистов, паразитирующих в организме животных. В человеческом организме паразитирует около 200 видов гельминтов, из них 70 видов распространены в России.
Процесс развития и роста глистов протекает по-разному. Некоторые паразитируют и в личиночной стадии, и во взрослой, не меняя хозяина (власоглавы, острицы, аскариды, карликовые цепни и др.).
Другие глисты личиночную стадию проводят в одном хозяине, а во взрослом состоянии живут в другом (бычий и свиной цепни, эхинококк и др.).
Некоторые паразиты имеют еще более сложный жизненный цикл, меняя на его протяжении трех хозяев (лентец широкий). Как правило, взрослые особи глистов живут в кишечнике, но есть и такие паразиты, которые обитают в мышцах, сердце, печени, мозгу, почках, глазах и крови человека.
Чтобы удержаться в тканях организма, глисты обладают специальными органами: присосками, плоскими крючочками или своеобразными зубами. Эти паразиты наносят сильный вред здоровью животных и человека.
Они пьют кровь и тканевые соки, поглощают из кишечника питательные вещества, которые должны были дать питание организму человека. Но это еще самый малый вред, наносимый паразитами.
Глисты при питании выделяют в организме хозяина ядовитые вещества, которые мгновенно всасываются в кровь, разносятся по тканям хозяина, воздействуя на его нервную систему и другие жизненно важные органы.
По способу заражения глисты подразделяются на две группы. К первой группе относятся паразиты (власоглавы, острицы, аскариды), которыми можно заразиться через почву, воду, овощи и другие предметы. Яйца этих гельминтов часто переносят мухи.
Во вторую группу входят глисты (трихинеллы, трематоды), заражение которыми может произойти через мясо животных и рыбу.
Собаки являются переносчиками такого опасного паразита, как эхинококк, вызывающего у человека тяжелейшее заболевание. Кроме того, от собак и кошек можно заразиться собачьими и кошачьими аскаридами, паразитирующими в личиночной стадии в организме человека.
Особенности течения глистных инвазий
Ни один орган и ни одна ткань человека не застрахованы от возможности инвазии тем или иным гельминтом, но это тогда, когда паразит уже находится в организме человека. До этого же происходит столько событий и метаморфоз, что приходится удивляться, как при этом из года в год поддерживается высокий уровень заболевания при той или иной глистной инвазии. Например, что происходит при дифиллоботриозе, вызываемом лентецом широким, или, как его еще называют, рыбьим солитером? Из яиц, для развития которых необходима водная среда, выходит личинка. Чтобы не погибнуть, она должна попасть в рачков-циклопов, которых затем поедает речная рыба — щуки, окунь, ерш, налим.
И при условии, что эта рыба будет технологически неправильно приготовлена или будет употреблена в пищу в сыром виде (например, «живая» щучья икра), а также при условии, что у данного субъекта именно в этот период и в силу каких-то причин значительно ослаблена защита организма, и происходит заражение. Не много ли условий? Более того, из головки паразита, диаметр которой соответствует диаметру спичечной головки в 1 мм, вырастает гельминт длиной до 10—15 м и более. Живет в хозяине годами, вызывая при этом различные грубые, многообразные патологические изменения, или живет там «тихо», почти себя не проявляя. Выживаемость, «непотопляемость» гельминтов обусловлена еще и тем, что существует закон большого числа яиц, когда за счет огромного количества выделяемых во внешнюю среду яиц часть из них выживает.
Не менее важны и другие свойства гельминтов, а именно:
1. например, у такого древнего гельминта, как аскарида, нужно учитывать действие ее антиэнзимов — антипепсина и антитрипсина, нарушающих процесс пищеварения. Летучие же вещества, содержащиеся во внутренней жидкости аскарид, вызывают различные по тяжести токсико-аллергические реакции: крапивницу, бронхоспазм и судороги, слезотечение и головную боль;
2. стадийность развития (яйцо, личинка, смена хозяев);
3. половое размножение, при котором происходит обмен генной информацией, а это уже высшая стадия развития, приводящая к усилению гетерогенной популяции, т. е. гельминты становятся при этом менее уязвимыми и досягаемыми, до них труднее «достучаться»;
4. большая продолжительность индивидуальной жизни (годы, а иногда столько, сколько живет хозяин паразита, под этим подразумевается и хроническое течение гельминтозов);
5. способность подавлять или видоизменять иммунный ответ хозяина, т. е. рано или поздно возникает состояние функционального иммунодефицита, а это крайне нежелательно, потому что создаются почти идеальные условия для проникновения любых патогенных агентов экзогенным путем, а также условия для «растормаживания» эндогенных очагов инфекции, если таковые имелись ранее (что, к сожалению, часто бывает) и «дремали», сдерживаемые иммунной системой;
6. присутствие того или иного гельминта иммунный ответ слабый и нестойкий, а значит, практически отсутствуют методы иммунопрофилактики;
7. широчайшее распространение, множество сред обитания (вода, почва, воздух, растения и т. д.);
8. способность яиц длительно сохраняться во внешней среде (годами).
Эти свойства позволяют тому или иному виду выживать в казалось бы «нечеловеческих условиях»: запредельно высокая (за 50 °С) или низкая (до — 35 —40 °С) температура, стойкая влажность или сухость, отсутствие «средств к существованию» — пищи, воздуха, тепла. И тем не менее, при определенных условиях происходит развитие, созревание, появляются признаки инвазивности.
Уровень заболеваемости гельминтозами в мире крайне высок: из почти 6 миллиардов людей, живущих сейчас на планете, 4 миллиарда поражены тем или иным видом гельминтоза, а если учесть тот факт, что многие из них являются «носителями» сразу нескольких паразитов, то картина станет еще более впечатляющей.
Человек со своим мощным набором компенсаторно-приспособительных реакций, иммунной системой, различными неспецифическими защитными барьерами не может не реагировать на присутствие гельминта, хотя иногда и отмечается почти бессимптомное течение гельминтозов. Но это бывает крайне редко, а чаще всего можно выявить следующее:
1. различные токсико-аллергические реакции, чаще кожные. Более того, если причина таких реакций остается невыявленной, а клинические проявления имеют место, то в первую очередь необходимо тщательное обследование на наличие глистной инвазии;
2. нервно-психические расстройства. Они обусловлены глистной инвазией, при которой в кровь постоянно поступают токсические вещества, поддерживая определенный уровень токсина, приводящий к раздражительности, эмоциональной лабильности, «немотивированным» вспышкам гнева, потере концентрации внимания, усидчивости, быстрой утомляемости, расстройству сна. Характерна нарастающая общая слабость. Один из пациентов, спортсмен, жаловался, что у него «нет сил пожать руку товарищу при встрече»;
3. диспептический синдром многообразен, от эфемерной до манифестной симптоматики, включающей в себя и дискомфорт, и боль в животе, зачастую редкой локализации и разной интенсивности, и урчание, и вздутие, и чувство распирания в животе; изменение аппетита как в сторону повышения (одна из причин необращения к врачу — «аппетит хороший, значит, я здоров»), так и значительного понижения аппетита вплоть до анорексии; расстройства стула от запоров до поносов; развитие многофакторных глубоких дисбактериозов;
4. многие гельминты питаются кровью хозяина, являясь гемофагами, поглощают витамин B12 и нарушают процесс всасывания антианемического вещества в тонкой кишке, повреждают слизистую оболочку кишечника, хотя и неглубоко, но на большой площади. Все это приводит к хронической потере крови и в ряде случаев, к развитию анемии (малокровию). Здесь необходимо учитывать и угнетающее воздействие токсинов на органы кроветворения, что также немаловажно при развитии анемии. При гельминтозах часто выявляется повышенное содержание эозинофилов (лейкоцитарные клетки, активно участвующие в аллергических реакциях);
5. наличие глистной инвазии, при условии развития анемии, особенно у детей, может привести к задержке роста и физическому недоразвитию, даже при повышенном аппетите;
6. у детей во время проведения плановых прививок нередко отмечаются различные поствакцинальные токсико-аллергические реакции;
7. гельминтозы часто провоцируют обострение хронических заболеваний, при этом местонахождение гельминта и месторасположение заинтересованного органа могут быть абсолютно различны по локализации;
8. иногда, хотя не очень часто (возможно, здесь срабатывает принцип, что «любому паразиту не выгодно уничтожать свою жертву, иначе ему не на ком будет паразитировать, лишившись в одночасье и крова, и пищи»), возникают несовместимые с жизнью хозяина условия, например при эхинококкозе печени, финнозе головного мозга. Необходимо отметить, что даже патогенность гельминтов колеблется в широких пределах в зависимости от объекта паразитизма. Например, для человека эхинококк крайне опасен, а крупный рогатый скот многие годы благополучно живет с органами, проросшими эхинококковыми пузырями, достигающими массы в несколько килограммов.
Рассмотрев основные общие для всех гельминтов черты, необходимо дать характеристику различным подтипам паразитических червей, а также выявить принципиальные различия, которые имеют большое значение в диагностике и в выборе методов лечения при гельминтозах.
Гельминты в организме человека не размножаются, за исключением таких видов, как острица, цепень карликовый. Попадает гельминт в организм в виде яиц или личинок. Прямого заражения людей, пораженных гельминтами, не происходит, кроме тех, которые являются контагиозными (гимонолепидоз, энтеробиоз).
Заражение же остальными гельминтозами происходит либо через почву (грязные руки — кишечник — аскаридоз), либо при контакте кожи с почвой (стронгилоидоз) или водой (шистосомоз), либо при приеме пищи (тениаринхоз, дифиллоботриоз).
В организме гельминты обитают в различных органах и тканях: в кишечнике — аскариды, острицы, цепни, лентецы; в печени — эхинококки, описторхи; в мышцах — трихинеллы; в легких— парагонимус, в крови — филярии, шистосомы.
Сосальщики - плоские черви-паразиты
К плоским червям относятся такие представители, как сосальщики.
Все виды гельминтов этого типа имеют сплющенное тело языкообразной или листовидной формы. У плоских червей хорошо развиты пищеварительная, нервная, выделительная и половая системы, кровеносная и дыхательная отсутствуют.
Пищеварительная система гельминтов-сосальшиков состоит из рта, глотки, пищевода и двух кишечных каналов. В кишечнике происходит переваривание и всасывание пищи. Анальное отверстие отсутствует, а непереваренные остатки пищи выбрасываются через рот. У ленточных гельминтов пищеварительная система отсутствует.
Сосальщики, или трематоды, имеют одну присоску на переднем конце тела (в глубине присоскипредставитель класса сосальщиков - ланцетовидный сосальщик находится рот), вторую — на животе (у подкласса двуусток).
Существует вид сосальщиков, у которых много присосок иди на заднем конце тела имеется целый диск для присасывания (многоустки).
Сосальщики питаются содержимым кишечника хозяина, кровью, слизью, эпителием. Пищеварение у них внеклеточное, ферментативное. Органом выделения является богато развитая водоносная система. Прогоняемая с помощью ресничек вода вымывает экскреторные продукты из выделительных каналов.
Кровеносная система и органы дыхания у сосальщиков отсутствуют, равно как и органы чувств.
Нервная система состоит из двух нервных узлов, расположенных на переднем конце тела, и отходящих от них нервных стволов. К органам чувств относятся нервные окончания (сенсиллы).
Самки и самцы плоских червей имеют сложную половую систему. Паразиты человека представлены классом сосальщиков и классом ленточных червей.
Подавляющее большинство представителей являются гермафродитами, кроме кровеносных сосальщиков (шистосомы) — они раздельнополы. Яйца сосальщиков от светло-желтого до темно-коричневого цвета, на одном из полюсов имеется крышечка. При исследовании яйца обнаруживаются в дуоденальном содержимом, кале, моче, мокроте.
Первым промежуточным хозяином у сосальщиков являются различные моллюски, вторым хозяином служат рыбы, земноводные. Окончательным хозяином являются различные позвоночные.
Жизненный цикл многоусток предельно прост: из яйца, покинув рыбу, выходит личинка, которая через небольшой отрезок времени вновь присасывается к рыбе и превращается во взрослого червя. Двуустки имеют более сложный цикл развития, меняя 2-3 хозяев.
Взрослые сосальщики паразитируют в самых разнообразных органах, таких как кишечник, печень, легкие, мочевой пузырь и даже в таких редких местах обитания, как евстахиева труба или конъюнктивальный мешок.
Плоскими червями-сосальщиками можно заразиться при употреблении в пищу сырой и непрожаренной рыбы, а также раков. Они могут паразитировать в выводных протоках разных органов, присасываясь к их стенкам.
Размеры сосальщиков бывают от 1 мм до 1,5 м.
Название гельминтам было дано не совсем точное, так как они ничего не высасывают из организма, но вред наносят огромный.
Ленточные черви-паразиты
К плоским червям относится и другой класс — это ленточные черви, которые, в свою очередь, подразделяются на отряды лентецов и цепней.
Эти черви отличаются от круглых червей тем, что имеют промежуточного хозяина, в организме которого развиваются их личинки. Как правило, промежуточными хозяевами становятся рыбы и животные.
Ленточные черви в половозрелом состоянии являются обитателями кишечника позвоночных. На переднем конце тела имеется головка — сколекс, являющаяся органом прикрепления, позади нее — зона роста; тело подразделяется на членики, или проглоттиды. Гермафродит. Кишечник редуцирован.
В связи с этим питание осуществляется всей поверхностью тела паразита пищей, переваренной кишечником хозяина (эндосмотическое питание). Такая среда обитания, как тонкая кишка, подразумевает, что здесь переварится любой подходящий для этого субстрат, но цестоды имеют специфические антиферментные свойства, позволяющие им выживать в условиях высокой ферментной активности. Доказано, что многие гельминты в норме выделяют в течение жизни антикиназу, которая нейтрализует панкреатический сок и тем самым защищает гельминтов от переваривания.
Развитых органов чувств у цестод нет, но имеются чувствительные клетки, пронизывающие своими периферическими отростками поверхность тела паразита. Органы дыхания и кровеносная система отсутствуют.
В мясе рыбы и животных, пораженном ленточными гельминтами, находятся небольшие пузырьки с личинками паразитов. При употреблении зараженных продуктов личинки попадают в организм постоянного хозяина и остаются в кишечнике. Здесь они завершают свое развитие и становятся взрослыми особями.
Наряду со схожими чертами, присущими ленточным червям, имеются и существенные различия между лентецами и цепнями. Это особенно важно в диагностическом плане, когда необходимо проводить идентификацию паразитов.
Для лентецов характерна головка — сколекс с двумя присасывательными ямками или бороздками — ботриями или только с одной ямкой на переднем конце паразита. Матка имеет свое собственное отверстие, что значит, что яйца будут выделяться во внешнюю среду и могут быть обнаружены при исследовании испражнений; яйца с крышечкой.
членики (проглоттиды) цепняЦепни получили свое название из-за внешнего вида. Их характерным внешним признаком является лентовидное тело, разделенное на членики (проглоттиды). Размеры паразитов варьируются от 1 мм до 18 м в длину.
У цепней головка с четырьмя присосками, с помощью которых черви прикрепляются к стенкам кишечника. Далее следует зона роста, или шейка, от которой берут начало членики. По мере роста шейки на ней возникает отчетливая поперечная перетяжка, отделяющая задний участок, превращающийся в проглоттиду.
Матка не имеет выводного отверстия, а значит, яиц в испражнениях обнаружить практически не удается; яйца без крышечки.
При росте гельминта новые членики постепенно отодвигают назад ранее образованные. Таким образом, в передней части тела находятся самые молодые членики, а на конце — старые, самые зрелые.
В процессе перемещения члеников дальше от шейки происходит их созревание, изменяется их форма и внутреннее строение. Молодые членики — самые мелкие. Постепенно их размеры увеличиваются, изменяется их половая система, которой совсем лишены молодые, только что образованные членики. Множество члеников, соединенных друг с другом, напоминают цепочку, в которой может быть от 3 до нескольких тысяч члеников.
Замыкающие цепочку членики содержат яйца паразита, которые по мере созревания постепенно отрываются и выходят наружу. С помощью покрывающих их ресничек яйца передвигаются по кишечнику и через задний проход попадают в окружающую среду.
Как уже говорилось, пищеварительная система у ленточных гельминтов отсутствует, они поглощают пищу всей поверхностью тела.
Ученые объясняют это тем, что цепни паразитируют в тонком кишечнике, где находится уже переваренная и готовая к усвоению пища. Дыхательная и кровеносная системы также отсутствуют, а выделительная и нервная имеют типичное строение.
Характерной особенностью половой системы ленточных червей является многократное повторение мужских и женских половых органов в каждом членике. Благодаря такому строению паразиты обладают колоссальной плодовитостью.
Жизненный цикл ленточных червей протекает со сменой хозяев и с личиночными стадиями. Постоянными хозяевами являются позвоночные животные и человек, а промежуточными — позвоночные и беспозвоночные.
http://glists.narod.ru/001.htm
Вирусы и микробы.
Вирусы и микробы это внутриклеточные паразиты. Мы знаем вирусы гриппа, гепатита, полиомиелита, герпеса, лимфогранулематоза, СПИДа и т.д. Вирусы и микробы могут и не воздействовать на организм человека, а могут вызвать смертельные заболевания.
Вирусы и микробы подразделяют на инфекционные, которые разрушают клетки, и опухолеродные, которые не разрушают клетки, но превращают их в опухолевые.
Инфекционные вирусы и микробы вызывают в организме человека бессимптомные (скрытые) и явные инфекции той или иной степени тяжести.
Проникают вирусы в организм через слизистые оболочки и кожу. Здоровье этих рубежей организма имеет большое значение. Чем более они ослаблены, тем более уязвим организм человека.<
Простейшие - слизевики, грибки.
Проникают простейшие в организм, как и вирусы, через кожу и слизистые оболочки. Развиваться начинают там, где имеются соответствующие условия.
Например, наличие слизи в гайморовых пазухах головы будет способствовать развитию гноеродных бактерий; сдвиг кислотно-щелочного баланса кожи в гнилостную сторону будет способствовать появлению грибковых заболеваний кожи; подавление нормальной микрофлоры дрожжами будет способствовать возникновению дисбактериозов; изменение кислой среды толстого кишечника на гнилостную будет способствовать возникновению патогенной микрофлоры, которая образует слизь, полипы и т.д.
Простейшие паразиты (хламидии) могут внедрятся в стенки кровеносных сосудов и вызывать их разрушение, инфаркт миокарда и ряд других серьезных заболеваний (воспаление половых органов, бесплодие, воспаление поджелудочной железы, печени и т.д.). Взгляните на свой язык и вы увидите белый налет - это грибы кандиды, а если они есть на языке, то и далее простираются по стенкам пищевода, кишечника и слизистых других полостей.
Чистя зубы, не пытайтесь снять налет с языка - безуспешно. И знайте, каждый раз, когда вы принимаете антибиотики, то способствуете росту этой инфекции. Токсины грибков оказывают токсическое действие на печень.
Опыт мировых паразитологов показывает, что любое заболевание всегда начинали лечить с избавлением от паразитов. Медики - паразитологи объявили сегодня патогенную микрофлору нашего организма безобидным существом, но ученые, изучающие эту проблему, доказывают обратное.
Паразитические черви - гельминты.
Локализация гельминтов в теле человека может быть весьма разнообразной. Интенсивность заражения также очень различна - от единичных экземпляров до сотен и тысяч. Число видов, одновременно паразитирующих в организме, может колебаться от 1 до 16 и больше.
Вид глистов, которые могут обитать в организме человека, может быть крайне различен.
Паразитические черви могут обитать в любой части человеческого организма: в органах (эхинококк в печени), под кожей (дракунулез), в желудочно-кишечном тракте (аскариды, острицы, цепни и т.д.).
Глисты, нематоды и огромное количество амеб (они образуют слизь) в гораздо большем количестве распространены среди населения, чем утверждает традиционная медицина. Высокая концентрация паразитов наблюдается в коммерческих свитых продуктах (бекон, ветчина, сосиски, колбасы, свиные отбивные и т.д.).
Самый быстрый способ проникновения личинок паразитов в наше организм - это зараженные продукты питания: плохо вымытые фрукты и овощи, недожаренное и недоваренное мясо. Существует еще один путь паразитического заражения - от наших домашних животных. В организме большинства животных живет несколько видов паразитов, и их яйца часто попадают в окружающую среду через испражнения животного. От испражнений они переходят в шерсть животного, и человек может заразиться, когда он гладит, обнимает или целует своего любимца или даже через воздух. Это особенно опасно для маленьких детей, которые любят своих животных, а также для беременных женщин или больных, чья иммунная система уже ослаблена.
Паразиты получают самое лучшее питание. Они потребляют все самое питательное из меню своего хозяина, оставляя ему лишь крохи. У многих людей, ведущих здоровый образ жизни и правильно питающихся, не наблюдается значительных улучшений состояния здоровья из-за наличия у них паразитов. Оздоровление организма с помощью питания, упражнений, закаливающих процедур без предварительного избавления организма от паразитов дает гораздо меньший эффект. Некоторые специалисты утверждают, что паразиты являются главной причиной тучности, поскольку они лишают организм необходимых питательных веществ, оставляя ему только пустые калории. Организм начинает требовать все больше пищи, поскольку ему не хватает витаминов и минералов.
Признаки паразитарных инвазий
Запор
Понос
Газы и вздутие
Гастрокишечный синдром
Аллергия
Проблемная кожа
Анемия
Гранулемы
Нервозность
Нарушение сна
Скрежетание зубами
Хроническая усталость
Иммунные нарушения
Онкология
Запор.
Глисты, благодаря своей форме и большим размерам, могут механически закрывать некоторые протоки, просвет кишок. Обильная глистная инвазия может закрыть общие желчные и кишечные протоки, что приводит к редким и затрудненным испражнениям.
Понос.
Ряд паразитов, особенно протозойные, производят гормоноподобные вещества, ведущие к потере натрия и хлоридов, что, в свою очередь, приводит к частым водянистым испражнениям. Таким образом, понос при паразитической инфекции является функцией паразита, а не попыткой организма избавиться от присутствующей в нем инфекции или неправильного питания.
Газы и вздутие.
Многие паразиты проживает в верхней тонкой кишке, где вызванное ими воспаление приводит к вздутию и газам. Проблема может усугубляться при потреблении трудноперевариваемых продуктов. Постоянное вздутие брюшных органов часто является признаком присутствия тайных паразитов. Эти гастрокишечные симптомы могут проявляться с переменной силой в течение долгих месяцев и даже лет, если не выгнать паразитов из организма.
Гастрокишечный синдром.
Паразиты могут раздражать и вызвать воспаление стенок кишечника, что ведет к целому ряду гастрокишечных симптомов и незначительному усвоению жизненно необходимых питательных и особенно жировых веществ. Такое малое усвоение питательных веществ ведет к твердому калу и избытку жира в кале.
Боли в суставах и мышцах. Известно, что паразиты могут перемещаться по организму человека с целью оседания в наиболее удобных для их жизни местах, например, в суставной жидкости и в мышцах. Когда это происходит, человек испытывает боли, которые часто считают следствием артрита. Боли и воспаления суставов и мышц являются также результатом травмирования тканей, причиненного некоторыми паразитами, либо иммунной реакцией организма на их присутствие.
Аллергия.
Паразиты могут раздражать, а иногда даже и пробивать оболочку кишок, что повышает риск проникновения в них крупных непереваренных молекул. Это может активизировать иммунный отклик организма в виде производства повышенных доз эозинофилов - одного из типов защитных клеток организма. Эозинофилы могут способствовать воспалению тканей организма, что приводит к аллергической реакции. Паразиты вызывают также повышенное производство организмом иммуноглобулина Е.
Проблемная кожа.
Кишечные паразиты могут вызывать крапивницу, сыпи, экзему и другие кожные реакции аллергического характера. Язвы кожи, опухоли и болячки, папилломы и дермититы могут быть результатом присутствия простейших микроорганизмов.
Анемия.
Некоторые виды кишечных глистов присасываются к слизистой оболочке кишок и высасывают питательные вещества у хозяина. Находясь в организме в большом количестве, они могут вызвать достаточно большую потерю крови, что приводит к недостатку железа (анемии). Анемию вызывает трихомонада и другие микропаразиты, которые питаются клетками крови.
Трихомонада может питаться сперматозоидами, что вызывает импотенцию.
Гранулемы.
Гранулемы - это опухолеобразные массы, обволакивающие разрушенные яйца паразитов. Чаще всего они образуются на стенках толстой и прямой кишки, но могут образовываться также в легких, печени, брюшной полости, в матке.
Нервозность.
Отходы обмена веществ и токсические вещества паразитов могут раздражать центральную нервную систему. Беспокойство и нервозность часто являются результатом систематического заражения паразитами.
Нарушение сна.
Частое пробуждение среди ночи, особенно между 2 и 3 часами ночи, тоже могут являться результатом попыток организма избавиться от токсических веществ через печень. Биоритмологически эти часы ночи управляются печению. Нарушение сна могут быть спровоцированы также ночным выходом некоторых паразитов через задний проход, что приводит к неприятным болезненным ощущениям и зуду. Одна из причин геморроя - развитие паразитов (остриц) под слизистой оболочкой прямой кишки.
Скрежетание зубами.
Бруксизм - ненормальное скрежетание зубами, сжатие зубов и трение ими часто сопровождает паразитические инфекции. Эти симптомы особенно заметны у спящих детей. Бруксизм может быть откликом нервной системы на инородный раздражитель.
Хроническая усталость.
Симптомы хронической усталости включают в себя слабость, жалобы на гриппоподобные и эмоциональные симптомы могут быть вызваны паразитами, которые создают анемию, интоксикацию, недостаток питательных веществ в организме из-за плохого всасывания белков, углеводов, жиров и особенно витаминов А и В12.
Иммунные нарушения.
Паразиты ослабляют иммунную систему, понижая выделение иммуноглобулина А. Их присутствие постоянно стимулирует реакцию системы и со временем может ослабить этот жизненно важный иммунный механизм, открывая путь проникновению в организм бактериальных и вирусных инфекций. В число ярких признаков присутствия паразитов в организме могут входить также следующие нарушения: увеличение веса, чрезмерный голод, потеря веса, плохой привкус во рту и запах изо рта, астма, диабет, эпилепсия, прыщи, мигрени и даже самые частые причины смерти: сердечные заболевания и рак.
Онкология.
Как стало теперь известно, разнообразные виды онкологических заболеваний - это "дело рук" всевозможных паразитов - от грибков и трихомонад до глистов. Американцы установили, что заболевание вызывается трематодами, достигающими головного и спинного мозга и размножающимися там.
Глисты или гельминты - черви-паразиты
Среди червей имеется большое количество (более 260 видов) паразитических форм, которые принадлежат к подтипам плоских и круглых червей. Паразитические черви издавна известны под научным термином «гельминты», в связи с чем отрасль паразитологии, изучающая их, получила название гельминтологии. С термином «гельминты» по значению совпадает слово «глисты», происходящее от латинского корня, что означает «скользкий».
Представители возбудителей паразитарных болезней относятся к царству животных. Они паразитируют на других живых существах (растения, грибы, животные), поэтому и возникла наука паразитология, занимающаяся изучением всех паразитарных организмов. Это — общая паразитология, а уже из нее выделилась гельминтология, т. е. наука, занимающаяся изучением заболеваний, вызванных паразитическими червями. Их более 260 видов, 70 из которых распространены в России. В связи с нарастающими процессами миграции народонаселения в мире в России значительно увеличивается разнообразие видов гельминтов, паразитирующих у людей. Возрастает опасность завоза глистных инвазий, не свойственных для России. К их числу относятся распространенные в странах Юго-Восточной Азии, Африки, Латинской Америки шистозомы и филляриозы.
Для развития паразитических червей обязательно нужен хозяин, т. е. то существо, организм которого является постоянным или временным местообитанием паразита и одновременно служит источником его питания. Хозяева паразитов делятся на промежуточных (в них гельминт проходит личиночные стадии) и окончательных (в них и только в них гельминт становится половозрелым, инвазионным).
По строению и форме глисты подразделяются на две группы: круглые глисты (нематоды) и плоские. Плоские глисты делятся на цестод (ленточных червей) и трематод.
Трематоды отличаются плоской листовидной формой тела и имеют одну или две присоски. Эти глисты бывают как очень маленьких размеров (1-3 мм), так и довольно крупных (более 10 см).
Цестоды - глисты обладающие удлиненным телом, похожим на ленту, состоящим из головки, шейки и отдельных члеников. Эти паразиты достигают длины более 10 м. Число члеников этих глистов колеблется от 12 до 1000.
Головкой цестода присасывается к тканям организма хозяина. За головкой тело червя сужается, это место получило название шейки. От шейки один за другим нарастают членики, постепенно увеличивая длину паразита. Старые постепенно оказываются в самом конце тела гельминта, а самый молодой членик всегда находится возле шейки.
Нематоды - глисты имеющие удлиненное тело нитевидной формы и круглое поперечное сечение. Длина нематод колеблется от 1 мм до 1 м. Изредка встречаются особи и гораздо большей - длины (8-10 м).
Особенности биологии глистов и разные пути их распространения позволяют разделить их на три следующие группы: биогельминты, геогельминты и контактные гельминты.
Гельминтологи выявили и изучили более 12 тыс. видов глистов, паразитирующих в организме животных. В человеческом организме паразитирует около 200 видов гельминтов, из них 70 видов распространены в России.
Процесс развития и роста глистов протекает по-разному. Некоторые паразитируют и в личиночной стадии, и во взрослой, не меняя хозяина (власоглавы, острицы, аскариды, карликовые цепни и др.).
Другие глисты личиночную стадию проводят в одном хозяине, а во взрослом состоянии живут в другом (бычий и свиной цепни, эхинококк и др.).
Некоторые паразиты имеют еще более сложный жизненный цикл, меняя на его протяжении трех хозяев (лентец широкий). Как правило, взрослые особи глистов живут в кишечнике, но есть и такие паразиты, которые обитают в мышцах, сердце, печени, мозгу, почках, глазах и крови человека.
Чтобы удержаться в тканях организма, глисты обладают специальными органами: присосками, плоскими крючочками или своеобразными зубами. Эти паразиты наносят сильный вред здоровью животных и человека.
Они пьют кровь и тканевые соки, поглощают из кишечника питательные вещества, которые должны были дать питание организму человека. Но это еще самый малый вред, наносимый паразитами.
Глисты при питании выделяют в организме хозяина ядовитые вещества, которые мгновенно всасываются в кровь, разносятся по тканям хозяина, воздействуя на его нервную систему и другие жизненно важные органы.
По способу заражения глисты подразделяются на две группы. К первой группе относятся паразиты (власоглавы, острицы, аскариды), которыми можно заразиться через почву, воду, овощи и другие предметы. Яйца этих гельминтов часто переносят мухи.
Во вторую группу входят глисты (трихинеллы, трематоды), заражение которыми может произойти через мясо животных и рыбу.
Собаки являются переносчиками такого опасного паразита, как эхинококк, вызывающего у человека тяжелейшее заболевание. Кроме того, от собак и кошек можно заразиться собачьими и кошачьими аскаридами, паразитирующими в личиночной стадии в организме человека.
Особенности течения глистных инвазий
Ни один орган и ни одна ткань человека не застрахованы от возможности инвазии тем или иным гельминтом, но это тогда, когда паразит уже находится в организме человека. До этого же происходит столько событий и метаморфоз, что приходится удивляться, как при этом из года в год поддерживается высокий уровень заболевания при той или иной глистной инвазии. Например, что происходит при дифиллоботриозе, вызываемом лентецом широким, или, как его еще называют, рыбьим солитером? Из яиц, для развития которых необходима водная среда, выходит личинка. Чтобы не погибнуть, она должна попасть в рачков-циклопов, которых затем поедает речная рыба — щуки, окунь, ерш, налим.
И при условии, что эта рыба будет технологически неправильно приготовлена или будет употреблена в пищу в сыром виде (например, «живая» щучья икра), а также при условии, что у данного субъекта именно в этот период и в силу каких-то причин значительно ослаблена защита организма, и происходит заражение. Не много ли условий? Более того, из головки паразита, диаметр которой соответствует диаметру спичечной головки в 1 мм, вырастает гельминт длиной до 10—15 м и более. Живет в хозяине годами, вызывая при этом различные грубые, многообразные патологические изменения, или живет там «тихо», почти себя не проявляя. Выживаемость, «непотопляемость» гельминтов обусловлена еще и тем, что существует закон большого числа яиц, когда за счет огромного количества выделяемых во внешнюю среду яиц часть из них выживает.
Не менее важны и другие свойства гельминтов, а именно:
1. например, у такого древнего гельминта, как аскарида, нужно учитывать действие ее антиэнзимов — антипепсина и антитрипсина, нарушающих процесс пищеварения. Летучие же вещества, содержащиеся во внутренней жидкости аскарид, вызывают различные по тяжести токсико-аллергические реакции: крапивницу, бронхоспазм и судороги, слезотечение и головную боль;
2. стадийность развития (яйцо, личинка, смена хозяев);
3. половое размножение, при котором происходит обмен генной информацией, а это уже высшая стадия развития, приводящая к усилению гетерогенной популяции, т. е. гельминты становятся при этом менее уязвимыми и досягаемыми, до них труднее «достучаться»;
4. большая продолжительность индивидуальной жизни (годы, а иногда столько, сколько живет хозяин паразита, под этим подразумевается и хроническое течение гельминтозов);
5. способность подавлять или видоизменять иммунный ответ хозяина, т. е. рано или поздно возникает состояние функционального иммунодефицита, а это крайне нежелательно, потому что создаются почти идеальные условия для проникновения любых патогенных агентов экзогенным путем, а также условия для «растормаживания» эндогенных очагов инфекции, если таковые имелись ранее (что, к сожалению, часто бывает) и «дремали», сдерживаемые иммунной системой;
6. присутствие того или иного гельминта иммунный ответ слабый и нестойкий, а значит, практически отсутствуют методы иммунопрофилактики;
7. широчайшее распространение, множество сред обитания (вода, почва, воздух, растения и т. д.);
8. способность яиц длительно сохраняться во внешней среде (годами).
Эти свойства позволяют тому или иному виду выживать в казалось бы «нечеловеческих условиях»: запредельно высокая (за 50 °С) или низкая (до — 35 —40 °С) температура, стойкая влажность или сухость, отсутствие «средств к существованию» — пищи, воздуха, тепла. И тем не менее, при определенных условиях происходит развитие, созревание, появляются признаки инвазивности.
Уровень заболеваемости гельминтозами в мире крайне высок: из почти 6 миллиардов людей, живущих сейчас на планете, 4 миллиарда поражены тем или иным видом гельминтоза, а если учесть тот факт, что многие из них являются «носителями» сразу нескольких паразитов, то картина станет еще более впечатляющей.
Человек со своим мощным набором компенсаторно-приспособительных реакций, иммунной системой, различными неспецифическими защитными барьерами не может не реагировать на присутствие гельминта, хотя иногда и отмечается почти бессимптомное течение гельминтозов. Но это бывает крайне редко, а чаще всего можно выявить следующее:
1. различные токсико-аллергические реакции, чаще кожные. Более того, если причина таких реакций остается невыявленной, а клинические проявления имеют место, то в первую очередь необходимо тщательное обследование на наличие глистной инвазии;
2. нервно-психические расстройства. Они обусловлены глистной инвазией, при которой в кровь постоянно поступают токсические вещества, поддерживая определенный уровень токсина, приводящий к раздражительности, эмоциональной лабильности, «немотивированным» вспышкам гнева, потере концентрации внимания, усидчивости, быстрой утомляемости, расстройству сна. Характерна нарастающая общая слабость. Один из пациентов, спортсмен, жаловался, что у него «нет сил пожать руку товарищу при встрече»;
3. диспептический синдром многообразен, от эфемерной до манифестной симптоматики, включающей в себя и дискомфорт, и боль в животе, зачастую редкой локализации и разной интенсивности, и урчание, и вздутие, и чувство распирания в животе; изменение аппетита как в сторону повышения (одна из причин необращения к врачу — «аппетит хороший, значит, я здоров»), так и значительного понижения аппетита вплоть до анорексии; расстройства стула от запоров до поносов; развитие многофакторных глубоких дисбактериозов;
4. многие гельминты питаются кровью хозяина, являясь гемофагами, поглощают витамин B12 и нарушают процесс всасывания антианемического вещества в тонкой кишке, повреждают слизистую оболочку кишечника, хотя и неглубоко, но на большой площади. Все это приводит к хронической потере крови и в ряде случаев, к развитию анемии (малокровию). Здесь необходимо учитывать и угнетающее воздействие токсинов на органы кроветворения, что также немаловажно при развитии анемии. При гельминтозах часто выявляется повышенное содержание эозинофилов (лейкоцитарные клетки, активно участвующие в аллергических реакциях);
5. наличие глистной инвазии, при условии развития анемии, особенно у детей, может привести к задержке роста и физическому недоразвитию, даже при повышенном аппетите;
6. у детей во время проведения плановых прививок нередко отмечаются различные поствакцинальные токсико-аллергические реакции;
7. гельминтозы часто провоцируют обострение хронических заболеваний, при этом местонахождение гельминта и месторасположение заинтересованного органа могут быть абсолютно различны по локализации;
8. иногда, хотя не очень часто (возможно, здесь срабатывает принцип, что «любому паразиту не выгодно уничтожать свою жертву, иначе ему не на ком будет паразитировать, лишившись в одночасье и крова, и пищи»), возникают несовместимые с жизнью хозяина условия, например при эхинококкозе печени, финнозе головного мозга. Необходимо отметить, что даже патогенность гельминтов колеблется в широких пределах в зависимости от объекта паразитизма. Например, для человека эхинококк крайне опасен, а крупный рогатый скот многие годы благополучно живет с органами, проросшими эхинококковыми пузырями, достигающими массы в несколько килограммов.
Рассмотрев основные общие для всех гельминтов черты, необходимо дать характеристику различным подтипам паразитических червей, а также выявить принципиальные различия, которые имеют большое значение в диагностике и в выборе методов лечения при гельминтозах.
Гельминты в организме человека не размножаются, за исключением таких видов, как острица, цепень карликовый. Попадает гельминт в организм в виде яиц или личинок. Прямого заражения людей, пораженных гельминтами, не происходит, кроме тех, которые являются контагиозными (гимонолепидоз, энтеробиоз).
Заражение же остальными гельминтозами происходит либо через почву (грязные руки — кишечник — аскаридоз), либо при контакте кожи с почвой (стронгилоидоз) или водой (шистосомоз), либо при приеме пищи (тениаринхоз, дифиллоботриоз).
В организме гельминты обитают в различных органах и тканях: в кишечнике — аскариды, острицы, цепни, лентецы; в печени — эхинококки, описторхи; в мышцах — трихинеллы; в легких— парагонимус, в крови — филярии, шистосомы.
Сосальщики - плоские черви-паразиты
К плоским червям относятся такие представители, как сосальщики.
Все виды гельминтов этого типа имеют сплющенное тело языкообразной или листовидной формы. У плоских червей хорошо развиты пищеварительная, нервная, выделительная и половая системы, кровеносная и дыхательная отсутствуют.
Пищеварительная система гельминтов-сосальшиков состоит из рта, глотки, пищевода и двух кишечных каналов. В кишечнике происходит переваривание и всасывание пищи. Анальное отверстие отсутствует, а непереваренные остатки пищи выбрасываются через рот. У ленточных гельминтов пищеварительная система отсутствует.
Сосальщики, или трематоды, имеют одну присоску на переднем конце тела (в глубине присоскипредставитель класса сосальщиков - ланцетовидный сосальщик находится рот), вторую — на животе (у подкласса двуусток).
Существует вид сосальщиков, у которых много присосок иди на заднем конце тела имеется целый диск для присасывания (многоустки).
Сосальщики питаются содержимым кишечника хозяина, кровью, слизью, эпителием. Пищеварение у них внеклеточное, ферментативное. Органом выделения является богато развитая водоносная система. Прогоняемая с помощью ресничек вода вымывает экскреторные продукты из выделительных каналов.
Кровеносная система и органы дыхания у сосальщиков отсутствуют, равно как и органы чувств.
Нервная система состоит из двух нервных узлов, расположенных на переднем конце тела, и отходящих от них нервных стволов. К органам чувств относятся нервные окончания (сенсиллы).
Самки и самцы плоских червей имеют сложную половую систему. Паразиты человека представлены классом сосальщиков и классом ленточных червей.
Подавляющее большинство представителей являются гермафродитами, кроме кровеносных сосальщиков (шистосомы) — они раздельнополы. Яйца сосальщиков от светло-желтого до темно-коричневого цвета, на одном из полюсов имеется крышечка. При исследовании яйца обнаруживаются в дуоденальном содержимом, кале, моче, мокроте.
Первым промежуточным хозяином у сосальщиков являются различные моллюски, вторым хозяином служат рыбы, земноводные. Окончательным хозяином являются различные позвоночные.
Жизненный цикл многоусток предельно прост: из яйца, покинув рыбу, выходит личинка, которая через небольшой отрезок времени вновь присасывается к рыбе и превращается во взрослого червя. Двуустки имеют более сложный цикл развития, меняя 2-3 хозяев.
Взрослые сосальщики паразитируют в самых разнообразных органах, таких как кишечник, печень, легкие, мочевой пузырь и даже в таких редких местах обитания, как евстахиева труба или конъюнктивальный мешок.
Плоскими червями-сосальщиками можно заразиться при употреблении в пищу сырой и непрожаренной рыбы, а также раков. Они могут паразитировать в выводных протоках разных органов, присасываясь к их стенкам.
Размеры сосальщиков бывают от 1 мм до 1,5 м.
Название гельминтам было дано не совсем точное, так как они ничего не высасывают из организма, но вред наносят огромный.
Ленточные черви-паразиты
К плоским червям относится и другой класс — это ленточные черви, которые, в свою очередь, подразделяются на отряды лентецов и цепней.
Эти черви отличаются от круглых червей тем, что имеют промежуточного хозяина, в организме которого развиваются их личинки. Как правило, промежуточными хозяевами становятся рыбы и животные.
Ленточные черви в половозрелом состоянии являются обитателями кишечника позвоночных. На переднем конце тела имеется головка — сколекс, являющаяся органом прикрепления, позади нее — зона роста; тело подразделяется на членики, или проглоттиды. Гермафродит. Кишечник редуцирован.
В связи с этим питание осуществляется всей поверхностью тела паразита пищей, переваренной кишечником хозяина (эндосмотическое питание). Такая среда обитания, как тонкая кишка, подразумевает, что здесь переварится любой подходящий для этого субстрат, но цестоды имеют специфические антиферментные свойства, позволяющие им выживать в условиях высокой ферментной активности. Доказано, что многие гельминты в норме выделяют в течение жизни антикиназу, которая нейтрализует панкреатический сок и тем самым защищает гельминтов от переваривания.
Развитых органов чувств у цестод нет, но имеются чувствительные клетки, пронизывающие своими периферическими отростками поверхность тела паразита. Органы дыхания и кровеносная система отсутствуют.
В мясе рыбы и животных, пораженном ленточными гельминтами, находятся небольшие пузырьки с личинками паразитов. При употреблении зараженных продуктов личинки попадают в организм постоянного хозяина и остаются в кишечнике. Здесь они завершают свое развитие и становятся взрослыми особями.
Наряду со схожими чертами, присущими ленточным червям, имеются и существенные различия между лентецами и цепнями. Это особенно важно в диагностическом плане, когда необходимо проводить идентификацию паразитов.
Для лентецов характерна головка — сколекс с двумя присасывательными ямками или бороздками — ботриями или только с одной ямкой на переднем конце паразита. Матка имеет свое собственное отверстие, что значит, что яйца будут выделяться во внешнюю среду и могут быть обнаружены при исследовании испражнений; яйца с крышечкой.
членики (проглоттиды) цепняЦепни получили свое название из-за внешнего вида. Их характерным внешним признаком является лентовидное тело, разделенное на членики (проглоттиды). Размеры паразитов варьируются от 1 мм до 18 м в длину.
У цепней головка с четырьмя присосками, с помощью которых черви прикрепляются к стенкам кишечника. Далее следует зона роста, или шейка, от которой берут начало членики. По мере роста шейки на ней возникает отчетливая поперечная перетяжка, отделяющая задний участок, превращающийся в проглоттиду.
Матка не имеет выводного отверстия, а значит, яиц в испражнениях обнаружить практически не удается; яйца без крышечки.
При росте гельминта новые членики постепенно отодвигают назад ранее образованные. Таким образом, в передней части тела находятся самые молодые членики, а на конце — старые, самые зрелые.
В процессе перемещения члеников дальше от шейки происходит их созревание, изменяется их форма и внутреннее строение. Молодые членики — самые мелкие. Постепенно их размеры увеличиваются, изменяется их половая система, которой совсем лишены молодые, только что образованные членики. Множество члеников, соединенных друг с другом, напоминают цепочку, в которой может быть от 3 до нескольких тысяч члеников.
Замыкающие цепочку членики содержат яйца паразита, которые по мере созревания постепенно отрываются и выходят наружу. С помощью покрывающих их ресничек яйца передвигаются по кишечнику и через задний проход попадают в окружающую среду.
Как уже говорилось, пищеварительная система у ленточных гельминтов отсутствует, они поглощают пищу всей поверхностью тела.
Ученые объясняют это тем, что цепни паразитируют в тонком кишечнике, где находится уже переваренная и готовая к усвоению пища. Дыхательная и кровеносная системы также отсутствуют, а выделительная и нервная имеют типичное строение.
Характерной особенностью половой системы ленточных червей является многократное повторение мужских и женских половых органов в каждом членике. Благодаря такому строению паразиты обладают колоссальной плодовитостью.
Жизненный цикл ленточных червей протекает со сменой хозяев и с личиночными стадиями. Постоянными хозяевами являются позвоночные животные и человек, а промежуточными — позвоночные и беспозвоночные.
|
Паразиты |
Человек может являться «хозяином» более 2000 видов паразитов, от мельчайших микроорганизмов до метровых глистов. Паразиты живут не только в прямой кишке – их можно обнаружить практически в любой части тела: легких, печени, мышцах, суставах, желудке, пищеводе, мозге, крови, коже и даже в глазах.
Основными симптомами присутствия паразитов являются:
• почти любые хронические заболевания,
• кишечные и желудочные расстройства,
• депрессивные состояния,
• нарушения веса и обмена веществ,
• боли в суставах и мышцах,
• хроническая усталость,
• сбои в работе иммунной системы,
• аллергии, анемия,
• повышенная чувствительность к переменам погоды,
• проблемная кожа,
• скрежет зубами,
• нарушения сна,
• воспаления, бородавки, гранулемы и др.
Toxoplasma gondii - представитель класса кокцидий , паразитирующий у птиц и млекопитающих. Жизненный цикл паразита состоит из двух стадий - бесполой и половой. Промежуточный хозяин (например, человек, мышь, овца, свинья) заглатывает спорулированные ооцисты паразита, содержащие спорозоитов, либо цисты, содержащие цистозоитов. Под действием кислого содержимого желудка оболочка ооцист и цист быстро разрушается. Вышедшие из них спорозоиты и цистозоиты внедряются в эпителий слизистой тонкой кишки и превращаются в эндозоитов - быстро делящиеся формы паразита. Эндозоиты способны размножаться в любых клетках млекопитающих (за исключением эритроцитов). Паразит прикрепляется к клетке и проникает в нее, формируя паразитофорную вакуоль, внутри которой он делится. Размножение продолжается до тех пор, пока число эндозоитов не превысит возможности клетки - в конце концов она лопается, а освободившиеся паразиты проникают в соседние клетки.
Основными симптомами присутствия паразитов являются:
• почти любые хронические заболевания,
• кишечные и желудочные расстройства,
• депрессивные состояния,
• нарушения веса и обмена веществ,
• боли в суставах и мышцах,
• хроническая усталость,
• сбои в работе иммунной системы,
• аллергии, анемия,
• повышенная чувствительность к переменам погоды,
• проблемная кожа,
• скрежет зубами,
• нарушения сна,
• воспаления, бородавки, гранулемы и др.
Toxoplasma gondii - представитель класса кокцидий , паразитирующий у птиц и млекопитающих. Жизненный цикл паразита состоит из двух стадий - бесполой и половой. Промежуточный хозяин (например, человек, мышь, овца, свинья) заглатывает спорулированные ооцисты паразита, содержащие спорозоитов, либо цисты, содержащие цистозоитов. Под действием кислого содержимого желудка оболочка ооцист и цист быстро разрушается. Вышедшие из них спорозоиты и цистозоиты внедряются в эпителий слизистой тонкой кишки и превращаются в эндозоитов - быстро делящиеся формы паразита. Эндозоиты способны размножаться в любых клетках млекопитающих (за исключением эритроцитов). Паразит прикрепляется к клетке и проникает в нее, формируя паразитофорную вакуоль, внутри которой он делится. Размножение продолжается до тех пор, пока число эндозоитов не превысит возможности клетки - в конце концов она лопается, а освободившиеся паразиты проникают в соседние клетки.
|
Мышечные ветви шейного сплетения |
http://studmed.ru/
1. Значительное количество коротких мышечных ветвей начинается непосредственно от передних ветвей отдельных шейных нервов (см. рис. 988, 1001, 1003) и направляется к некоторым мышцам головы, шеи и спины.
К мышцам головы: передняя прямая мышца головы иннервируется от CI(CII); латеральная прямая мышца головы — от CI; длинная мышца головы — от CI — CIII(CIV).
К мышцам шеи и спины: длинная мышца шеи иннервируется от СII — СVI грудино-ключично-сосце-видная мышца — от СII — СIII; передняя лестничная мышца — от (CIV)Cv — CVII(CVIII); средняя лестничная мышца — от (CIII)CIV — СVIII задняя лестничная мышца — от СVII, СIII; мышца, поднимающая лопатку,— от (СII)СIII, CIV, (СV); трапециевидная мышца — от СII — CIV; передние межпоперечные мышцы - от СII - СVII.
2. Шейная петля, ansa cervicalis (см. рис. 989, 999, 1002—1004, 1011), состоит из двигательных волокон передних ветвей шейных нервов, не принимающих участия в образовании шейного сплетения, и образуется верхним и нижним корешками (см. «Соединения шейного сплетения»).
Смешанная ветвь шейного
сплетения
Диафрагмальный нерв, n. phrenicus (СIII), CIV, (CV) (см. рис. 996, 998, 1002—1006, 1065), наряду с большим количеством двигательных волокон имеет чувствительные, следует вниз по передней поверхности передней лестничной мышцы, приближаясь к ее медиальному краю в нижнем отделе шеи, проходит между подключичной артерией и подключичной веной в полость груди, залегая впереди купола плевры и кнутри от него. В грудной полости диафрагмальный нерв располагается в верхнем и среднем средостениях, между плеврой и перикардом, достигая диафрагмы, в которой широко разветвляется.
Расположение правого и левого диафрагмальных нервов неодинаково. Правый диафрагмальный нерв идет более вертикально. В верхних отделах грудной полости он пересекает правую внутреннюю грудную артерию, ложится латерально от правой плечеголовнои вены и верхней полой вены. Далее он располагается между перикардом и медиастинальной плеврой (в сопровождении перикардодиафрагмальных артерии
и вен), впереди корня правого легкого соответственно латеральной стенке правого предсердия. Впереди и латерально от отверстия нижней полой вены правый диафрагмальный нерв достигает диафрагмы.
Левый диафрагмальный нерв идет несколько дугообразно. В верхних отделах грудной полости он пересекает внутреннюю грудную артерию, ложится латерально от дуги аорты; далее располагается впереди корня левого легкого, более поверхностно, чем правый диафрагмальный
нерв. Следуя соответственно латеральной поверхности левого желудочка, позади верхушки сердца, левый диафрагмальный нерв достигает диафрагмы более кпереди и латерально, чем правый.
На своем пути диафрагмальный нерв отдает и получает ряд ветвей.
1. Соединительные ветви в области шеи, со средним и нижним шейными узлами симпатического ствола, а также с нервными сплетениями, окружающими некоторые сосуды (щитошейный ствол, восходящую артерию шеи), с подключичной петлей.
2. Соединительная ветвь с подключичным нервом (СV). Иногда корешки диафрагмального нерва от Cv могут быть настолько длинными, что проникают в полость груди, где на различном уровне соединяются с основным стволом диафрагмального нерва. В таких случаях они получают название добавочных диафрагмальных нервов, nn. phrenici accessorii (см. рис. 1000, 1004).
3. От основного ствола, реже от добавочных диафрагмальных нервов в области корня легкого отходят 2—3 ветви к медиастинальной плевре.
4. Перикардиальные ветви, rr. pericardiaci, сопровождая разветвления перикардодиафрагмальных сосудов, проникают в перикард.
5. Концевыми ветвями основного ствола диафрагмального нерва являются диафрагмальные ветви (см. рис. 1002, 1004, 1006), которые перед внедрением в толщу мышцы разделяются на три ветви: переднюю — в сторону грудинной части диафрагмы, латеральную — в сторону реберной части и заднюю — в сторону поясничной части. Все три ветви проникают в толщу диафрагмы, где, широко разветвляясь, образуют сетевидной формы сплетение. Иногда ветви этого сплетения соединяются с ветвями межреберных нервов. В передних отделах сухожильного растяжения, на границе его с мышечной частью, можно проследить соединительную ветвь между правым и левым диафрагмальными нервами (см. рис. 1005, 1006).
По ходу некоторых ветвей имеется небольшое количество внутриствольных нервных клеток.
6. Диафрагмально-брюшные ветви, rr. phrenicоabdominales (см. рис. 1004), среди которых различают ветви, входящие в состав правого и левого нижних диафрагмальных сплетений [см. «Автономная (вегетативная) часть
нервной системы»]; ветви к печеночному сплетению; ветви к верхнему желудочному сплетению; ветви к брюшине, связкам печени и передней стенке живота.
1004. Нервы диафрагмы; вид сверху (препарат П. Евдокимова).

1005. Нервы диафрагмы плода 8 мес (фотография. Препарат С. Калашниковой).
(Распределение ветвей диафрагмальных нервов; вид сверху.)
1—ствол правого диафрагмалыюго нерва (отрезан); 2—внутримышечное сплетение (образовано вторичными ветвями от передней, наружной и задней ветвей диафрагмального нерва); 3 — задняя ветвь диафрагмального нерва; 4—ветвь к сухожильному центру диафрагмы; 5—боковая (латеральная) ветвь диафрагмального нерва; 6 — ствол левого диафрагмального нерва; 7 — передняя ветвь диафрагмального нерва; 8 — вторичная ветвь; 9—ветвь к межреберному нерву; 10 — ветвь к нижней части перикарда и сухожильному центру; 11 — передняя ветвь диафрагмального нерва; 12 — латеральная ветвь диафрагмального нерва; 13 — задняя ветвь диафрагмального нерва; 14—внутримышечное сплетение; 15—ветвь от чревного сплетения.

1006. Нервы диафрагмы (фотография. Препарат П. Евдокимова).
(Распределение ветвей диафрагмальных нервов в толще диафрагмы; вид сверху.)
1—нижняя левая диафрагмальная артерия и сопровождающее ее нервное сплетение; 2—ствол правого диафрагмального нерва (отрезан); 3 — внутримышечное сплетение (образовано вторичными ветвями от передней, наружной и задней ветвей диафрагмалыюго нерва); 4 — задняя ветвь диафрагмалыюго нерва; 5—ветвь к сухожильному центру диафрагмы; 6—боковая (латеральная) ветвь диафрагмального нерва; 7—ствол левого диафрагмального нерва; 8—передняя ветвь диафрагмального нерва; 9—вторичная ветвь; 10—ветвь к межреберному нерву; 11, 12 — ветви к нижней части перикарда и сухожильному центру; 13—передняя ветвь диафрагмального нерва; 14—латеральные ветви диафрагмального нерва; 15 — задняя ветвь диафрагмального нерва; 16—внутримышечное сплетение; 17 — ветвь от чревного сплетения.
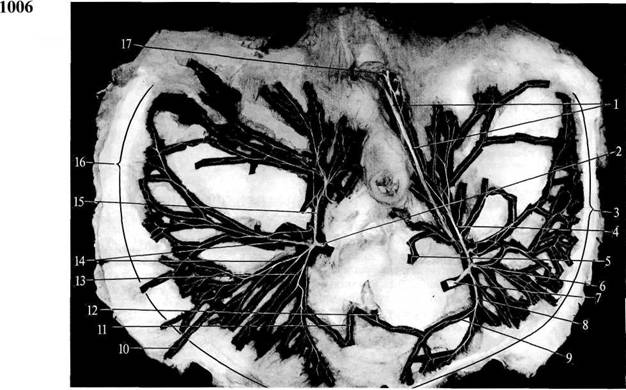
1. Значительное количество коротких мышечных ветвей начинается непосредственно от передних ветвей отдельных шейных нервов (см. рис. 988, 1001, 1003) и направляется к некоторым мышцам головы, шеи и спины.
К мышцам головы: передняя прямая мышца головы иннервируется от CI(CII); латеральная прямая мышца головы — от CI; длинная мышца головы — от CI — CIII(CIV).
К мышцам шеи и спины: длинная мышца шеи иннервируется от СII — СVI грудино-ключично-сосце-видная мышца — от СII — СIII; передняя лестничная мышца — от (CIV)Cv — CVII(CVIII); средняя лестничная мышца — от (CIII)CIV — СVIII задняя лестничная мышца — от СVII, СIII; мышца, поднимающая лопатку,— от (СII)СIII, CIV, (СV); трапециевидная мышца — от СII — CIV; передние межпоперечные мышцы - от СII - СVII.
2. Шейная петля, ansa cervicalis (см. рис. 989, 999, 1002—1004, 1011), состоит из двигательных волокон передних ветвей шейных нервов, не принимающих участия в образовании шейного сплетения, и образуется верхним и нижним корешками (см. «Соединения шейного сплетения»).
Смешанная ветвь шейного
сплетения
Диафрагмальный нерв, n. phrenicus (СIII), CIV, (CV) (см. рис. 996, 998, 1002—1006, 1065), наряду с большим количеством двигательных волокон имеет чувствительные, следует вниз по передней поверхности передней лестничной мышцы, приближаясь к ее медиальному краю в нижнем отделе шеи, проходит между подключичной артерией и подключичной веной в полость груди, залегая впереди купола плевры и кнутри от него. В грудной полости диафрагмальный нерв располагается в верхнем и среднем средостениях, между плеврой и перикардом, достигая диафрагмы, в которой широко разветвляется.
Расположение правого и левого диафрагмальных нервов неодинаково. Правый диафрагмальный нерв идет более вертикально. В верхних отделах грудной полости он пересекает правую внутреннюю грудную артерию, ложится латерально от правой плечеголовнои вены и верхней полой вены. Далее он располагается между перикардом и медиастинальной плеврой (в сопровождении перикардодиафрагмальных артерии
и вен), впереди корня правого легкого соответственно латеральной стенке правого предсердия. Впереди и латерально от отверстия нижней полой вены правый диафрагмальный нерв достигает диафрагмы.
Левый диафрагмальный нерв идет несколько дугообразно. В верхних отделах грудной полости он пересекает внутреннюю грудную артерию, ложится латерально от дуги аорты; далее располагается впереди корня левого легкого, более поверхностно, чем правый диафрагмальный
нерв. Следуя соответственно латеральной поверхности левого желудочка, позади верхушки сердца, левый диафрагмальный нерв достигает диафрагмы более кпереди и латерально, чем правый.
На своем пути диафрагмальный нерв отдает и получает ряд ветвей.
1. Соединительные ветви в области шеи, со средним и нижним шейными узлами симпатического ствола, а также с нервными сплетениями, окружающими некоторые сосуды (щитошейный ствол, восходящую артерию шеи), с подключичной петлей.
2. Соединительная ветвь с подключичным нервом (СV). Иногда корешки диафрагмального нерва от Cv могут быть настолько длинными, что проникают в полость груди, где на различном уровне соединяются с основным стволом диафрагмального нерва. В таких случаях они получают название добавочных диафрагмальных нервов, nn. phrenici accessorii (см. рис. 1000, 1004).
3. От основного ствола, реже от добавочных диафрагмальных нервов в области корня легкого отходят 2—3 ветви к медиастинальной плевре.
4. Перикардиальные ветви, rr. pericardiaci, сопровождая разветвления перикардодиафрагмальных сосудов, проникают в перикард.
5. Концевыми ветвями основного ствола диафрагмального нерва являются диафрагмальные ветви (см. рис. 1002, 1004, 1006), которые перед внедрением в толщу мышцы разделяются на три ветви: переднюю — в сторону грудинной части диафрагмы, латеральную — в сторону реберной части и заднюю — в сторону поясничной части. Все три ветви проникают в толщу диафрагмы, где, широко разветвляясь, образуют сетевидной формы сплетение. Иногда ветви этого сплетения соединяются с ветвями межреберных нервов. В передних отделах сухожильного растяжения, на границе его с мышечной частью, можно проследить соединительную ветвь между правым и левым диафрагмальными нервами (см. рис. 1005, 1006).
По ходу некоторых ветвей имеется небольшое количество внутриствольных нервных клеток.
6. Диафрагмально-брюшные ветви, rr. phrenicоabdominales (см. рис. 1004), среди которых различают ветви, входящие в состав правого и левого нижних диафрагмальных сплетений [см. «Автономная (вегетативная) часть
нервной системы»]; ветви к печеночному сплетению; ветви к верхнему желудочному сплетению; ветви к брюшине, связкам печени и передней стенке живота.
1004. Нервы диафрагмы; вид сверху (препарат П. Евдокимова).

1005. Нервы диафрагмы плода 8 мес (фотография. Препарат С. Калашниковой).
(Распределение ветвей диафрагмальных нервов; вид сверху.)
1—ствол правого диафрагмалыюго нерва (отрезан); 2—внутримышечное сплетение (образовано вторичными ветвями от передней, наружной и задней ветвей диафрагмального нерва); 3 — задняя ветвь диафрагмального нерва; 4—ветвь к сухожильному центру диафрагмы; 5—боковая (латеральная) ветвь диафрагмального нерва; 6 — ствол левого диафрагмального нерва; 7 — передняя ветвь диафрагмального нерва; 8 — вторичная ветвь; 9—ветвь к межреберному нерву; 10 — ветвь к нижней части перикарда и сухожильному центру; 11 — передняя ветвь диафрагмального нерва; 12 — латеральная ветвь диафрагмального нерва; 13 — задняя ветвь диафрагмального нерва; 14—внутримышечное сплетение; 15—ветвь от чревного сплетения.

1006. Нервы диафрагмы (фотография. Препарат П. Евдокимова).
(Распределение ветвей диафрагмальных нервов в толще диафрагмы; вид сверху.)
1—нижняя левая диафрагмальная артерия и сопровождающее ее нервное сплетение; 2—ствол правого диафрагмального нерва (отрезан); 3 — внутримышечное сплетение (образовано вторичными ветвями от передней, наружной и задней ветвей диафрагмалыюго нерва); 4 — задняя ветвь диафрагмалыюго нерва; 5—ветвь к сухожильному центру диафрагмы; 6—боковая (латеральная) ветвь диафрагмального нерва; 7—ствол левого диафрагмального нерва; 8—передняя ветвь диафрагмального нерва; 9—вторичная ветвь; 10—ветвь к межреберному нерву; 11, 12 — ветви к нижней части перикарда и сухожильному центру; 13—передняя ветвь диафрагмального нерва; 14—латеральные ветви диафрагмального нерва; 15 — задняя ветвь диафрагмального нерва; 16—внутримышечное сплетение; 17 — ветвь от чревного сплетения.

|






