Стирол. Структуры полимеров |
Большую часть стирола (около 85 %) в промышленности получают дегидрирование мэтилбензола при температуре 600—650°С, атмосферном давлении и разбавлении перегретым водяным паром в 3 — 10 раз. Используются оксидные железо-хромовые катализаторы с добавкой карбоната калия.
Другой промышленный способ, которым получают оставшиеся 15 %, заключается в дегидратации метилфенилкарбинола, образующегося в процессе получения оксида пропилена из гидропероксида этилбензола. Гидропероксид этилбензола получают из этилбензола некаталитическим окислением воздуха.
Схехма анионоидной полимеризации стирола:
|
Метки: стирол полистирол полимеры структура полимеров сетчатая структура полимера |
Строение, свойства и применение кремнийорганических полимеров |
Задание 445(ш)
Какие соединения называют элементорганическими, кремнийорганическими? Укажите важнейшие свойства кремнийорганических полимеров. Как влияет на свойства кремнийорганических полимеров. увеличение числа органических радикалов, связанных с атомом кремния?
Решение:
Элементоорганическая химия, зародившаяся на стыке неорганической и органической химии, знаменует собой интеграцию химии на современном этапе и определяет прогресс химической науки в целом.
|
Метки: кремнийорганические соединения элементорганические соединения силаны полиорганосилоксаны |
Полимерное действие генов |
Задача 1
Сын белой женщины и негра женился на белой женщине. Может ли ребёнок от этого брака быть темнее своего отца?
Решение:
Так как полимерные гены в одинаковой степени оказывают влияние на развитие одного и того же признака, то иногда их обозначают одинаковыми буквами алфавита с указанием цифрового индекса, например: А1А1А2А1
— негры..., а1а1а2а1 — белые. Но нам кажется, что удобнее обозначать двумя разными буквами.
Используем таблицу №1.
|
Метки: полимерные гены гены генетика мулаты белый мулат полимерное действие генов |
Задачи по генетике на эпистаз |
Задача 1
При скрещивании растений одного из сортов тыквы с белыми и желтыми плодами все потомство F1 имело белые плоды. При скрещивании этого потомства между собой в их потомстве F2 было получено:
• 207 растений с белыми плодами,
• 54 растения с желтыми плодами,
• 18 растений с зелеными плодами.
Определить возможные генотипы родителей и потомства.
|
Метки: генетика эпистаз генотипы родителей расщепление при эпистазе |
Монозиготные и дизиготные близнецы |
Близнецами называют одновременно родившихся детей. Монозиготные (однояйцевые) близнецы развиваются из одной зиготы — оплодотворенной яйцеклетки, причем в оплодотворении яйцеклетки принимает участие только один сперматозоид. Обычно из зиготы развивается один зародыш. Но иногда после первого митотического деления два бластомера отделяются друг от друга и начинают самостоятельное развитие: из каждого бластомера формируется обособленный от другого зародыш, в результате чего у матери рождаются два ребенка, одинаковые по полу, генотипу и фенотипу. Имеющиеся у них очень незначительные различия обусловлены небольшими наследственными и не наследственными изменениями, которые возникают в их соматических клетках в ходе индивидуального развития.
|
Метки: дизиготные близнецы близнецы монозиготные близнецы антропогенетика |
Близнецовый метод антропогенетики |
Задача 1
Конкордантность монозиготных близнецов по массе тела составляет 80%, а дизиготных близнецов – 30%. Каковы доля наследственности и доля среды в формировании этого признака.
Решение:
Рассчитаем долю участия наследственности и долю участия внешней среды в развитии изучаемого признака по массе тела:
1. Рассчитаем коэффициент наследуемости признака по формуле Хольцингера:
|
Метки: близнецовый метод антропогенетика конкордантность коэффициент коркондартности близнецы |
Определение рН раствора соли | Гидролиз соли |
Задание 216.
Какая из двух солей при равных условиях в большей степени подвергается гидролизу: NaCN или NaClO; MgCl2 или ZnCl2? Почему? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
Решение:
а) NaCN и NaClO – соли сильного однокислотного основания NaOH и слабых кислот соответственно HCN и HClO гидролизуются по аниону:
CN- + H2O ⇔ HCN + OH-;
ClO- + H2O ⇔ HClO + OH-.
При равных условиях гидролизу в большей степени будет подвергаться соль, у которой константа диссоциации кислоты, образующая соль, будет меньшей, т. е. гидролизу в большей степени подвергается соль, образованная относительно менее сильной кислотой. Так как КD(HCN) < КD(HClO) [КD(HCN) = 7,9 . 10-10; КD(HClO) = 5,01 . 10-8], следовательно, гидролизу в большей степени будет подвергаться NaCN.
|
Метки: гидролиз гидролиз соли гидролиз соли сильного основания гидролиз соли сильной кислоты |
Пероксид водорода в окислительно-восстановительных реакциях |
Задание 325
Какие свойства может проявлять пероксид водорода в окислительно-восстановительных реакциях? На основании электронных уравнений напишите уравнения реакций Н2О2: а) с Аg2O;б) с КI.
Решение:
В пероксиде водорода Н2О2 кислород находится в своей промежуточной степени окисления -1, поэтому в зависимости от условий он может быть как восстановителем (когда увеличивает свою степень окисления атом кислорода), так и окислителем (когда атом кисло-рода уменьшает свою степень окисления). Например:
а) Н2О2 + Ag2O = 2Ag + O2 + H2O
Уравнения электронного баланса:
|
Метки: пероксид пероксид водорода диспропорционирование самоокисление самовосстановление |
Получение и полимеризация стирола. Схемы линейной и трехмерной структуры полимеров |
Задание 449 (ш)
Как получают в промышленности стирол? Приведите схему его полимеризации. Изобразите с помощью схем линейную и трехмерную структуры полимеров.
Решение:
Получение и полимеризация стирола
Большую часть стирола (около 85 %) в промышленности получают дегидрирование мэтилбензола при температуре 600—650°С, атмосферном давлении и разбавлении перегретым водяным паром в 3 — 10 раз. Используются оксидные железо-хромовые катализаторы с добавкой карбоната калия.
Другой промышленный способ, которым получают оставшиеся 15 %, заключается в дегидратации метилфенилкарбинола, образующегося в процессе получения оксида пропилена из гидропероксида этилбензола. Гидропероксид этилбензола получают из этилбензола некаталитическим окислением воздуха.
|
Метки: стирол полистирол структуры полимеров трехмерная структура полимеров линейная структура полимеров полимеры |
Популяционная генетика |
Задача 2
Система групп крови Кидд определяется аллельными генами Ik и Ik. Ген Ik является доминантным по отношению к гену Ik и лица, имеющие его, являются кидд-положительными. Частота гена Ik среди населения г. Кракова составляет 0,458 (В. Соха, 1970). Частота кидд-положительных людей среди негров составляет 80% (К. Штерн, 1965). Определите генетическую структуру популяции г. Кракова и негров по системе Кидд.
Решение:
Оформляем условие задачи в виде таблицы:
|
Метки: генетика популяционная генетика кистозный фиброз популяция альбинизм закон Харди—Вайнберга |
Жесткость воды и методы ее устранения |
Задание 341
Какую массу Na3PO4 надо прибавить к 500 л воды, чтобы устранить ее карбонатную жесткость, равную 5 ммоль/л? Ответ: 136,625 г.
Решение:
Молярная масса эквивалента Na3PO4 = M/3 = 163,945/3 = 54,65 г/моль. Жёсткость воды выражается суммой миллиэквивалентов ионов Са2+ и Mg2+, содержащихся в 1 л воды (моль/л). В 500 л воды содержится 500 . 5 = 2500 моль солей, обуславливающих жёсткость воды. Для устранения жёсткости следует прибавить 2500 .54,65 = 136625 мг или 136,625 г Na3PO4.
|
Метки: жесткость воды карбонатная жесткость |
Правильное решение расчетных типовых задач по химии |
В наиболее сложных задачах, в дополнение к вычислениям по теме «растворы», предполагается расчет по уравнению реакции. Приведен пример решения задачи на приготовление растворов ацетальдегида, а также дана задача на приготовление раствора формалина.
Задача 1.
В результате гидратации ацетилена объемом 67,2 л (н.у.) можно получить водный раствор ацетальдегида с массовой долей 15% . Масса полученного раствора равна ... г. (запишите число с точностью до целых).
Дано:
объем ацетилена (н.у.): V(С2Н2) = 67,2 л;
массовая доля ацетальдегида в растворе:  (Н3С-НС=О) = 15%.
(Н3С-НС=О) = 15%.
Найти: массу раствора: mр-ра = ?
Решение:
М(Н–НС=О) = 30 г/моль.
1. Записываем уравнение реакции и рассчитываем по нему массу образовавшегося ацетальдегида:
|
Метки: задачи по химии химия егэ приготовление раствора раствор массовая доля плотность раствора |
Расчеты по термохимическому уравнению |
Задача 1.
При сгорании 560 мл (н.у.) ацетилена согласно термохимическому уравнению:
2С2Н2(Г) + 5О2(г) = 4СО2(Г) + 2Н2О(Г) + 2602,4 кДж
выделилось:
1) 16,256 кДж; 2) 32,53кДж; 3) 32530 кДж; 4) 16265кДж
Дано:
объем ацетилена: V(С2Н2) = 560 мл.
Найти: количество выделившейся теплоты.
Решение:
Для выбора верного ответа удобнее всего провести расчет искомой в задаче величины и сравнить ее с предлагаемыми вариантами. Расчет по термохимическому уравнению ничем не отличается от расчета по обычному уравнению реакции. Над реакцией мы указываем данные в условии и искомые величины, под реакцией — их соотношения согласно коэффициентам. Теплота представляет собой один из продуктов, поэтому ее числовое значение мы рассматриваем как коэффициент.
|
Метки: теплота образования термохимия количество теплоты теплота |
Термопластичность, термореактивность, три состояния полимеров |
|
Метки: полимеры термопласты реактопласты термопластичность термореактивность |
Составление и анализ родословных |
Задача 1
Болезнь наследуется по аутосомно-рецессивному типу. Пробанд болен, и его родословная имеет следующий вид:

Рис. 1. Графическое изображение родословной по аутосомно-рецессивному типу наследования признака.
Жена пробанда здорова и не содержит в своем генотипе патологических аллелей. Чему равна вероятность рождения у пробанда здорового ребенка?
Решение здесь:
|
Метки: анализ родословных составление родословных пробанд генотип пробанда |
Эквивалент. Эквивалентная масса. Молярная и относительная атомная массы |
Задача 15.
Избытком хлороводородной (соляной) кислоты подействовали на растворы: а) гидрокарбоната кальция;
б) дихлорида гидроксоалюминия. Напишите уравнения реакций этих веществ с HCl и определите количество вещества эквивалентов и молярные массы эквивалента.
Решение:
а) Уравнение реакции:
2HCl + Ca(HCO3)2 = CaCl2 + 2H2O + 2CO2↑
Молярная масса эквивалента кислоты равна её молярной массе делённой на основность (число атомов водорода, содержащихся в молекуле кислоты), значит, МЭ(HCl) = 1/1M(HC). Молярная масса эквивалента сложного вещества, как и молярная масса эквивалента элемента, может иметь различные значения и зависит от того, в какую реакцию обмена вступает это вещество. В данной реакции два эквивалента соляной кислоты реагирует с двумя эквивалентами гидрокарбоната калия. Следовательно, Э(Ca(HCO3)2) равно 2, а эквивалентная масса Ca(HCO3)2 в реакции (а) будет равна МЭ(Ca(HCO3)2)/2 = 162/2 = 81 г/моль.
б) Уравнение реакции:
HCl + AlOHCl2 = AlCl3 + H2O
В данной реакции 1 моль HCl реагируют с 1 моль AlOHCl2, значит, число веществ эквивалентов AlOHCl2равно 1. Так как AlOHCl2 взаимодействует с одной молекулярной массой эквивалента (молекулой) HCl в реакции (б), то её молярная масса эквивалента равна МЭ(AlOHCl2)/1 = 114,886/1 = 114,886 г/моль.
Задание 16.
При окислении 16,74 г двухвалентного металла образовалось 21,54 г оксида. Вычислите молярные массы эквивалента металла и его оксида. Чему равны молярная и относительная атомная массы металла?
Решение:
Учитывая, что МЭ(МеО) = МЭ(Ме) + МЭ(О), находим молярную массу эквивалента оксида металла, получим:
МЭ(МеО) = 27,9 + 8 = 35,9 г/моль.
Молярная масса металла определяется из соотношения МЭ = А/В, где МЭ – молярная масса эквивалента металла; А – молярная масса металла; В – стехиометрическая валентность элемента;
А = МЭ . В = 27,9 . 2 = 55,81 г/моль.
Так как относительная атомная масса в а. е. м. численно равна относительной молярной массе, выраженной в г/моль, то искомая масса металла равна 55,81 а. е. м.
Ответ: 27,9 г/моль; 35,9 г/моль; 55,8 1 /моль; 55,8 а.е.м.
Задание 17.
При взаимодействии 3,24 г трехвалентного металла с кислотой выделяется 4,03 л водорода (н.у.). Вычислите молярную массу эквивалента, молярную и относительную атомную массы металла.
Решение:
Объём, занимаемый при данных условиях молярной массой эквивалента газообразного вещества, называется молярным объемом эквивалента этого вещества. Молярный объём любого газа при н. у. равен 22,4 л. Отсюда эквивалентный объём водорода VЭ(Н2), молекула которого состоит из двух одновалентных атомов водорода, т.е. содержит два моля атомов водорода, равен 22,4/2 = 11,2 л [VЭ(Н2) = VM/2 =22,4/2 = 11,2].
Согласно закону эквивалентов массы (объёмы) реагирующих веществ m1 и m2 пропорциональны их молярным массам (объёмам):

VЭ(Н2) – эквивалентный объём водорода; V(H2) – объём водорода.
Тогда
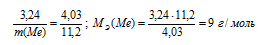
Молярная масса металла определяется из соотношения МЭ = А/В, где МЭ – молярная масса эквивалента металла; А – молярная масса металла; В – стехиометрическая валентность элемента; А = МЭ . В = 9 . 3 = 27 г/моль.
Так как относительная атомная масса в а. е. м. численно равна относительной молярной массе, выраженной
в г/моль, то искомая масса металла равна 27 а. е. м.
Ответ: 9 г/моль; 27 г/моль; 27а. е. м.
|
Метки: эквивалент молярная масса эквивалента относительная атомная масса |
Количество вещества эквивалента. Молярная масса эквивалента |
Задание 12.
Напишите уравнение реакций Fе(ОН)3 с хлороводородной (соляной) кислотой, при которых образуются следующие соединения железа: а) хлорид дигидроксожелеза; б) дихлорид гидроксожелеза; в) трихлорид железа. Вычислите количество вещества эквивалента и молярную массу эквивалента Fе(ОН)3 в каждой из этих реакций.
Решение:
а); Fe(OH)3 + HCl = Fe(OH)2Cl + H2O;
б) Fe(OH)3 + 2HCl = FeOHCl2 + 2H2O;
в) Fe(OH)3 + 3HCl = FeCl3 + 3H2O
Молярная масса эквивалента сложного вещества, как и молярная масса эквивалента эле-мента, может иметь различные значения и зависит от того, в какую реакцию обмена вступает это вещество. Молярная масса эквивалента основания равна молярной массе (М), делённой на число гидроксильных групп, замещённых в данной реакции на металл (на число вступающих в реакцию гидроксильных групп). Следовательно, эквивалентная масса Fe(OH)3 в реакции (а) М(Fe(OH)3)/1 = 106,84/1 = 106,84 г/моль, в реакции (б) - М(Fe(OH)3)/2 = 106,84/2 = 53,42 г/моль, а в реакции (в) - М(Fe(OH)3)/3 = 106,84/3 = 35,61 г/моль.
Подробнее здесь: http://buzani.ru/
|
Метки: эквивалент молярная масса эквивалента |
Контрольная работа |
Нужна контрольная работа по общей химии, обращайтесь http://buzani.ru
|
Метки: химия задачи по химии |
Контрольные работы по химии |
|
Метки: химия |
Дневник bakan |

|
|






